Esetismertetések / Case reports
The use of extracorporal immunomodulatory treatments in acute gastroenterological disorders
Summary
Among acute, life-threatening gastroenterological disorders, severe acute pancreatitis and acute liver failure are high-mortality diseases, and their treatment remains a challenge today. In both cases, significant cell damage occurs and, in addition, frequently associated infections may result in an excessive immune response, a “cytokine storm”. Since attempts to control this condition using medication therapy have not been successful enough, extracorporal techniques are more often preferred. Of cytokine absorbers, CytoSorb is the most widely used agent globally, which can also be combined with other extracorporeal organ replacement treatments. This paper presents our current therapeutic options and experiences based on two cases.
Az akut, életet veszélyeztető gasztroenterológiai kórképek közül a súlyos akut pancreatitis és az akut májelégtelenség magas mortalitású kórképek, kezelésük napjainkban is kihívást jelent. Mindkét kórkép esetén jelentős sejtkárosodás jön létre, ezen felül a gyakran társuló infekció is túlzott immunválaszt, „citokinvihart” eredményezhet, amelynek kontrollálására a gyógyszeres próbálkozások nem jelentettek kellő hatékonyságú megoldást, ezért az extracorporalis technikák kerültek előtérbe. A citokin-adszorberek közül a CytoSorb alkalmazásával van jelenleg világszerte a legtöbb tapasztalat, amely kombinálható egyéb extracorporalis szervpótló kezelésekkel is. Két esetünk kapcsán szeretnénk bemutatni a jelenlegi terápiás lehetőségeinket, illetve tapasztalatainkat.
A szervezetet érintő káros hatások (pl. infekció, toxinok, trauma, autoimmun folyamatok) a sejtekből felszabaduló DAMP-ok, illetve a kórokozók által prezentált PAMP-ok révén az innate immunrendszer gyors aktivációját eredményezik, ami citokinek termelődéséhez és szisztémás gyulladás (SIRS) kialakulásához vezet. A koordinált citokinszekréció szükséges a gazdaszervezet megfelelő immunválaszának felépítéséhez és a kiváltó trigger megszűnését követően annak terminálásához. A pro-(pl. IL-1, IL-6, TNF-a) és antiinflammatorikus (pl. IL-4, IL-10) citokinek arányának felborulása, az immunválasz diszregulációja, citokinvihart eredményezhet, ami életet veszélyeztető hiperinflammációval jár. Ezáltal a kezdetben lokális gyulladás szisztémássá válhat és többszervi elégtelenséget (MODS), majd halált okozhat (1, 2).
Extracorporalis immunmoduláció
A hiperinflammáció kontrollálására a gyógyszeres próbálkozások (pl. TLR-4-antagonisták, anti IL-1R, anti-IL-1b, anti-TNF, és anti-LPS) annak ellenére, hogy szignifikánsan csökkentették egyes citokinek koncentrációját, nem jelentettek kellő hatékonyságú megoldást, ezért napjainkban egyre inkább az extracorporalis technikák felé terelődik a figyelem (2). Ezen vértiszítási technikák egyik alapelve az adszorpció, amely nemcsak egy citokint, hanem a citokinek és egyéb molekulák egész spektrumát képes megkötni. Több ilyen adszorberrel folynak vizsgálatok, (pl. Toraymyxin, oXiris), de jelenleg az egyik legelterjedtebb a CytoSorb hemoadszorpiós oszlop. A CytoSorb különböző méretű és oldalláncú, biokompatibilis porózus polimer gyöngyökből áll, amelyek nagy (45 000 m2!) felületet képeznek, ezáltal lehetővé válik az átáramoltatott vérből az 5-60 kDa méretű molekulák megkötése. A citokinek nagy része ebbe a tartományba tartozik, de hatékonyan képes a bilirubin, epesavak, ammónia, egyes toxinok és gyógyszerek szintjét is csökkenteni (3–5). Az adszorber működéséhez antikoaguláció, illetve folyamatos vérátáramoltatás szükséges, amelyet valamilyen pumparendszerrel összekapcsolt zárt extracorporalis kör – pl. folyamatos vesepótló-kezelés (CRRT) – biztosít. CytoSorb kezeléssel legtöbb adat szepszis, illetve kardiopulmonalis bypass műtétek kapcsán van, a lehetséges indikációs kör azonban gyorsan bővül (6–10). Számos különböző etiológiájú, de súlyos szisztémás gyulladásos válaszreakcióval járó kórkép pl. égés, rhabdomyolysis, intoxikációk, trauma, pancreatitis, ALF-ACLF esetén vannak kedvező tapasztalatok, bár ezek főként esetriportok, nagy esetszámú, randomizált, kontrollált vizsgálatok még hiányoznak (11–15). Közleményünkben 2 betegünk esetét mutatjuk be, akiknél CytoSorb kezelést alkalmaztunk.
Esetbemutatások
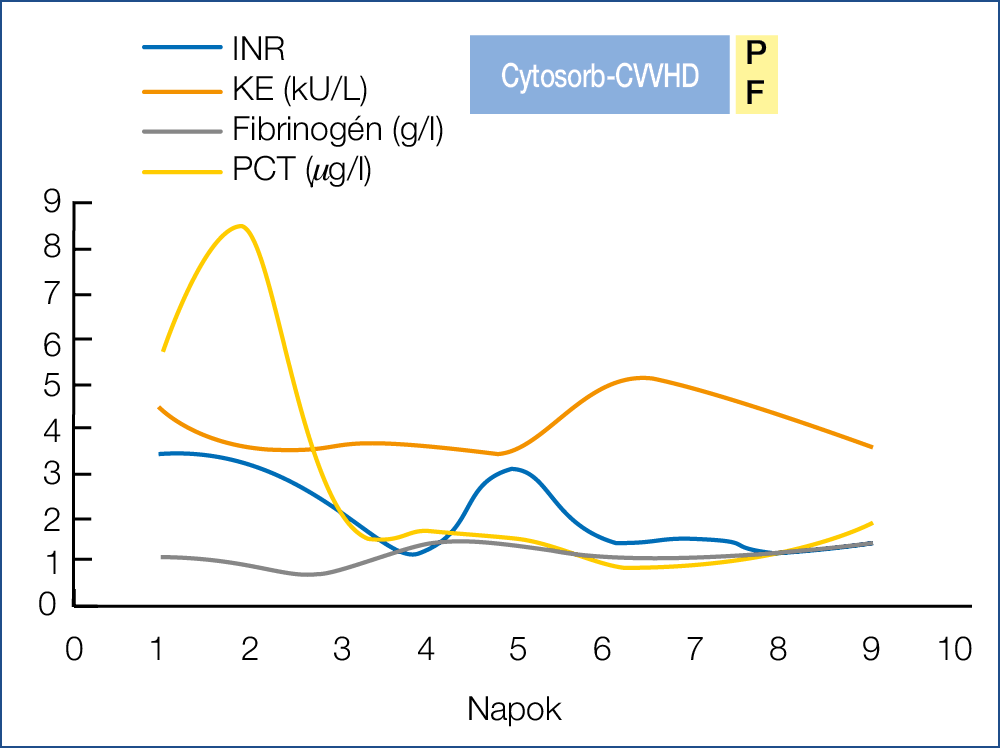
Első betegünk egy 23 éves nő volt, akinek anamnézisében nagyobb betegség nem szerepelt. A beteg területi kórházba került felvételre zavartság, hányás, hetek óta jelentkező gyengeség, fáradékonyság, fogyás miatt. Felvételekor súlyos diabéteszes ketoacidózist észleltek. Másnap hasi fájdalom jelentkezett, akut pancreatitis igazolódott, harmadnap szepszis, majd 4. napra akut májkárosodás és DIC alakult ki, ekkor került átvételre klinikánk intenzív osztályára. A lege artis elkezdett oki és szupportív terápia (sav-bázis és vércukorháztartás rendezése, folyadék és albuminpótlás, nasojejunalis táplálás, imipenem-cilastatin antibiotikum, trombózisprofilaxis) mellett javulást nem sikerült elérnünk, így a 4. napon 72 órás CVVHD-CytoSorb kezelést indítottunk citrát antikoagulálással. Az 1. ábrán látható, hogy a bilirubinérték jelentősen csökkent a CytoSorb kezelés elindítását követően, azonban valószínűleg az adszorber telítődése miatt ez csak átmeneti javulás volt. A hepatikus encephalpathia a CytoSorb CVVHD-kezelést követően továbbra is 2. stádiumú volt, ezért egy alkalommal plazmaferezis történt (10E FFP), amelyet követően az encephalopathia javult, majd 2 nap múlva meg is szűnt. A per os táplálást is ezt követően tudtuk elkezdeni. A 1. ábrán látható továbbá, hogy a májenzimek a kezelés megkezdését követően jelentősen csökkentek. Javultak a máj szintetikus kapacitását jelző paraméterek, mint az INR, kolinészteráz, fibrinogénszint, illetve a gyulladásos marker PCT is (2. ábra).
1.ábra: Biokémia paraméterek változása Cytosorb-CVVHD és plasmaferesis (10E FFP) kezelés során (1. eset)
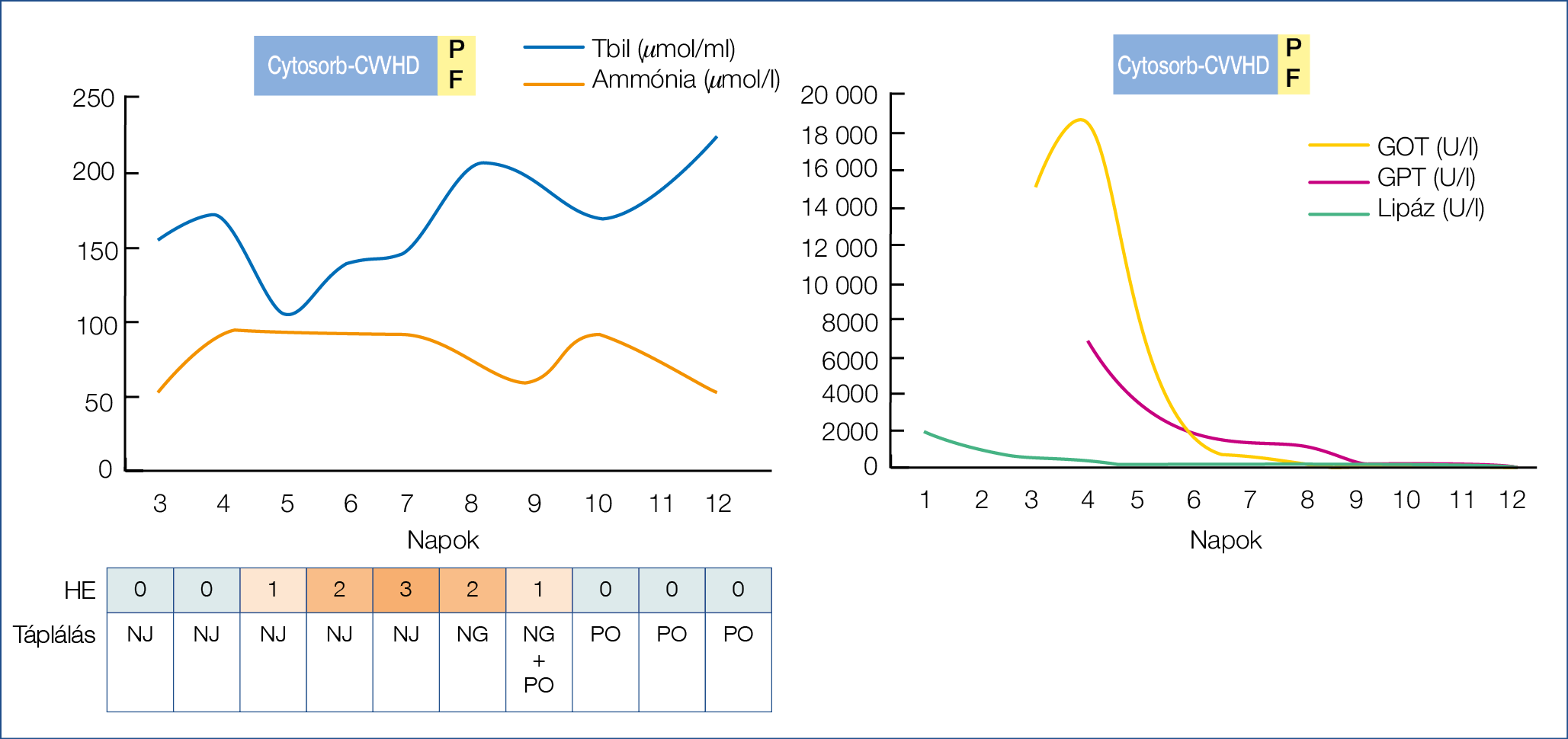
Ezt követően a beteg állapota, laborparaméterei folyamatosan javultak, 1-es típusú diabetes mellitus miatt inzulinkezelést állítottunk be, ápolása 30. napján otthonába tudtuk bocsátani. A májfunkciós értékek teljes normalizálódásához még további 3 hónapra volt szükség.
2. ábra: A gyulladásos és májfunkciós értékek változása (1. eset)
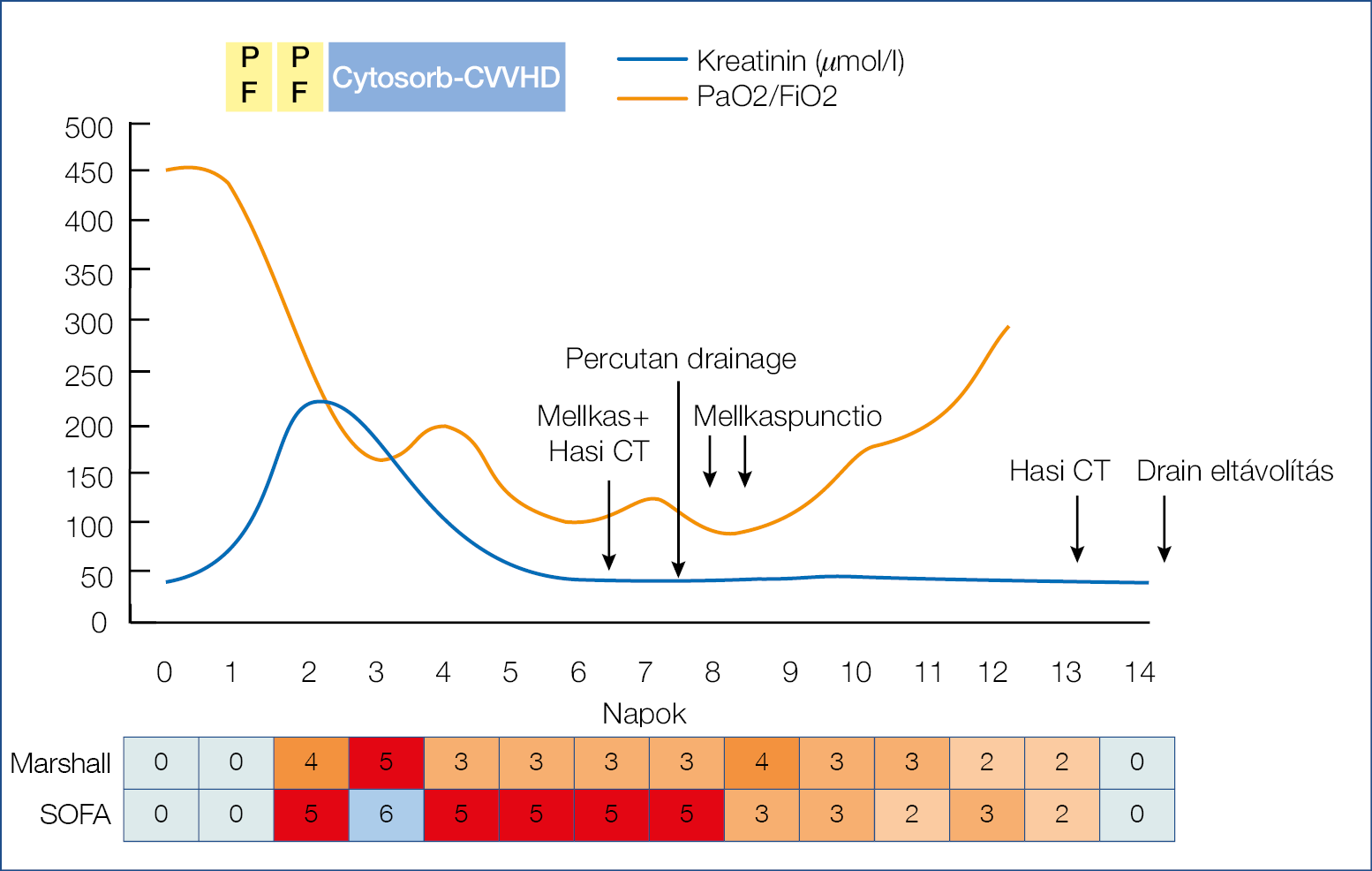
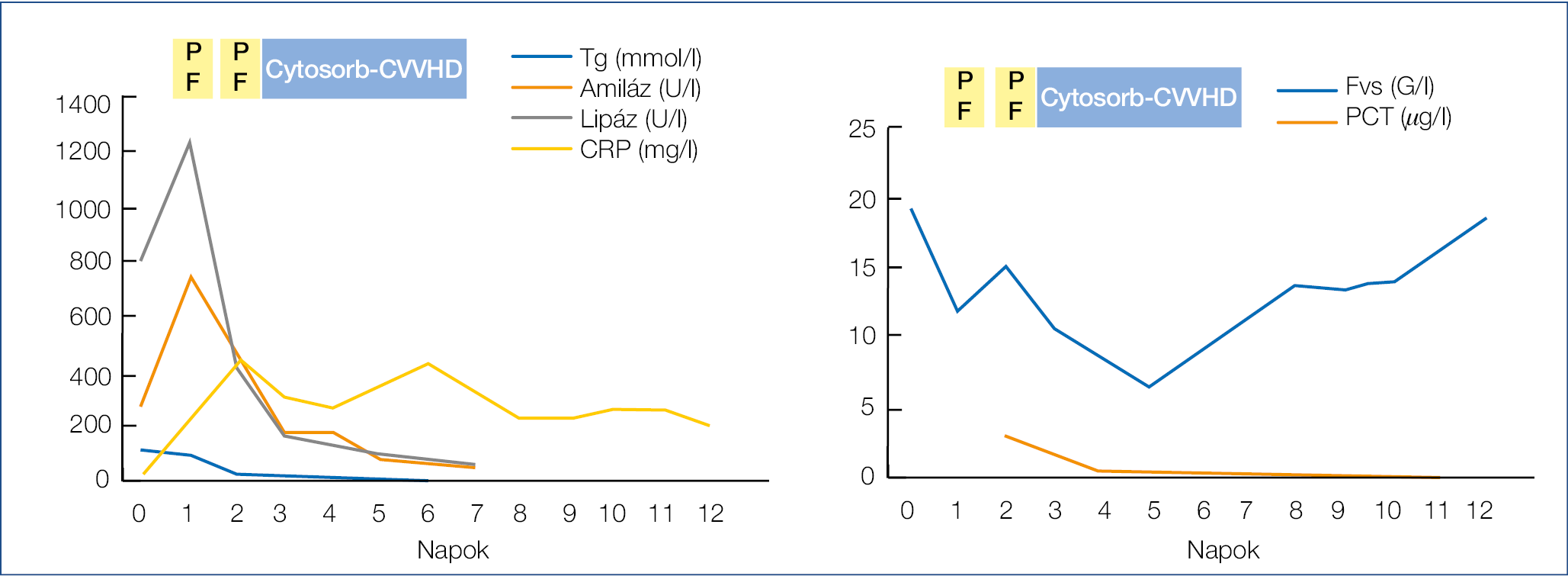
Második betegünk egy 51 éves hipertóniás nő – akinek édesanyja 39 éves korában akut pancreatitisben halt meg – hypertrigliceridaemia (Tg: 109 mmol/l) indukálta súlyos akut pancreatitis miatt került felvételre, intenzív osztályunkra. Felvételét követően komplex kezelésben részesült (folyadékreszuszcitáció, analgetikum, ulcus profilaxis, kolonoszkópos detenzionálás), a trigliceridszint csökkentése céljából Na-heparin és inzulinkezelést kezdtünk, majd 2 alkalommal terápiás plazmaferezis történt albuminpótlással, amely hatékonyan csökkentette a trigliceridszintet (Tg: 8 mmol/l). Ezzel párhuzamosan az amiláz- és lipázszintek is csökkentek, azonban ez a szervdiszfunkciók (vese, tüdő) kialakulását nem akadályozta meg, ezért a 2. napon 72 órás CytoSorb-CVVHD-kezelést indítottunk. A beteg hemodinamikailag végig stabil volt. A 3. ábrán látható, hogy a gyulladásos markerek csak a CytoSorb kezelés elindítását követően kezdtek csökkenni. Az 4. ábrán a súlyosságot jelző Marshall és SOFA score-ok változása látható, illetve nyilakkal jelöltük a fő diagnosztikus és terápiás beavatkozásokat. A plazmaferezis maximális szupportív kezelés mellett sem akadályozta meg a többszervi diszfunkció kialakulását, azonban CytoSorb-CVVHD-kezelés mellett a vesefunkció jelentősen javult, majd normalizálódott. A légzési elégtelenség több komponensből állt, egyrészt a magas rekeszállás, kiterjedt dystelectasia, kezdődő ARDS, illetve fokozatosan növekvő mennyiségű mellkasi folyadékgyülem okozta. A légzési elégtelenség súlyosságát jelző PaO2/FiO2 arány esetén van egy kisebb javulás a CytoSorb kezelés alatt, azonban a gépi lélegeztetés elkerüléséhez a hasűri nyomás csökkentésére és a pankreatogén mellkasi folyadékgyülem két alkalommal történő lebocsátására is szükség volt. Ezt követően szervelégtelenség tünetei megszűntek, a pancreatitis komplex kezelését folytattuk (tartós jejunális táplálás, CT-vezérelt drenázs, antibiotikum), amelynek eredményeként az intraabdominális folyadékgyülemek mérete jelentősen csökkent, sebészeti beavatkozásra nem volt szükség, a beteget ápolása 28. napján otthonába tudtuk engedni.
3. ábra: A gyulladásos markerek, trigliceridszint és pancreas enzimek változása a kezelés során (2. eset)
4. ábra: A szervdiszfunkciót jelző paraméterek változása a kezelések során (2. eset)
Megbeszélés
A CytoSorb-kezeléssel kombinált CVVHD, illetve plazmaferezis mindkét beteg estében jelentős javulást eredményezett. A Cytosorb alkalmazásával nemcsak a gyulladásos markerek szintje csökkent, hanem májelégtelenség esetén a májenzim, ammónia és átmenetileg a bilirubinértékek is. Súlyos akut pancreatitis esetén a kombinált kezelés a szervdiszfunkciók javulását eredményezte. CytoSorb alkalmazásával legtöbb tapasztalat szepszis, illetve kardiopulmonalis bypass műtétek kapcsán áll rendelkezésre, azonban egyre több adat utal arra, hogy bridging kezelésként szolgálhat akut májelégtelenségben a májműködés regenerálódásáig, vagy a májtranszplantációig (14, 16, 17).
A kezeléssel kapcsolatban számos kérdés merül fel, többek között még nem tisztázott pontosan az indikációja, elindításának optimális időpontja, módja, időtartama. Gasztroenterológiai szempontból súlyos akut pancreatitis, ALF-ACLF területén várhatóak további eredmények (18, 19). Összegzésként elmondható, hogy az extracorporalis modalitások célzott, kombinált alkalmazásával gyakran olyan kórképek is gyógyíthatók, ahol a komplex patológia egyedi támadáspontjainak a kezelése önmagában nagy valószínűséggel nem járna sikerrel, azonban az egymásra épülő kezelésekkel sikert érhetünk el.

2. Bonavia A, et al. Clinical Utility of Extracorporeal Cytokine Hemoadsorption Therapy: A Literature Review. Blood Purif 2018; 46(4): 337–349. https://doi.org/10.1159/000492379
3. Gruda MC, et al. Broad adsorption of sepsis-related PAMP and DAMP molecules, mycotoxins, and cytokines from whole blood using CytoSorb(R) sorbent porous polymer beads. PLoS One 2018; 13(1): e0191676. https://doi.org/10.1371/journal.pone.0191676
4. Taniguchi T. Cytokine adsorbing columns. Contrib Nephrol 2010; 166: 134–141. https://doi.org/10.1159/000314863
5. Gemelli C, et al. Removal of Bilirubin with a New Adsorbent System: In Vitro Kinetics. Blood Purif 2019; 47(1–3): 10–15. https://doi.org/10.1159/000492378
6. Kogelmann K, et al. Hemoadsorption by CytoSorb in septic patients: a case series. Crit Care 2017; 21(1): 74. https://doi.org/10.1186/s13054-017-1662-9
7. Hawchar F, et al. Extracorporeal cytokine adsorption in septic shock: A proof of concept randomized, controlled pilot study. J Crit Care 2019; 49: 172–178. https://doi.org/10.1016/j.jcrc.2018.11.003
8. Honore PM, et al. Cytokine removal in human septic shock: Where are we and where are we going? Ann Intensive Care 2019; 9(1): 56. https://doi.org/10.1186/s13613-019-0530-y
9. Poli EC, et al. Cytokine clearance with CytoSorb(R) during cardiac surgery: a pilot randomized controlled trial. Crit Care 2019; 23(1): 108. https://doi.org/10.1186/s13054-019-2399-4
10. Nemeth E, et al. Impact of intraoperative cytokine adsorption on outcome of patients undergoing orthotopic heart transplantation-an observational study. Clin Transplant, 2018. 32(4): e13211. https://doi.org/10.1111/ctr.13211
11. Berkes A, et al. Use of Hemadsorption in a Case of Pediatric Toxic Shock Syndrome. Case Rep Crit Care 2017; ID 3818407. https://doi.org/10.1155/2017/3818407
12. Tomescu D, et al. Clinical effects of hemoadsorption with CytoSorb((R)) in patients with severe acute pancreatitis: A case series. Int J Artif Organs 2019; 42(4): 190–193. https://doi.org/10.1177/0391398818823762
13. Buttner S, et al. Application of Hemoadsorption in a Case of Liver Cirrhosis and Alcohol-Related Steatohepatitis with Preexisting Hepatitis C Infection. Blood Purif 2017; 44(1): 30–31. https://doi.org/10.1159/000455064
14. Dhokia VD, et al. Novel use of CytoSorb haemadsorption to provide biochemical control in liver impairment. J Intensive Care Soc 2019; 20(2): 174–181. https://doi.org/10.1177/1751143718772789
15. Angheloiu AA, Angheloiu GO. Removal of dabigatran using sorbent hemadsorption. Int J Cardiol 2019. https://doi.org/10.1177/1751143718772789
16. Tomescu DR, et al. First report of cytokine removal using CytoSorb(R) in severe noninfectious inflammatory syndrome after liver transplantation. Int J Artif Organs 2016; 39(3): 136–40. https://doi.org/10.5301/ijao.5000489
17. Frimmel S, et al. Cytokine adsorption is a promising tool in the therapy of hemophagocytic lymphohistiocytosis. Int J Artif Organs 2019: 391398819857444. https://doi.org/10.1177/0391398819857444
18. Huber W, et al. Pancreatitis cytosorbents (CytoSorb) inflammatory cytokine removal: A Prospective Study (PACIFIC). Medicine (Baltimore) 2019; 98(4): e13044. https://doi.org/10.1097/md.0000000000013044
19. Friesecke S, et al. International registry on the use of the CytoSorb(R) adsorber in ICU patients : Study protocol and preliminary results. Med Klin Intensivmed Notfmed 2017. https://doi.org/10.1007/s00063-017-0342-5