Orvostörténet / History in medicine
History of breath tests in gastroenterology
Summary
Although apparently simple both for patients and for physicians and nurses, the history of breath tests is as long as the medicine itself. The first knowledge on the role of air and its composition occurred in antiquity. Understanding the mechanism of respiration and tests for lung functions developed in the second half of the 19th century. Due to progress in basic sciences and medical technology, there have been many developments (labeled isotope tests, chromatography, mass spectrometry and combinations thereof, ion-selective sensors, electronic nose): some of these discoveries were awarded by Nobel Prize and later incorporated in the modern equipment’s. Consequently, today’s gastroenterology became enriched with accurate breath tests, which are complementary to or even replace invasive examinations.
Bármily egyszerűnek tűnnek mind a betegek, mind az orvosok és szakasszisztensek számára, a kilégzési tesztek története évszázadokra vezethető vissza. Az első ismeretek a levegő szerepéről és összetételéről az ókorból származnak. A légzés élettani ismeretei és a légzésfunkciós tesztek a 19. század második felében alakultak ki. A mai értelemben vett kilégzési tesztek az alapkutatások és az orvosi technológia fejlődése révén jelentek meg a 20. század második felében: a módszerek kifejlesztésében számos Nobel-díjas tudós vett részt (jelzett izotópos vizsgálatok, kromatográfia, tömegspektrometria és ezek kombinációja, ionszenzitív műszerek, elektronikus orr). Ennek következtében a modern gasztroenterológia olyan pontos kilégzési tesztekkel gyarapodott, amelyek az invazív vizsgálatokat sikeresen helyettesítik és kiegészítik.
Bevezetés
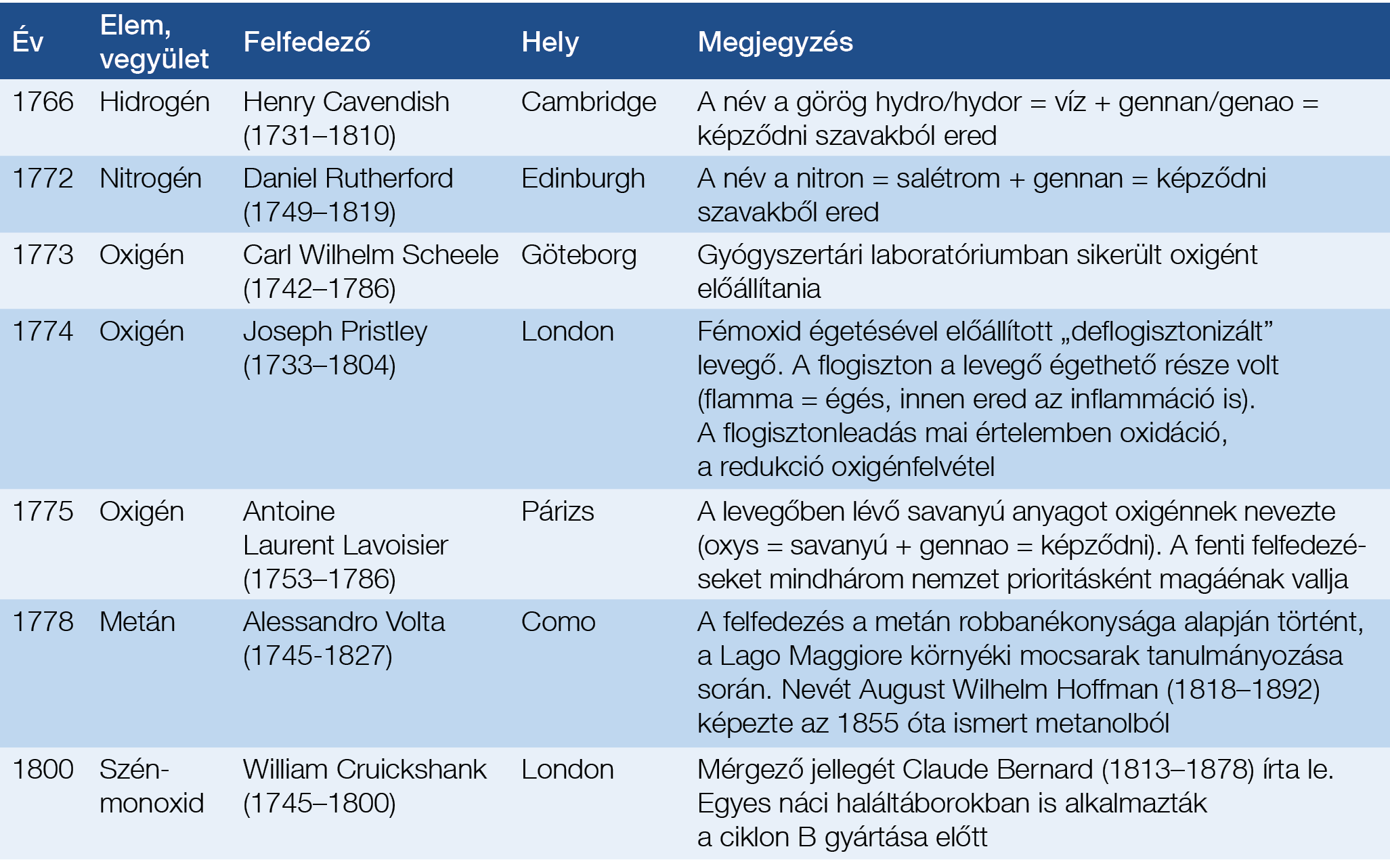
A gasztroenterológiában használt kilégzési tesztek olyan légzésfunkciós vizsgálatok, amelyek az emésztőszervek anyagcseréjéről adnak tájékoztatást. Az élő szervezetek létének alapfeltétele a levegő. Az ókori görögöknél Eraszisztratosz (Kr. e. 304–250) az alexandriai anatómiai iskola megalapítója szerint a levegő, azaz a pneuma a tüdőből a véredényeken át a szívbe kerül, ahol vitális szellemmé alakul és szétoszlik a szervekben. Véleménye ellentmondott Hippokrátesz (Kr. e. 460–377) humoralista szemléletének. Galénosz (Kr. u. 129–200) azonban tanait elfogadta és a római Athénaiosz (Kr. u. 50 körül?–?), megalapította a pneumatikus iskolát: szerintük a belélegzett és a bőrön át felvett levegő tartja egyensúlyban a szervezet működését: ez a szemlélet 1500 évig fennmaradt (1, 2). A levegő kémiai összetevőit a 18. század második felében fedezték fel jelezve, hogy globalizáció már akkor is volt (1. táblázat) (3, 4).
A mai kilégzési tesztek a levegő kémiai összetételét mérik a gázelemzés módszereivel (izotópdiagnosztika, kromatográfia, tömegspektrometria, izotópszelektív elektródok) (5, 6).
Izotópdiagnosztika
A radioizotópok felfedezése a modern atomfizika kialakulásának idején történt. Megkerülhetetlen személyisége Hevesy Károly György (1885–1966), aki 1923–1940 között kidolgozta a radioaktív nyomjelzés módszerét. Első kísérletében a természetben előforduló 212Pb izotóppal sikerült a babnövény gyökerét, levelét és termését megjelölni és kimutatni.
1. táblázat: A kilélegzett levegő összetevőinek története (2, 4)
Munkájáért 1944-ben fizikai Nobel-díjban részesült (7). A 14C izotópot 1940-ben fedezték fel a kaliforniai egyetem sugárfizikai laboratóriumában. A diagnosztikai célokra alkalmas gammakamerát 1958-ban Berkeleyben tervezték és Chicagóban gyártották 1958-ban: ennek kompakt, miniatürizált változatai találhatók a mai kilégzési készülékekben.
Kromatográfia
A vegyületek első kromatográfiás vizsgálatát Mihail Szemjonovics Cvet (1872–1919) orosz botanikus végezte 1900-ban: kalcium-karbonátos adszorbenssel és éter/alkoholos oldószerrel a klorofilt és karotenoidokat különített el. 1941-ben John Porter Martin Archer (1910–2002) és Richard Laurence Millington Synge (1914–1994) a papíralapú módszert fejlesztették tovább: ezzel a Leeds-i egyetemen sikerült aminosavakat szeparálni (kémiai Nobel-díj, 1952). Az oszlopkromatográfiát amerikai biokémikusok 1950-ben dolgozták ki a Rockefeller Intézetben (2).
Ionszelektív elektródok és szenzorok
Az elektród kifejezést Michael Faraday (1791–1867) az elektron = sugár, borostyánkő + hodos = út görög szavakból alakította ki (2, 3). Azon felületeket jelenti, amelyekbe elektromos áram hatol be vagy hagyja el. Az elektródok kifejlesztése a 20. század elején történt. 1906-ban mutatták ki, hogy egy üvegmembrán két oldalán keletkező feszültségkülönbség arányos a hidrogénionok koncentrációjával. 1909-ben Sören P. L. Sørensen (1868–193) vezette be a pH fogalmát és ugyanabban az évben német fizikusoknak sikerült az első üvegelektródot készíteni. 1922-ben hidrogénre érzékeny alkáli-szilikát elektródot készítettek (2). A biokémiai vizsgálatokra alkalmas üveg minielektródot 1925-ben készítette a londoni egyetem Élettani intézetében Phyllis Margaret Tookey Kerridge (1900–1940) (aki úttörő munkát végzett a most annyira aktuális lélegeztetőgépek kifejlesztésében is) (8).
Tömegspektrometria
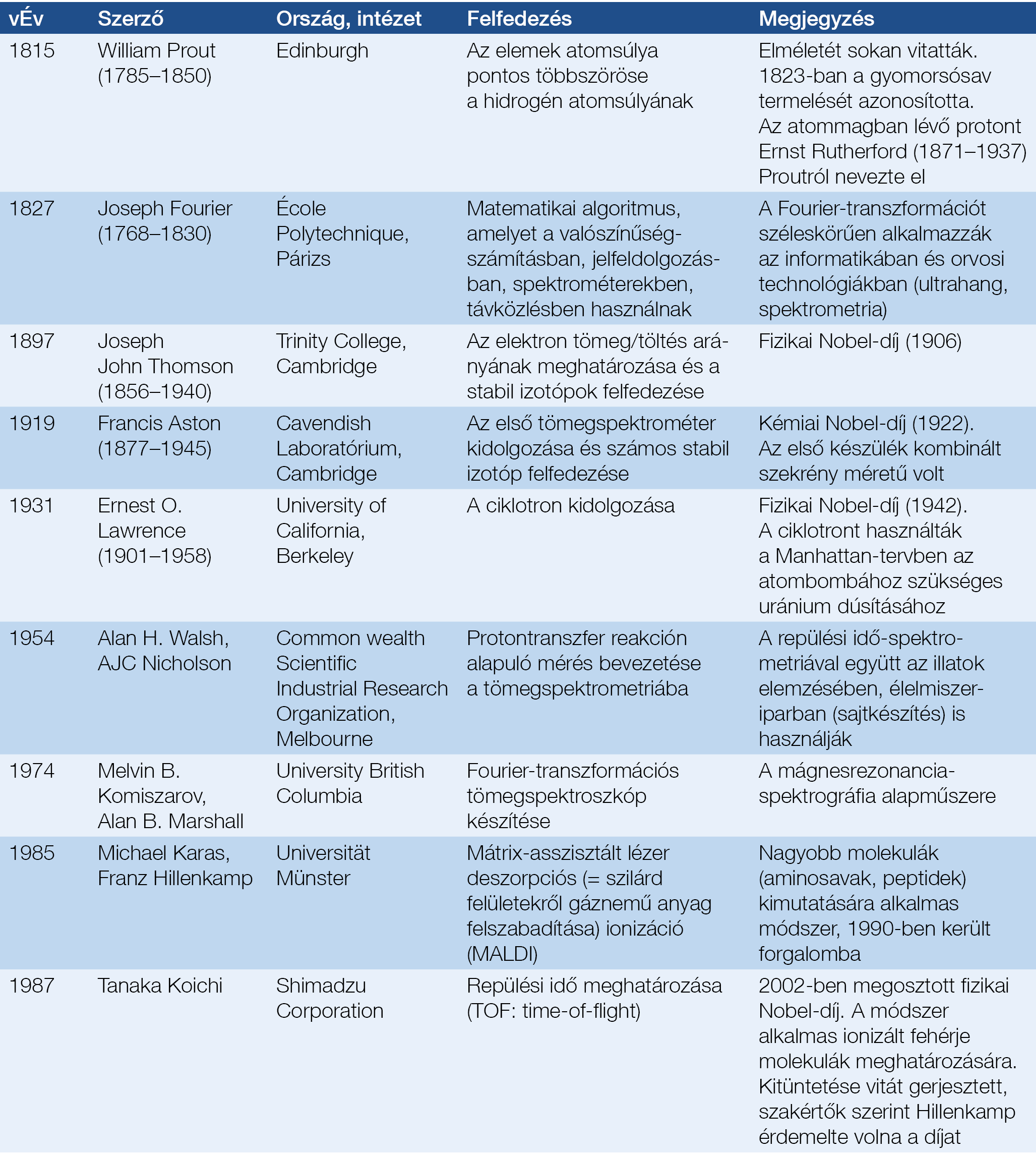
Története a 19. század elejéig vezethető vissza. Az ismeretek fejlődése a 2. táblázatban olvasható. A 2020-as évekre a tömegspektrometria modern változatai előtérbe kerültek és a radioaktív anyagok használatát néhány kivétellel háttérbe szorították, helyüket átvették a stabil izotópos vizsgálatok (3. táblázat).
Gasztroenterológiai kilégzési tesztek
Történetileg az első kilégzési teszt maga a fizikális vizsgálat: az orvos észleli a beteg leheletének szagát, amelyből következtethet kóros folyamatokra. A kellemetlen lehelet kezelésére az Ebers-papiruszban (Kr. e. 1500 körül) mézet, mirhát és fahéjat ajánlottak. Hippokratész szájöblítést és vörösbort javasolt. A Talmudban a szájbűzt fogyatékosságnak tartották és válóoknak tekintették. A halitus latinul leheletet, párát, a halitosis bűzös leheletet jelent (3). A foetor oris/foetor ex ore szájbűzt jelent, Aulus Cornelius Celsustól (Kr. e. 25–Kr. u. 50) származik. Hepatológusok a foetor hepaticus alapján a májelégtelenséget felismerik, diabetológusoknak az acetonszag utal az anyagcsere-kisiklásra.
Az emberi emésztőtraktusban lévő hidrogént és metánt 1816-ban mutatta ki guillotinnal kivégzett emberek boncolása során a párizsi Hôtel Dieu Kórház orvosa, François Magendie (1783–1855) (2). Az 1890-es évektől számos közleményben beszámoltak arról, hogy az eructatioval gyúlékony gázok ürülnek: leírták egy angol úr esetét, aki pipájának gyújtása alatt böfögött és a kiürült levegő lángra kapott (10, 11). Hasonló „baleseteket” írtak le a korabeli aneszteziológusok a betegek altatása közben, bélműtétek alatt, illetve gastrocolicus fisztulás betegeknél. Katonaságnál, zárt intézetekben közismert tréfa a flatus meggyújtása.
Jelzett izotópos vizsgálatok
Az anyagcsere végtermékei a széndioxid és a víz, így kézenfekvőnek tűnt, hogy a 14C izotóp azonosítása után jelzett CO2-ot használjanak a tápanyagok, gyógyszerek, vegyszerek lebomlásának és kiürülésének tanulmányozására. A szénnek 15 közül a 12C és 13C stabil, orvosi felhasználásra a 14C került, fizikai felezési ideje 5700 év, kozmikus sugárzás hatására keletkezik és bekerülve a levegőbe, biológiailag hasznosul és kimutatható. 1949-ben patkányban mérték meg először a 14C-vel jelzett acetát, bikarbonát és szukcinát kiválasztását. Emberben 1962-ben tanulmányozták először a jelzett zsírok felszívódását 14C mérésével a kilélegzett levegőből (12). Kezdetben közepes láncú triglicerideket jeleztek, de azok lebomlás nélkül is felszívódnak, ezért áttértek a hosszú láncú trigliceridek használatára. Számos jelzett zsírsav, triglicerid, epesav, koleszterin, galaktóz, ribóz került kereskedelmi forgalomba: ma már legtöbbjüknek van stabil 13C izotópos változata (12).
2. táblázat: A tömegspektrometria kialakulásának története (2, 9)
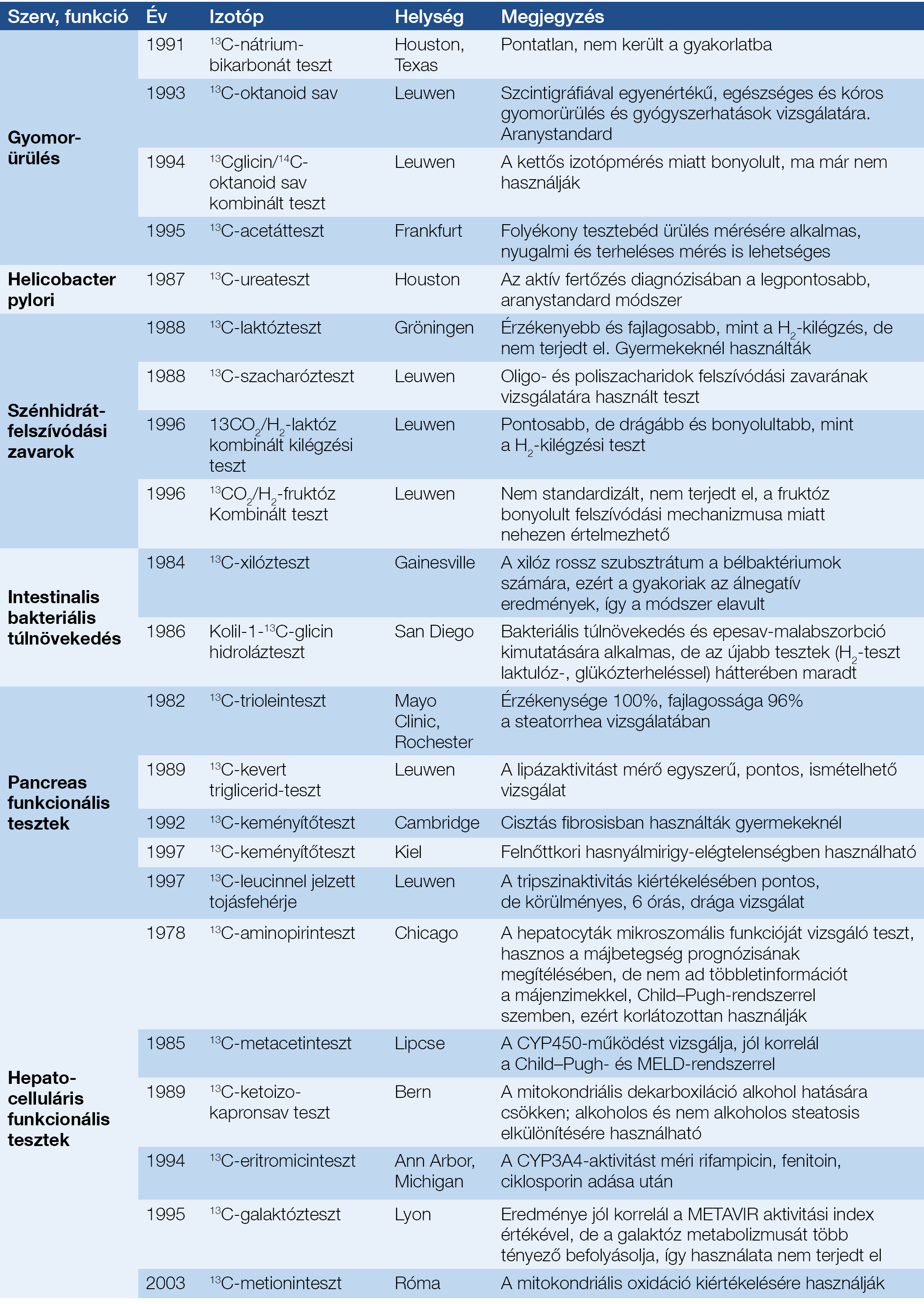
3. táblázat: Stabil izotópos kilégzési tesztek a gasztroenterológiában (33, 34)
Tejcukor-érzékenységben 1964-ben mutatták ki gyermekekben (!!!), hogy jelzett laktóz adása után a 14CO2 ürítése a kilélegzett levegőben csökkent (13): ezt 1975-ben felnőtteken is igazolták 5 mCi 14C-vel jelzett 50 g laktóz adásával, kidomborítva előnyeit a laktóztolerancia-teszt, laktázaktivitás mérése, a vékonybél röntgenvizsgálata, sőt, a H2-kilégzés eredményeivel szemben (12).
A 14C használatával felmerült a biztonságosság kérdése. Az izotóp kis energiájú béta-részecskéket sugároz, ami potenciálisan veszélyes. A vizsgálatokban 5-10 mCi-nél kisebb adag a pontosság rovására megy. 1955-ben végzett tanulmányban 10 uCi adása 70 kg súlyú emberben 400 nap alatt 15 mrad sugárzást okozott, amely eltörpül a kozmikus sugárzás 1200 mrad értéke mellett (14). Normális enterohepatikus keringésű egyéneknél a diagnosztikában használt jelzett vegyületek mindegyike hamar kiürül a szervezetből. Bár a radioaktív izotópok diagnosztikai használatáról sosem derült ki, hogy rákkeltő vagy magzatkárosító hatásuk van, manapság a legtöbb tudományos fórum korlátozott használatuk mellett foglal állást.
Ureakilégzési-teszt
Az ammónia jelenléte a gyomorban 1852-től ismert. A gyomor ureázt 1924-ben írta le James Murray Luck (1899–1993) Cambridge-ben, kimutatva, hogy a portális vér ammóniatartalma 50-100-szor magasabb, mint az artériás véré (15). Élettani szerepét 1951–1954 között macskákon végzett kísérletekkel mutatta ki 14C és 15N segítségével az angliai Sheffieldben Henry L Kronberg és munkatársai (16).
Évtizedekig úgy vélték, hogy az enzimet a nyálkahártya termeli, de 1968-ban igazolták, hogy a csíramentes állatokban nem termelődik ureáz (17). A Helicobacter pylori ureáztermelését 1984-ben mutatták ki. 1988-ban Barry J Marshall és munkatársai dolgozták ki a 14C-urea kilégzési tesztet, amely világszerte elterjedt (18). A kezdeti 10 μCi 14C adagja 1-2 μCi-re csökkent és az 90%-ban 72 óra alatt kiürül a szervezetből. Terhességben a foetalis sugáradag 0,31 mrad, amely töredéke a háttérsugárzás 5000 mrad értékének. Javasolták a kilégzési teszt utáni gyakori vizelést, ezáltal gyorsul az izotóp ürülése (19).
A 14C mérése 15-20-szor olcsóbb, mint a tömegspektrometria és ma rendelkezésre áll hordozható, járóbeteg-ellátásra/háziorvosi rendelőbe is telepíthető mérőműszer. Pontos, de hátránya, hogy csak minőségi (pozitív/negatív), mennyiségi eredményt nem ad, így a fertőzés intenzitásának becslésére nem alkalmas. Hazánkban előbb a svéd Orexo AB, majd Kibion-Malloy francia–német cég készülékét az Izinta Kft. forgalmazza.
A stabil 13C-vel jelzett urea kimutatásának módszerét Houstonban David Y. Graham és munkatársai dolgozták ki (20). Meghatározásához tömegspektrometria, izotóp-szelektív infravörös spektrometria vagy lézerasszisztált spektrometria szükséges. Érzékenysége, fajlagossága és pontossága révén a fertőzés non-invazív diagnosztikai módszereinek aranystandardja, de drága, mert a mérőműszer és az izotóp dúsítása költséges. Hazánkban Gervain Judit 1997-ben Székesfehérvárott tömegspektrométerrel végezte az első vizsgálatokat, a fővárosban a II. kerületi Önkormányzat Egészségügyi Szolgálatánál, illetve az 1993-ban alapított Izinta Kft-nél szerezték be az első izotóp-szelektív infravörös spektrométert (Wagner Analysentechnik, Bréma, Németország, ma szintén a Kibionhoz tartozik). Mózsik Gyula munkacsoportja Pécsett igazolta, hogy a teszt pontossága meghaladja a szövettan és az ureáz gyorsteszt eredményeit (21).
Vizelet 15NH4-teszt
1990-ben Lipcsében a 13C-ureateszt alternatívájaként dolgoztak a vizeletben ürülő, a jelzett ammónia mérését. A vizsgálat élettani elve ugyanaz: a 15N-nel jelzett urea Helicobacter pylori hatására lebomlik, a CO2 a levegővel, a 15NH4 a vizelettel ürül. A teszt hasonló pontosságúnak bizonyult, mint a kilégzési vizsgálat és elsősorban epidemiológiai célra, de a gyakorlatban soha nem terjedt el (22).
Hidrogénkilégzési teszt (H2-teszt)
Egyetlen emberi sejt sem képes a H2 termelésére: kizárólagos forrása a bélben a bakteriális anaerob fermentáció. Közismert, hogy a bab fogyasztása fokozott bélgázképződéssel jár, így 1961-ben babtermesztéssel foglalkozó amerikai kutató önkénteseknél kromatográfiával mutatta ki, hogy bab fogyasztása után a kilélegzett levegőben hidrogén jelenik meg (12). 1966–68 között egy babtermesztő vállalat támogatásával a Stanford kutatóintézetben a levegőből és a flatusból mérték meg kromatográfiával babkonzerv fogyasztása után a hidrogén-, metán- és oxigéntermelődést (23). 1968-ban többlumenű szondával kimutatták, hogy laktóz adagolása esetén a H2-termelés a colon teljes hosszában kimutatható: 2 g laktózból 1,5 ml/perc H2 szabadul fel, amelynek 21%-a a levegőn át ürül (25). A mérések gázkromatográfiával történtek és az értékek alsó határa 10-20 ppm volt. 1981-ben a Quintron amerikai cégnél dolgozták ki a hidrogénspecifikus szolid szenzort, amely világszerte elterjedt (26). A hidrogén domináns bélgáz, mellette a metán, kénhidrogén és más illó vegyületek mennyisége eltörpül.
Magyarországon a H2-kilégzési tesztet elsőként Beró Tamás Pécsett (27), Bodánszky Hedvig a fővárosi I. sz. Gyermekklinikán (28), Herszényi László és munkatársai a II. sz. Belgyógyászati Klinikán honosították meg (29).
A mai diagnosztikában használt, laktóz-, laktulóz-, glükózkilégzési tesztek közös hátránya, hogy sem a tesztanyag adagja, sem a vizsgálati idő nem standardizált:
ennek egységesítésére 2017-ben amerikai (30), majd 2018-ban magyar állásfoglalás született (31). A tesztértékeket befolyásolja a beteg életkora, neme, légzésfunkciója, sav-bázis egyensúlya, szénhidrát-anyagcseréje és vesefunkciója, de az egyszerűség kedvéért a küszöbértékek megállapításánál ezeket nem veszik figyelembe.
Metánkilégzési teszt
Az emberi sejtek a metán előállítására sem képesek. A bélben található CH4 bakteriális eredetű (Methanobrevibacter smithii és Methanosphaera stadtmanae). A metánképző baktériumok az egészséges egyének 30-60%-ában vannak jelen. A bélből a metán passzívan felszívódik a vérbe, de mivel gáznemű, nem kötődik sem sejtekhez, sem albuminhoz, hanem a gázcserével kiürül. A bélbaktériumok a metánt a bélben képződött hidrogén felhasználásával termelik, ezért ahol túlszaporodnak, a H2-kilégzési teszt álnegatív lehet. A kilélegzett metán mennyisége nagyságrenddel kisebb a hidrogénénél, 2-4 ppm érték között van (32).
Stabil szénizotópos kilégzési tesztek
A 12C és 13C természetes aránya 93:1, ezért a diagnosztikában használt 13C-vel jelzett vegyületekhez az izotópot dúsítani kell: ehhez a tömegspektrometriát, lézeres és ionizált izotópszelekciós módszereket használnak. Ezek az urán dúsításához használt, az atombomba gyártásának korszakából származó eljárásokból erednek.
A 13C-alapú kilégzési teszteket a 3. táblázatban ismertetjük. Legtöbbjük eredetileg 14C-vel jelzett tesztanyaggal készült, amikoris a vegyületek sorsát állatkísérletekben és emberben is meghatározták. A 13C-tartalmú tesztanyagok gyógyszernek minősülnek, engedélyezésük 1-2 éves költséges folyamat. Közös jellemzőjük, hogy drágák, de a maguk alkalmazási területén számos invazív vizsgálati módszert váltanak ki (33, 34). A 3. táblázatban feltüntetett számos teszt közül mára csak a 13C-urea- és 13C-oktanoát- tesztet használják széleskörűen.
Kilélegzett illó szerves vegyületek kimutatása
Amerikai szerzők 1895-ben feltételezték, hogy a kilélegzett levegőben megjelenhetnek mérgező szerves anyagok (35). 1911-ben német kémikus észlelte, hogy a kilélegzett levegő gátolja a guajak oxidációját: úgy vélte, hogy ez egy fehérje bomlásterméke, amely zsúfolt hálószobák alvás utáni levegőjében található. Az illó szerves vegyületek kimutatására (angolul volatile organic compounds, VOC) csak a kromatográfia és a tömegspektrometria megjelenése után nyílt lehetőség.
Elsőként 1971-ben Linus Carl Pauling (1900–1994) (Nobel-díj 1954) 250 párolgó vegyületet mutatott ki gázkromatográfiával kilélegzett levegőből és vizeletből: ma már több ezer ismert (36). A tömegspektrometria elterjedése után a két módszert sikerült kombinálni és további fejlesztések révén (2D-technika, gyors detektorok, repülési idő és protontranszfermérés) (2. táblázat) kellően érzékeny műszerek állnak rendelkezésre: ezeket a környezeti szennyeződések mérésére, az illatszeriparban és a terrorellenes védekezésben használják. Orvosi, diagnosztikai mérésekre fejlesztett készülék még nincs (37). Az ún. elektronikus orr- érzékeny szenzorokat alkalmaz a VOC kimutatására: erre ma olcsó, hordozható műszerek állnak rendelkezésre, de hátrány, hogy nem tudják elkülöníteni az egyes vegyületeket.
A fenti módszerekkel 256 vegyületet mutattak ki daganatos betegek levegőmintáiból. Egy 2019-es metaanalízisben 63 tanulmányban tüdő-, emlő-, vastagbél-, szájüregi, máj-, prosztata- és pajzsmirigyrákos betegnél történtek vizsgálatok. A leggyakrabban kimutatott vegyületek az aromás és alifás szénhidrátok, aldehidek, alkohol, fenolok, karboxisavak, éterek és furánok voltak (8 butanon, 1-propanol, izoprén, etilbenzén, 4-metiloktán, aceton, toluén, etanol, pentán) (37). Szemben a H2-kilégzéssel, ahol az eredményt részecske/millió (ppm, parts per million) fejezik ki, VOC esetében nagyságrendekkel kisebb értékekről van szó (részecske/milliárd, ppb = parts per billion, sőt, részecske/trillió, ppt = parts per trillion, ami 10–12/mol/l koncentrációnak felel meg). Colorectalis rákban az aceton, etilacetát, etanol és 4-metiloktánszint magasabb volt, mint kontrollegyéneknél és a vizsgálat érzékenysége 85%, fajlagossága 92%, pontossága 91% (38). Hasnyálmirigyrákban a formaldehid, pentán, aceton, izopropilakohol-, hexán- és benzaldehidszint volt magasabb (39). Az optimista szakemberek a VOC mérését a jövőben mind szűrővizsgálatként, mind a daganatos betegek kezelésének követésében javasolják.
Magyarországon az Országos Korányi Pulmonológiai Intézetben és a Semmelweis Egyetem Pulmonológiai klinikáján, nemzetközi együttműködésben végeztek VOC-meghatározást tüdőbetegek részére (40).
Következtetések
A gasztroenterológiában használt kilégzési tesztek abból a szükségszerűségből alakultak ki, hogy, az invazív diagnosztikai beavatkozásokat helyettesítsék. A légzés élettanának tanulmányozása a légzésfunkciós vizsgálatokhoz vezetett, ezeknek származékai a mai kilégzési tesztek. Az atomfizika, a technológia és az informatika fejlődésével a kilélegzett levegő összetételének elemzésére alkalmas készülékek jelentek meg. A folyamatra jellemző a globalizáció és a szimultaneitás, azaz egy kutatási-fejlesztési témát egyszerre több országban, azonos időszakban tanulmányoztak, ez pedig előbb-utóbb fejlődéshez, újabb és újabb tesztek bevezetéséhez vezetett, bár a gyakorlatban nem mindegyik váltotta be a hozzá fűzött reményeket.
Köszönetnyilvánítás
Az irodalomkutatásért Oláh Ilona (Semmelweis Egyetem, Élettani Intézet), a szövegszerkesztésért Józan Jolán, az angol összefoglaló lektorálásért Douglas Arnott úr (EDMF Translations, Budapest) munkáját illeti köszönet.
2. Sebastian A. A Dictionary of the History of Medicine. New York-London: The Parthenon Publishing Group; 1999. pp. 148, 591, 626, 680.
3. Lozsádi K. Etymologia medica. Orvosi szótörténeti tár. Budapest: Medicina Könyvkiadó Rt.; 2006.
4. Balázs L. A kémia története. Budapest: Nemzeti Tankönyvkiadó; 1996. I. kötet, p. 287–304.
5. Pembrey MS. Chemistry of respiration, in: Text-Book of Physiology, szerk. Schäfer EA, Young J Pentland, Edinburgh&London: 1898. I. kötet, p. 692–784.
6. Henter L, Holbok S. Orvosi műszerek és készülékek. Budapest: Műszaki Könyvkiadó; pp. 1982, 78–84.
7. Hevesy G. LIII: The absorption and translocation of lead by plants. A contribution to the application of the method of radioactive indicators in the investigation of the changed of substance in plants. Biochem J 1923; 17: 439–445.
doi: https://doi.org/10.1042/bj0170439.
8. Tookey Kerridge PK. XCI. The use of the glass electrode in biochemistry. Biochem J 1925; 19: 11–617.
doi: https://doi.org/10.1042/bj0190611
9. Krammer R, Hoffman K-P, Pozos RS. Springer Handbook of Medical Technology, Springer; 2011. pp. 95–116, 971–985.
10. McNaught J. A case of dilatation of the stomach accompanied by the eructation nof inflammable gas. BMJ 1890; 1: 70.
doi: https://doi.org/10.1136/bmj.1.1522.470
11. Galley AH. Combustible gases generated in the alimentary tract and other hollow viscera and their relationship to explosions occurring during anaesthesia. Brit J Anaesth 1954; 26: 292–296.
doi: https://doi.org/10.1093/bja/2w6.3.181
12. Newman A. Breath-analysis tests in gastroenterology. Gut 1974; 15: 308–323.
doi: https://doi.org/10.10136/gut.15.4.308
13. Cozzetto FJ. Radiocarbon estimates of intestinal absorbtion. Studies of breath excretion of C14 O2 after ingestion of labeled fatty acids, glucose and lactose. Am J Dis Child 1962; 107: 605–611.
PMID: 14133820 doi: https://doi.org/10.1136/gut.15.3.308
14. Berlin NI, Tolbert BM. Metabolism of glycerine-2-C14 in man: V. Further considerations of the pulmonary excretion of C14O2. Proc Soc exp Biol
(N. Y) 1955; 88: 386–389.
doi: https://doi.org/10.3181/00379727-88-21596
15. Luck JM. Gastric urease. Biochem J 1924; 18: 1227–1231.
doi: https://doi.org/10.1042/bj0181227
16. Kornberg HL, Davies RE. Gastric urease. Physiol Rev 1955; 35: 169–177.
doi: https://doi.org/0.1152/physrev.1955.35.1.109
17. Delluva AM, Markley K, Davies RE. The absence of gastric urease in germ-free animals. Biochim Biophys Acta 1968; 1512: 646–650.
18. Marshall BJ, Surveyor I. Carbon-14 urea breath test for the diagnosis of Campylobacter pylori associated gastritis. J Nucl Med 1988; 29: 11–16.
PMID 3335917
19. Bentur Y, Matsui D. Safety of 14C-UBT for diagnosis of Helicobacter pylori infection in pregnancy. Canad Fam Phys 2009; 55: 479–480.
PMID: 19439698
20. Graham, DY, Klein PD. Evans DJ, Evans DG, Albert LC, Opekun TR, Boutton TW. Campylobacter pylori detected noninvasively by the 13C-urea breath test, Lancet 1987; 1(8543): 1174–1177.
doi: https://doi.org/100.1016/s-0140-6736(87)92145-3
21. Sütő G, Vincze Á, Pakodi F, Hunyady B, Karádi O, Garamszegi M, László T, Mózsik G. 13C-urea breath test is superior in sensitivity to detect Helicobacter pylori infection than either antral histology or rapid urease test. J Physiol Paris 2000; 94: 2, 153–156.
doi: https://doi.org/10.1016/s0928–4257(00)00157-1
22. Krumbiegel P, Faust H, Teichman B, Spencker F-B, Rogos B. Rapid non-invasive diagnosis of gastric Campylobacter pylori infection by a simple [15N2] urea urine test, . Eur J Nucl Med 1990; 16: 423.
doi: https://doi.org/10.1080/003655200750023903
23. Calloway DH. Respiratory hydrogen and methane as affected by consumption of gas. Gastroenterology 1966; 51: 383–389.
PMID: 59445818
24. Calloway DH, Burroghs SE. Effect of dried bean and silicone on intestinal hydrogen and methane production in man. Gut 1969; 10: 180–184.
doi: https://doi.org/010.1136/gut.10.3.180
25. Levitt MD, Ingelfinger FJ. Hydrogen and methane production in man. Ann NY Acad Sci 1968; 150: 75–81.
doi: https://doi.org/10.1111/j.1749-6632-1168.tb.19033.x
26. Lyle LH. Breath tests in gastroenterology. Milwaukee, USA: QuinTron Instrument Company;
27. Beró T, Past T, Tapsonyi Z, Mózsik Gy, Jávor T. A lehelet H2 meghatározás klinikai jelentősége. Orv Hetil 1983; 1234 (3): 67–69.
PMID: 6828319
További irodalom megtalálható a szerkesztőségben, valamint
a www.gastronews.olo.hu weboldalon.
