Összefoglaló közlemény / Review
COVID-19 and the liver
Summary
SARS-CoV-2 coronavirus, identified in 2019, is primarily causing respiratory tract COVID-19 diseases, in a good number of cases with severe or even fatal consequences. By now, COVID-19 related non-respiratory organ involvement with different severity has been proven. On the other hand, certain symptoms/diseases might persist for a prolonged period of time after the primary infection (post-acute COVID syndrome). Relationship between SARS-CoV-2 virus and the liver, including interactions of COVID-19 disease with pre-existing liver disease, consequences of COVID-19 and its therapy on the liver and vice versa, as well as hepatology aspects of vaccination are reviewed in this paper. Immunological, inflammatory and thrombotic processes, activation of immune system, and particularly the cytokine storm may cause liver injury during COVID-19, which – on the other hand – may worsen COVID-19 disease and its outcome. SARS-CoV-2 virus can directly bind to ACE2 receptors on cholangiocytes, however its direct hepato-pathogenicity is not confirmed. Half of COVID-19 patients develop laboratory abnormalities suggesting liver involvement. Factors associated with liver injury include severity of COVID-19 disease, type and severity of pre-existing liver disease, alcohol in etiology, and advanced age. Drug-induced liver injury is also to be considered in patients treated for COVID-19, and a thorough observation for side-effects is recommended.
A 2019-ben azonosított SARS-CoV-2 koronavírus által okozott COVID-19 betegség elsősorban a légutakat támadja meg, nemritkán súlyos, akár fatális kimenetellel járhat. Napjainkra nyilvánvalóvá vált, hogy egyrészt a betegség különböző gyakorisággal és súlyossággal más szerveket is érinthet, másrészt az akut fertőzési időszak után tartós tünetek/betegségek alakulhatnak ki (poszt-akut COVID szindróma). Ebben a közleményben a szerzők a SARS-CoV-2 vírus májjal kapcsolatos összefüggéseit mutatják be, beleértve a vírusfertőzés és a meglévő májbetegségek kölcsönhatását, a COVID-19 betegség és kezelésének a májműködésre, májbetegekre gyakorolt hatását, valamint a vakcinációval kapcsolatos hepatológiai szempontokat. A COVID-19-infekció során szerepet játszó immunológiai, gyulladásos és trombotikus folyamatok, az immunrendszer aktiválódása és különösen a citokinvihar májkárosodáshoz vezethet, ami viszont ronthatja a COVID-19 betegség lefolyását, kimenetelét. A SARS-CoV-2 vírus direkt kötődhet a cholangiocytákon kimutatható ACE2 receptorokhoz, de nem igazolt közvetlen hepatopatogenitása. A COVID-19-betegek felében májérintettségre utaló laboratóriumi eltérések alakulnak ki. A májkárosodás kockázati tényezője a COVID-19-fertőzés súlyossága, a korábbi májbetegség típusa és súlyossága, az alkoholos eredet, valamint a magasabb életkor. Gyógyszer okozta májkárosodással COVID-19-fertőzöttek kezelése során is számolni kell, fontos a mellékhatások gondos ellenőrzése.
Bevezetés
A 2019-ben azonosított SARS-CoV-2 koronavírus által okozott COVID-19 betegség elsősorban a légutakat betegíti meg (súlyos formában COVID-19-tüdőgyulladás), de bizonyítottan más szervek betegségeivel is járhat (1). A napjainkban is zajló világméretű járvány eddig több hullámban igazoltan több mint 300 millió egyén megbetegedését, több mint 5,5 millió személy halálát okozta (2). A ténylegesen megbetegedettek és áldozatok száma ennek többszöröse is lehet.
Bár a vírusfertőzés ellen több hatékony védőoltást fejlesztettek ki, a lakosság átoltottsággal vagy a fertőzés átvészelésével szerzett védettsége lényegében egyetlen országban sem elegendő az új megbetegedések számának tartós csökkenéséhez. Külön nehézséget jelent a vírus magas variabilitása, az egyre újabb, magas virulenciájú variánsok megjelenése (a legutóbbi az omikron variáns).
Mind az akut COVID-19-megbetegedés során (különösen a súlyos formák esetén), mind pedig azok után (poszt-akut COVID-időszak) nem légúti megbetegedések alakulhatnak ki, lényegében bármely szervben – így az emésztőrendszerben is (3, 4). Ebben a közleményben a szerzők a SARS-CoV-2-vírusfertőzésnek, valamint kezelésének és megelőzésének a májbetegségekkel kapcsolatos összefüggéseit mutatják be.
SARS-CoV-2-vírusfertőzés kimenetele májbetegeknél (1. táblázat)
Krónikus májbetegekben a SARS-CoV-2-vírusfertőzés a nem májbetegekhez hasonlóan lehet tünetmentes, vagy a megszokott tünetekkel járó COVID-19 betegséget okozhat. Egyes közlemények szerint a krónikus májbetegek fokozottan ki vannak téve a súlyos COVID-19 betegség kockázatának (5, 6). Más közlemények szerint kompenzált stádiumú krónikus májbetegeknél a COVID-19 betegség kimenetele nem különbözik a nem májbetegekre jellemzőtől, sem a COVID-19 betegség súlyossága, sem a hospitalizációk aránya, sem a kórházi tartózkodás időtartama, sem a légzéstámogatási/lélegeztetési igény, sem a mortalitás szempontjából (7–11). A dekompenzált májműködés (Child–Pugh C > Child–Pugh B), a májrák, valamint a rendszeresen jelentős mennyiségű alkohol fogyasztása viszont számos tanulmány szerint az előbbi mutatók mindegyike szempontjából kedvezőtlenebb kimenetellel jár mind a COVID-19 betegség, mind a májbetegség szempontjából.
1. táblázat: A COVID-19 lefolyása és klinikai jelentősége krónikus májbetegségben (5)
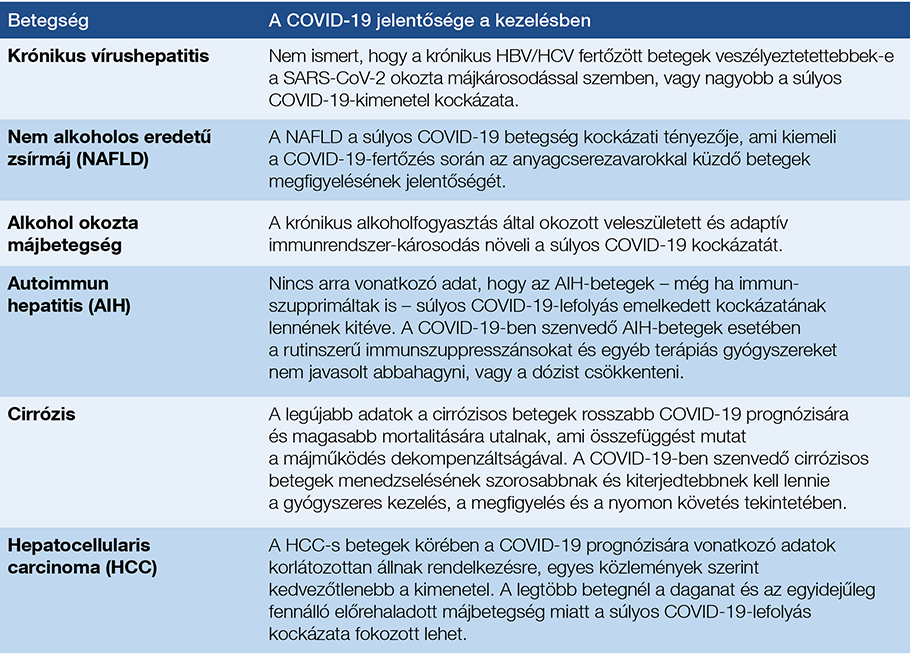
Nem igazolt, hogy összefüggés lenne a krónikus vírushepatitisek és a COVID-19 betegség között, azaz az egyik a másik kimenetelét érdemben befolyásolná, nem előrehaladott stádiumban lévő májbetegek esetében. Összefüggést mutattak viszont ki a COVID-19 és a nem alkoholos steatosis (NAFLD/MAFLD), steatohepatitis (NASH) között. Elképzelhető, hogy elsősorban az ezekkel gyakran együtt járó túlsúlynak, szénhidrátanyagcsere-zavarnak, hipertóniának vagy a metabolikus szindróma más faktorának lehet jelentősége, nem közvetlenül a májban zajló steatosisnak, steatohepatitisnek (12, 13).
A SARS-CoV-2-vírusfertőzés hatása a májműködésre
A SARS-CoV-2 vírus jelentős szisztémás megbetegedésekhez vezethet, és – más szervek mellett – érintheti a gasztrointesztinális traktust, a májat, az epeutakat és a hasnyálmirigyet is (3, 6, 7). Fontos szerepe lehet a vírus kötődésének a bélnyálkahártyán nagy sűrűséggel jelen lévő angiotenzinkonvertáló enzim 2 (ACE2-) és transzmembrán szerin-proteáz-2 (TMPRSS2-) receptoroknak, amelyeken keresztül a vírus bejut a bélnyálkahártyasejtekbe (14).
Májkárosodás, kóros májenzimeltérések gyakran (>40%) fordulnak elő COVID-19-ben szenvedő betegekben (15, 16). Nem tisztázott, hogy a COVID-19 betegség során a májkárosodás főként a vírusfertőzés, a potenciálisan hepatotoxikus gyógyszerek vagy más okok miatt alakul-e ki. A már meglévő krónikus májbetegség (CLD) fellángolása vagy progressziója is állhat a laboreltérések hátterében. A COVID-19 okozta májérintettség rizikófaktorai: a COVID-19 betegség súlyossága, a megelőző májbetegség és az idős életkor.
A SARS-CoV-2 vírus nem direkt hepatotróp, és nem igazolt közvetlen hepatopatogenitása, de a dekompenzáció kockázatának fokozásával növelheti az előrehaladott cirrózisban szenvedők mortalitását. Bár a máj epeúti hámsejtjeiben kimutathatók a vírus légúti patogenitásában fontos szerepet játszó ACE2 receptorok, a vírus közvetlen májkárosító hatása nem igazolt. Ennek ellenére előzőleg ismerten nem májbetegek COVID-19 betegsége során gyakran alakulnak ki májsejtkárosodásra utaló laboratóriumi eltérések: a kezelést igénylő COVID-19-esetek első diagnózisakor 25%-ban, a betegség lezajlása során további 25%-ban. COVID-19-fertőzésben a potenciális direkt májsejtkárosodás mellett a hipotenzió, a hypoxia, a citokinek által aktivált mikrovaszkuláris thrombusképződés, gyulladásos és immunológiai folyamatok tekinthetők a májkárosodás legfőbb okának (17). Ennek során a máj sinusoidalis endothelialis sejtek aktivációjában az interleukin-6, ennek szolubilis receptora, kemokin ligandok, adhéziós molekulák, glikoprotein 130, a Von Willebrand-faktor, a VIII faktor, az ezek miatt kialakuló thrombocytaaggregáció, neutrofilsejt-szaporulat- és aktiváció, valamint a hepatocyták aktivációja játszik szerepet (18). Utóbbi trombotikus és gyulladásos folyamatok részeként fibrinogén és akutfázis-fehérjék fokozott termelésével is jár.
A máj érintettsége általában enyhe, nem eredményez klinikai tünetekkel járó akut vagy krónikus májbetegséget, és nem igényel speciális kezelést. Ugyanakkor súlyos, szisztémás COVID-19 betegség kapcsán akut (elvétve fulmináns) hepatitisnek megfelelő májkárosodás vagy májelégtelenség alakulhat ki, ami átmehet szubakut vagy krónikus formába is. Másrészt a májérintettség súlyosságával növekszik a COVID-19 betegség mortalitása.
A májkárosodás autoimmun hepatitishez, vaszkuláris/iszkémiás/pangásos májkárosodáshoz, esetenként a cholestasis által dominált szklerotizáló cholangitishez hasonló klinikummal jár. Kritikus állapottal járó, lélegeztetést igénylő COVID-19 betegség után több szerző írta le poszt-akut COVID-19 cholangiopathia, szekunder szklerotizáló cholangitis kialakulását, elhúzódó súlyos cholestasissal, májelégtelenséggel, korai májcirrózissal (19, 20). A májkárosodásnak ugyanilyen formáját leírták ugyanakkor nem COVID-19 etiológiájú kritikus állapottal, lélegeztetéssel járó esetekben is.
Diszbiózis és áteresztő gasztrointesztinum COVID-19 betegség során
A COVID-19-fertőzés során és után nagyon gyakori a diszbiózis, amelyben a tüdőgyulladás, szepszis miatt szükségessé váló antibiotikum adásának, a többszerv-elégtelenségnek, a megváltozott bakteriális bélflórának (diszbiózis), valamint az ún. áteresztő gasztroeintesztinum („leaky gut”) jelenségnek van szerepe (21, 22). Az emésztőrendszer a légutakhoz hasonlóan rendelkezik a COVID-19 betegség kialakulásában fontos szerepet játszó ACE2 receptorokkal. A SARS-CoV-2 vírus ezekhez közvetlenül kötődni tud. Ez közvetlenül is, valamint a légúti megbetegedés során keletkező citokinek és protrombotikus faktorok immunológia és/vagy trombotikus folyamatokat aktiválnak, amelyek következtében a bélrendszerben és a májban ödéma, mikrocirkulációs zavar, iszkémia, trombózis, gyulladás és a gasztrointesztinális nyálkahártya áteresztőképességének fokozódása alakulhat ki. Mindez a mucosa barrier funkciójának csökkenését, bakteriális termékek és toxinok szervezetbe jutását, a gyulladásos és trombotikus citokinek/faktorok termelésének fokozódását eredményezik.
A COVID-19 terápiájával kapcsolatos májbetegségek (hepatotoxicitás)
A COVID-19 kezelésére használt egyes gyógyszerek egyrészt emésztőrendszeri tünetekkel járhatnak (főként hasi diszkomfort, fájdalom, puffadás, hányinger, hányás, hasmenés), másrészt súlyos mellékhatásokhoz, gyógyszerkölcsönhatásokhoz vezethetnek. Gyulladásos bélbetegek és krónikus májbetegek körében továbbra is kiterjedten vizsgálják az immunmoduláns- és biológiai kezelések kockázatait. A tapasztalatok alapján a remisszióban lévő betegek kezelésének megszakítása nem javasolt, tekintettel a relapszus valós és jelentős kockázatára (23).
2. táblázat: Potenciálisan májkárosodást okozó COVID-19 betegség és
szövődményeinek kezelésére használt gyógyszerek*

*Potenciálisan bármely gyógyszer okozhat májkárosodást.
COVID-19 kezelése során kifejezetten gyakoriak (>40%), de többnyire nem súlyosak a gyógyszer okozta hepatikus mellékhatások. Általában enyhe-mérsékelt fokú laboratóriumi eltérések jelzik, vagy enyhe tünetekkel járó hepatitisszindróma klinikai képe alakul ki (puffadás, máj táji fájdalom, étvágytalanság). Ritkán azonban sárgasággal járó súlyos hepatitis, nagyon ritkán májelégtelenség, fatális kimenetel is előfordulhat, vagy májátültetés válhat szükségessé. A patomechanizmus nem különbözik az egyéb betegségek kezelésére használt készítmények kapcsán észlelt májkárosodástól (drug induced liver injury, DILI). Azaz vagy a dózistól függetlenül, idioszinkráziás mechanizmussal vagy dózisfüggő módon, a készítmény vagy metabolitja direkt májkárosító hatása útján alakul ki. Szerepe lehet a gyógyszer-gyógyszer interakcióknak is. Ahogy a DILI más eseteiben is, a fő kockázati tényezők: súlyos klinikai állapot, szervelégtelenség, idős életkor, csecsemőkor, elhízás, alultápláltság, társbetegségek, többféle gyógyszer egyidejű használata. Az eltérések legtöbbször a gyógyszer elhagyása után néhány hét alatt spontán rendeződnek, a súlyos formákban azonban a nem COVID DILI-esetekben alkalmazott terápiák/eljárások lehetnek szükségesek. Ilyen lehet a szteroidkezelés, a májpótló kezelés vagy a májátültetés. A 2. táblázat metaanalízis alapján, potenciálisan májkárosodást okozó COVID-19 kezelésére használt készítményeket tüntet fel (7).
A COVID-19 elleni védőoltás és a máj
Hatékony antivirális kezelés hiányában a SARS-CoV-2-fertőzés megelőzésében a védőoltásnak döntő jelentősége van. A védőoltásokkal folytatott klinikai vizsgálatokba bevont egyének nagy száma ellenére is csak korlátozottan állnak rendelkezésre adatok a májbetegségben szenvedők védőoltásával kapcsolatban (24).
Valamennyi engedélyezett oltóanyag hatékony, jelentősen csökkenti a COVID-19 kockázatát, különösen a súlyos és kritikus megbetegedés kialakulásának a lehetőségét, és csökkenti a COVID-19-hez kapcsolódó kórházi kezeléseket és halálozást. Ugyanakkor a megfertőződés esélyét teljesen nem zárják ki (25). Nincs adat arra vonatkozóan, hogy májbetegeknél különbség lenne az egyes védőoltások hatékonysága között, vagy szükség lenne az átlagpopulációtól eltérő adagolásra és/vagy időzítésre. Ennek megfelelően nincsen elfogadott egységes irányelv arról sem, hogy melyiket kellene előnyben részesíteni májbetegek vakcinálásakor.
3. táblázat: COVID-19 és krónikus májbetegségek kapcsolatának főbb szempontjai, klinikai jelentősége
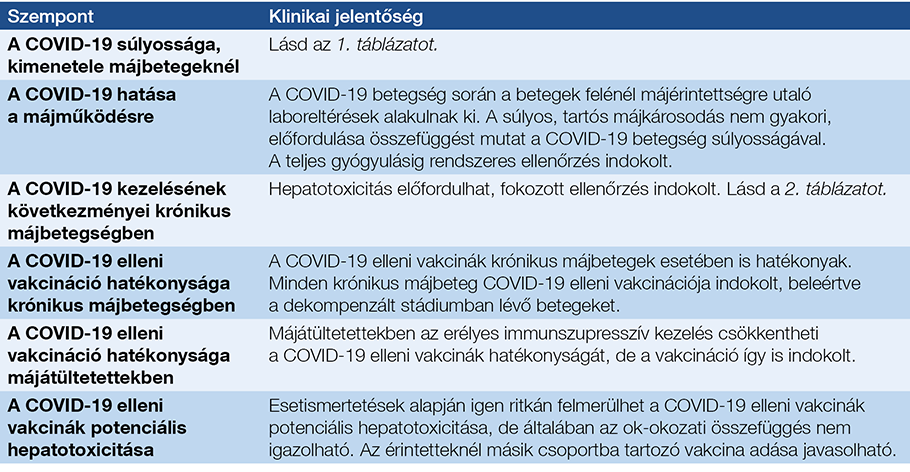
Magyarországon az mRNS-alapú (Pfizer/BioNTech BNT162b2/Comirnaty és Moderna mRNS-1273/Spikevax), a csimpánz-adenovírusvektor (AstraZeneca/University of Oxford ChAdOx1-nCoV-19/Vaxzevria és Janssen/Johnson & Johnson Ad26.COV2.S), a heterológ rekombináns adenovírus-alapú (Gam-COVID-Vac Szputnyik V) és az inaktivált teljes vírust tartalmazó (WIV04 és HB02 Sinopharm) védőoltás egyaránt engedélyezett. Ezek bármelyike hatékony, és adható krónikus májbetegségekben. Kritikus állapotú májbetegek, májtranszplantáltak passzív immunizálása is lehetséges.
Felmerült a lehetősége, hogy a SARS-CoV-2 elleni védőoltások hatékonysága krónikus májbetegségben (CLD) szenvedőknél elmaradhat az átlagpopulációétól (26). Ebben a speciális betegcsoportban a veleszületett és adaptív immunrendszer diszfunkciójával kell számolni, ami hajlamosító tényező a fertőzések kialakulására és a védőoltásokra adott csökkent válaszra (27, 28). Indirekt módon a hypersplenia, a malnutríció, az alkoholfogyasztás is negatívan befolyásolja az immunválaszt (29, 30). Ugyanakkor krónikus májbetegeknél nem igazolt a SARS-CoV-2-vakcinákkal kapcsolatos csökkent válaszkészség. Májátültetetteknél azonban a tartós, erélyes immunszuppresszív kezelés miatt a COVID-19-védőoltások immunogenitása elmarad a nem transzplantáltakéhoz képest (31, 32). A vakcináció után kialakuló COVID-19 elleni ellenanyag-termelés mértéke összefüggést mutat az immunszuppresszió erősségével: egyféle immunszuppresszív szer esetén enyhén, két- vagy többféle immunszuppresszív szer esetén jelentősen csökken (33). Májátültetetteknél egyes nem COVID-fertőzés ellen használt vakcinák esetében dupla dózist javasolnak az immunológiai válasz fokozására, de COVID-19 esetében nincsen ilyen ajánlás (34).
Nemzetközi ajánlások szerint májbetegeknek – beleértve az előrehaladott stádiumú cirrózisos betegeket, a hepatobiliaris daganatos betegségben szenvedőket, a máj-transzplantációs várólistán lévőket és a májtranszplantáltakat – egyaránt javasolt, és prioritást kell élveznie a COVID-19 elleni védőoltásnak a rendelkezésre álló COVID-19-vakcinák bármelyikével (35). Ha az egyik típusú vakcina ellenjavallt, nem ajánlott ugyanabba a csoportba tartozó másik vakcina, de más csoportba tartozó elővigyázatossággal igen.
4. táblázat: Az AASLD néhány gyakorlati ajánlása, megállapítása (41)

A májtranszplantációs várólistán lévő recipiensek oltása lehetőség szerint még a transzplantáció előtt javasolt a megfelelő immunválasz érdekében (34). Nem ellenjavallt kadávermáj transzplantációja azoknak a recipienseknek, akik a transzplantációs riadó előtt kaptak védőoltást, mivel a májtranszplantáció életmentő műtét, másrészt a COVID-19 elleni vakcinák nem tartalmaznak szaporodóképes vírust. Azon májátültetettek esetében, akik a transzplantáció előtt nem lettek beoltva, ezt pótolni kell, általában a műtét után legkorábban három hónappal, amikor az immunszuppressziójuk már alacsonyabb szintű, és az egyéb profilaktikus gyógyszerekre sincsen szükség, vagy csak minimális dózisban. Tekintettel azonban a SARS-CoV-2 folyamatos közösségi terjedésére, egyes ajánlások szerint az immunizálás már 6 héttel a transzplantáció után is megkezdhető, különösen a súlyos COVID-19-hez társuló egyéb társbetegségek szempontjából legnagyobb kockázatúak esetében. Nem indokolt az immunszuppresszió csökkentése annak érdekében, hogy a SARS-CoV-2 elleni immunizációra adott válasz erősebb legyen, mert ez az akut rejekció kialakulásának veszélyével jár. Igazolt akut rejekció kezelése alatt a vakcináció kerülendő. Indokolt a transzplantáltak családtagjainak és gondozóiknak a COVID-19 elleni immunizálása is a „fészekimmunitás” kialakítása érdekében (34).
Felmerült, hogy szervátültetettek vakcinálása alloimmunitás kialakulásához és a transzplantátum kilökődéséhez vezetne, de nincs olyan klinikai bizonyíték, amely ezt az aggodalmat alátámasztotta volna (36, 37).
Javasolt mielőbb COVID-19 elleni védőoltást adni hepatobiliaris carcinomában szenvedők lokoregionális vagy szisztémás kezelése, HBV- és HCV-fertőzöttek antivirális kezelése alatt, ezek megszakítása nélkül (38).
COVID-19-vakcinációval kapcsolatos májbetegségek (hepatotoxicitás)
Májspecifikus potenciális mellékhatásként COVID-19-vakcináció után autoimmun hepatitishez vagy szklerotizáló cholangitishez hasonló akut májsejtkárosodást írtak le többfajta védőoltás esetében is (39, 40). Bár ezek között elvétve súlyos eset is előfordult, nem bizonyított az oki összefüggés a vakcinákkal. A közlemények alapján – az időbeli kapcsolat ellenére – nem dönthető el, hogy tényleg a védőoltás váltotta-e ki a májkárosodást, vagy koincidenciáról, az addig fel nem ismert, eleve meglévő májbetegségről, annak aktivációjáról van-e szó. A közölt esetek száma rendkívül alacsony a vakcináltak számához képest. Összességében az esetlegesen előforduló oltási reakciók és mellékhatások kockázata rendkívül kicsi, ezeket a vakcináció előnyei messze felülmúlják az eddigi tapasztalatok szerint májbetegeknél is.
Megbeszélés
A COVID-19-pandémia számos nyitott kérdést vetett fel az elmúlt időszakban, amelyek egy részére evidenciákon alapuló, egyértelmű tudományos válasz jelenleg még nem adható. A gyakorló orvosok munkájának segítésére több szakmai szervezet (EASL, AASLD) közzétett a honlapján állásfoglalásokat, ajánlásokat, előadásokat, amelyeket rendszeresen aktualizálnak, kiegészítenek. Ezekben – a tudományosan alátámasztott evidenciák mellett – jelentős részben ún. „expert opinion”, azaz tapasztalt szakemberek véleménye/gyakorlata fogalmazódik meg, és ad iránymutatást a mindennapi klinikai gyakorlat számára. A folyamatban lévő klinikai vizsgálatok adatainak és a mindennapi gyakorlat tapasztalatinak folyamatos feldolgozása alapján az irányelvek, ajánlások folyamatos aktualizálása várható a májbetegek kezelésével és vakcinációjával kapcsolatban is. Ezek követése valamennyi ellátó feladata. A 3. táblázat a COVID-19 és a májbetegségek kapcsolatának főbb szempontjait és ezek klinikai jelentőségét foglalja össze, míg a 4. táblázat az AASLD néhány további gyakorlati ajánlását mutatja be.
A közleményben leírtak alapján kiemelendő, hogy a SARS-CoV-2-fertőzés során, csakúgy, mint a COVID-19 kezelése és megelőzése kapcsán a májműködéssel kapcsolatban jelentkező speciális szempontok fokozott figyelmet érdemelnek, az alábbi fő okok miatt. Dekompenzált májbetegeknél, alkoholos eredetű májbetegségben és májrák esetén a COVID-19 kimenetele – csakúgy, mint a májbetegség kimenetele – kedvezőtlenebb, mint májbetegség nélkül. Bár a SARS-CoV-2 vírus direkt hepatopatogenitása kérdéses, a COVID-19 betegség, valamint annak ellátása és a vakcináció kapcsán egyaránt kialakulhat akut, szubakut vagy krónikus májkárosodás. A COVID-19-betegek felében májérintettségre utaló laboratóriumi eltérések alakulnak ki. Ez legtöbbször enyhe, de kivételesen előfordulhat súlyos májkárosodás, korai májzsugor, fatális kimenetel is. Hátterében elsősorban immunmediált gyulladásos mechanizmusok, trombotikus, iszkémiás folyamatok vagy hypoxia valószínűsíthetők. A májkárosodás kockázati tényezője a COVID-19 súlyossága, a korábbi májbetegség típusa és súlyossága, az alkoholos eredet, valamint a magasabb életkor. Gyógyszer okozta májkárosodással COVID-19-fertőzöttek kezelése során szintén számolni kell. Fontos a mellékhatások korai felismerése és szoros követése a teljes gyógyulásig. Egységes szűrési, diagnosztikai és terápiás algoritmusok hiányában COVID-19-hez társuló májbetegségekben a hasonló megjelenésű nem COVID betegségekben szokásos ellátás javasolható. A májbetegek COVID-19 elleni vakcinálása – az erős immunszuppressziót igénylő májátültetetteket is beleértve – kifejezetten indokolt, prioritást élvez.
https://doi.org/10.1056/NEJMoa2001017.
2. Egészségügyi Világszervezet. WHO Coronavirus (COVID-19) Dashboard. Overwiev. https://covid19.who.int/ (accessed: 14 Jan 2022)
3. Silva FAFD, Brito BB, Santos MLC, et al. COVID-19 gastrointestinal manifestations: a systematic review. Rev Soc Bras Med Trop 2020 Nov 25; 53: e20200714.
https://doi.org/10.1590/0037-8682-0714-2020. eCollection 2020.
4. Elmunzer BJ, Spitzer RL, Foster LD, et al. North American Alliance for the Study of Digestive Manifestations of COVID-19. Digestive Manifestations in Patients Hospitalized With Coronavirus Disease 2019. Clin Gastroenterol Hepatol 2021 Jul; 19(7): 1355–1365.e4.
https://doi.org/10.1016/j.cgh.2020.09.041.
5. Hu X, Sun L, Guo Z, et al. Management of COVID-19 patients with
chronic liver diseases and liver transplants. Ann Hepatol 2021 Dec 18; 27(1): 100653. https://doi.org/10.1016/j.aohep.2021.100653.
6. Saviano A, Wrensch F, Ghany MG, et al. Liver Disease and Coronavirus Disease 2019: From Pathogenesis to Clinical Care. Hepatology 2021 Aug; 74(2): 1088–1100. https://doi.org/10.1002/hep.31684.
7. Kulkarni AV, Kumar P, Tevethia HV, et al. Systematic review with meta-analysis: liver manifestations and outcomes in COVID-19. Aliment Pharmacol Ther 2020 Aug; 52(4): 584–599. https://doi.org/10.1111/apt.15916.
8. Kim D, Adeniji N, Latt N, et al. Predictors of Outcomes of COVID-19 in Patients With Chronic Liver Disease: US Multi-center Study. Clin Gastroenterol Hepatol 2021 Jul; 19(7): 1469–1479.e19.
https://doi.org/10.1016/j.cgh.2020.09.027.
9. Mallet V, Beeker N, Bouam S, et al. Demosthenes research group. Prognosis of French COVID-19 patients with chronic liver disease: A national retrospective cohort study for 2020. J Hepatol 2021 Oct; 75(4): 848–855. https://doi.org/10.1016/j.jhep.2021.04.052.
10. Marjot T, Moon AM, Cook JA, et al. Outcomes following SARS-CoV-2 infection in patients with chronic liver disease: An international registry study. J Hepatol 2021 Mar; 74(3): 567–577.
https://doi.org/10.1016/j.jhep.2020.09.024.
11. Satapathy SK, Roth NC, Kvasnovsky C, et al. Northwell Health
COVID-19 Research Consortium. Risk factors and outcomes for acute-on-chronic liver failure in COVID-19: a large multi-center observational cohort study. Hepatol Int 2021 Jun; 15(3): 766–779.
https://doi.org/10.1007/s12072-021-10181-y.
12. Anirvan P, Singh SP, Giammarino A, et al. Association of non-alcoholic fatty liver disease and COVID-19: A literature review of current evidence. World J Hepatol 2021 Aug 27; 13(8): 916–925.
https://doi.org/10.4254/wjh.v13.i8.916.
13. Sanoudou D, Hill MA, Belanger MJ, et al. Editorial: Obesity, metabolic phenotypes and COVID-19. Metabolism 2022 Jan 10; 155121.
https://doi.org/10.1016/j.metabol.2021.155121. Online ahead of print. (Accessed: 14 Jan 2022)
A további irodalom megtalálható a szerkesztőségben, valamint
a www.gastronews.hu weboldalon.
