Összefoglaló közlemények / Reviews
Non-alcoholic fatty liver disease (NAFLD) or metabolic (dysfunction)-associated fatty liver disease (MAFLD)? (Opinions vs. evidence)
Summary
The non-alcoholic fatty liver disease (NAFLD) is the most common liver disorder worldwide, a clinicopathological spectrum from pure steatosis to steatohepatitis and cirrhosis. The progressive form of NAFLD is the non-alcoholic steatohepatitis (NASH) with or without fibrosis has a high risk of severe outcomes, including hepatic and extrahepatic complications. The diagnosis of NAFLD has been based on the presence of fatty liver and lack of excessive alcohol consumption and the exclusion of other causes of steatosis. Since the term NAFLD contains „negative criteria” (and alcohol in its name), during the last two decades several authors have suggested to rename the disease to a „positive” term, that should involve metabolic instead of non-alcoholic. In 2020 an international expert consensus statement has recommended a new definition of metabolic (dysfunction)-associated fatty liver disease (MAFLD) to replace NAFLD, and it was suggested how the disease should be diagnosed. The diagnosis of MAFLD should be based on the evidence of hepatic steatosis (by imaging techniques, biomarkers or biopsy), in addition to one of the following three criteria: overweight/obesity, type 2 diabetes mellitus, and metabolic dysfunction. The proposal has evoked intensive debates in the hepatology literature. A number of experts and liver societies have been supportive concerning the usefulness of the new diagnostic criteria. It was emphasized that MAFLD can help to identify those patients with steatosis who are at high risk of more advanced liver disease, in addition, the new name mirrors the metabolic nature of the disease, and is not stigmatizing. Others disagreed with the change, saying that it is premature, and can create rather confusion than advance in the field. This paper gives an account on the diagnostic criteria of MAFLD, overviews the experts’ opinions on MAFLD term, and discusses the implications of the name change. It can be concluded, that the debate is not over. There is a need for further researches on better understanding of the pathogenesis of the disease entity, and continue the exchange of ideas, assess the consequences of the new terminology, thus archive a true, evidence-based consensus.
A nem alkoholos zsírmájbetegség (NAFLD) a leggyakoribb krónikus májbetegség a világon, a klinikopatológiai spektrum a tiszta steatosistól a steatohepatitisen át a cirrózisig terjed. A NAFLD progresszív formája a nem alkoholos steatohepatitis (NASH), amely – fibrózissal vagy anélkül – súlyos következményekkel, hepatikus és extrahepatikus komplikációk magas kockázatával jár. A NAFLD diagnózisa a steatosis jelenlétén, valamint az alkoholfogyasztás és a steatosist okozó egyéb állapotok kizárásán alapul. Mivel az elnevezésben a stigmatizáló alkohol szó szerepel, és a kórisme „negatív kritériumokat” tartalmaz, az utolsó két évtizedben számos felhívás látott napvilágot a NAFLD elnevezés megváltoztatására. 2020-ban egy nemzetközi szakértői megegyezés a metabolikus diszfunkcióval asszociált zsírmájbetegség (MAFLD) terminust javasolta, megadva a diagnózis kritériumait is. Ezek szerint a MAFLD kórismézéséhez a steatosis képalkotóval, biomarkerrel vagy hisztológiával való bizonyítása mellett három tényező (a túlsúly/obesitas, a 2-es típusú diabetes mellitus és a metabolikus zavar) közül egy jelenléte szükséges. Az állásfoglalás intenzív vitát váltott ki a hepatológiai irodalomban. Számos szakértő és több májkutatási társaság támogatta az új kritériumrendszer hasznosságát. Hangsúlyozták, hogy a MAFLD jobban segíthet azonosítani az előrehaladott májbetegség kockázatának kitett zsírmájas betegeket, továbbá az új terminus kiemeli a kórkép metabolikus természetét, és nem stigmatizál. Más szerzők nem értenek egyet a változtatással, azt idő előttinek tartják, ami szerintük több zavart okoz, mint amennyi az előnye. A jelen dolgozat ismerteti a MAFLD diagnosztikus kritériumait, és áttekintést ad a NAFLD vs. MAFLD vitáról.
Következtetés: a kérdés nem eldöntött. A továbblépéshez folytatni szükséges a betegség patogenezisének kutatását és a széles körű eszmecseréket, értékelni az új terminológia következményeit, ily módon elérni a bizonyítékon alapuló konszenzust a témában.
Történeti áttekintés
Az Amerikai Májkutatási Társaság (AASLD) 1979. évi kongresszusának plenáris ülésén Klatskin és munkatársai 27, alkoholt nem fogyasztó betegben az alkoholos hepatitis és cirrózis típusos hisztológiai jeleiről számoltak be, és a kórképet mint „nem alkoholos májbetegség”-et írták le (1). Ugyanebben az évben Adler és Schaffner 29 elhízott egyénben közölték a zsírmájhepatitis és cirrózis előfordulását (2). Nyolc hónappal később Ludwig és munkatársai a Mayo Klinikáról 20, többségében elhízott, diabéteszes betegben észlelték az alkoholos hepatitisre jellemző típusos hisztológiai elváltozásokat, és az addig nem ismert betegséget nem alkoholos steatohepatitisnek (NASH) nevezték el (3).
A nem alkoholos zsírmájbetegség (NAFLD) terminus az irodalomban Schaffner és Thaler 1986-os közlése után lett általánosan ismert és elfogadott (4). Ezt követően a NAFLD közel két évtizedig alig kapott figyelmet, csak az ezredforduló körül kezdett megnőni iránta az érdeklődés. Ekkorra tisztázódott egyrészt, hogy a NAFLD a steatosistól a steatohepatitisen át a cirrózisig tartó betegségspektrum, másrészt hogy a kórkép a metabolikus szindróma májmanifesztációjának tekinthető.
A NAFLD természetrajzának ismeretében vetődött fel, hogy indokolt lenne a betegség elnevezésének megváltoztatása az alapvető anyagcsere-eltérések figyelembevételével.
2002-ben az AASLD konferenciája foglalkozott először a NAFLD terminus kérdésével, és a metabolikus steatohepatitist javasolták, de nem állapodtak meg (5).
Három évvel később Loria és munkatársai a non-A, non-B hepatitis hepatitis C-re történt névváltoztatáshoz hasonlóan lehetségesnek tartották, és ajánlották a nem alkoholos elnevezés megváltoztatását, mégpedig oly módon, hogy az új terminus tartalmazza a metabolikus vagy az inzulinrezisztencia fogalmat (6).
2009-ben az Európai Májkutatási Társaság (EASL) állásfoglalása is ajánlotta, hogy el kellene hagyni a nem alkoholos definíciót, helyette a metabolikus zsírmáj és a metabolikus steatohepatitis lehetne megfelelő, ami elismerné az inzulinrezisztencia potenciális oki szerepét NAFLD/NASH-ben (7). Brunt a patológus szempontjából kérdőjelezte meg az elnevezés pontosságát, és a számos felvetődött ajánlás között említette a metabolikus szindróma steatohepatitist és az obesitassal társult zsírmájbetegséget (8).
Eslam és munkatársai 2019-ben konszenzust kezdeményeztek egy megfelelőbb NAFLD nómenklatúra kidolgozására (9). Ennek eredményeképp 2020-ban 22 országból 32 hepatológus (Delfi-metódust alkalmazva) megegyezésre jutott: a NAFLD helyett a metabolikus diszfunkcióval társult zsírmájbetegség (metabolic dysfunction-associated fatty liver disease, MAFLD) terminust javasolták, és kidolgozták az így elnevezett kórkép diagnosztikus kritériumrendszerét (10, 11).
Definíciók:
NAFLD: steatosis a hepatocyták >5%-ában, a jelentős (>20-30 g/nap) alkoholfogyasztás és a májbetegség (steatosis) egyéb okainak kizárása mellett.
NASH: a májhisztológiában steatosis, májsejtek ballonképződése, lobularis gyulladás, fibrózissal vagy anélkül. (A diagnózis májbiopsziát igényel!)
Metabolikus diszfunkcióval asszociált zsírmájbetegség (MAFLD)
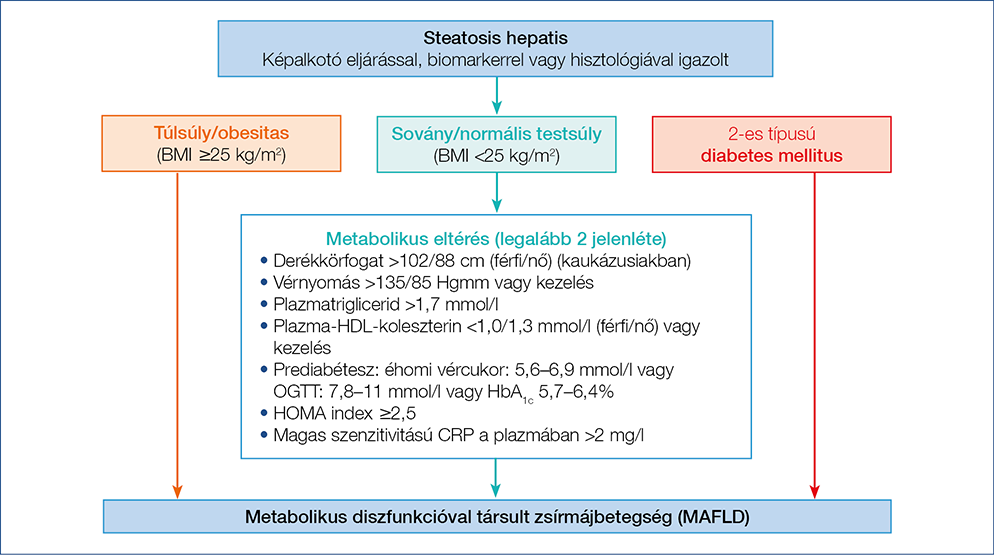
A MAFLD koncepcióban a kiindulópont, hogy a metabolikus májbetegség hátterében komplex patofiziológiai folyamatok zajlanak, ezért egyetlen diagnosztikus próba sem alkalmas önmagában a kórismézésre (11). A MAFLD diagnózisa független az alkoholfogyasztástól, vagy más együtt előforduló steatosist okozó betegségtől, viszont függ a képalkotó eljárással, biomarkerrel vagy hisztológiával igazolt steatosistól, és további három kritérium közül legalább egy jelenlététől: ezek a) a túlsúly/obesitas, b) a 2-es típusú diabétesz és c) a metabolikus zavar (diszfunkció).
Az 1. ábra a MAFLD diagnózis összetevőit mutatja, beleértve az anyagcserezavarra utaló 7 kockázati tényezőt, amelyek közül legalább 2 jelenléte esetén igazolt a „metabolikus diszreguláció” (11).
MAFLD-ben az új kritériumrendszer nem különbözteti meg a tiszta steatosist és a steatohepatitist (NASH-t), ehelyett a betegség súlyosságát állapítja meg az aktivitás és a stádium (fibrózis) alapján.
A steatosis kimutatására a gyakorlatban az elsőként, kiterjedten használt modalitás az ultrahang, hátránya, hogy a 20% alatti zsírtartalmat nem mutatja. Hasznos lehet a kvantitatív zsírmeghatározásra is alkalmas, a tranziens elasztográfiához kapcsolt kontrollált ultrahangelnyelési mutató (controlled attenution parameter, CAP). Ezen a téren a drágább, nehezebben elérhető mágnesesrezonancia-spektroszkópia (magnetic resonance spectroscopy, MRS) és a mágnesesrezonancia-képalkotás-protondenzitás-zsírfrakció (magnetic resonance imaging proton density fat fraction, MRI-PDFF) jelentik az egyelőre főként kutatási célból használt, nagy érzékenységű vizsgáló eljárásokat.
A steatosis biomarkere az epidemiológiai vizsgálatokra alkalmas zsírmájindex (fatty liver index, FLI), amely a testtömegindex, a gamma-glutamil-transzferáz (GGT) és a szérumtriglicerid értéke alapján online kalkulátorral számítható (www.FLI online calculator).
MAFLD-ben a sejtkárosodás és a gyulladásos aktivitás a NAFLD-aktivitásscore (NAFLD Activity Score, NAS) (steatosis 0-3, inflammáció 0-3, ballonképződés 0-2) alapján igazolható hisztológiailag. (Aktivitást a ≥4 pont jelent.)
A gyulladásos aktivitás fokozódásával progrediál a fibrózis, ami a hisztológia vagy a nem invazív fibrózismarkerek révén követhető. Ezek közül a legismertebbek az aszpartát-aminotranszferáz/thrombocyta hányados (APRI score) és a fibrózis-4 (FIB-4) index (életkor, GOT, GPT, thrombocytaszám alapján) – ez utóbbi a gyakorlatban egyre kiterjedtebben használt, könnyen elérhető lehetőség (www.FIB-4 online calculator). A fokozott májfibrózisscore (enhanced liver fibrosis, ELF score), a szérum prokollagén III N-terminál peptid, a hialuronsav és a mátrix-metalloproteináz szöveti inhibitor (TIMP) szint értékein alapul.
(Az 1. táblázat a steatohepatitis és a fibrózis fontosabb biomarkereit foglalja össze.)
1. táblázat: A MAFLD diagnosztikájában használatos fontosabb mutatók, pontrendszerek

Az elasztográfiák a májtömöttség vizsgálata révén adnak támpontot a fibrózis fokáról, e téren elsősorban a vibrációkontrollált tranziens elasztográfia (VCTE) és a mágneses rezonanciás elasztográfia (MRE) említhető.
A MAFLD-cirrózis típusos hisztológiai kép hiányában is megállapítható, ha a MAFLD diagnózisának megfelelő metabolikus diszfunkció (1. ábra) jelenléte mellett korábbi májbiopsziával MAFLD-ot (!) dokumentáltak, vagy képalkotó eljárással steatosist igazoltak.
1. ábra: A MAFLD diagnózis kritériumai (11)
A túlsúly/obesitas a normális testsúlyhoz képest növeli a mortalitást. Megkülönböztetnek ún. „metabolikusan egészséges” obesitast és „metabolikusan egészségtelen” obesitast (lásd a MAFLD diagnózisban szereplő 7 abnormalitást), de a kardiovaszkuláris (CV) betegség kockázata tekintetében nincs lényeges különbség. A MAFLD-betegek 20%-a sovány (alacsony BMI), de ha visceralis zsírfelhalmozódás (nagy derékkörfogat) áll fenn, akkor a soványság nem véd meg a CV szövődményektől.
A metabolikus diszfunkció korai indikátora a steatosis, ez tükrözi a visceralis adipositast, ami az alapja a citokinek és a hormonok kiváltotta, alacsony fokú krónikus gyulladásnak és az inzulinrezisztenciának MAFLD-ben.
A 2-es típusú diabéteszben szenvedők 56-70%-ának van steatosisa.
A MAFLD „ernyőterminus”: különböző altípusai lehetnek, pl. genetikai variánsok vagy epigenetikai faktorok módosíthatják a klinikai képet, vagyis a MAFLD „komplex betegség”: genetikai és környezeti tényezők kölcsönhatásának az eredménye.
Genetikai variánsoknak megfelelő szubfenotípusok: a patatinszerű foszfolipáz domént tartalmazó protein-3 (patatin-like phospholipase domain contaning protein 3, PNPLA3), a transzmembrán 6 szupercsalád 2 tagja (transmembrane 6 superfamily member 2, TM6SF2), a membránkötött O-aciltranszferáz domént tartalmazó fehérje-7 (membran bound O-acyl-transferase domain containing 7, MBOAT7) és a hidroxysteroid 17 béta-dehidrogenáz 13, HSD17B13) génpolimorfizmusokkal kapcsolatosak.
Kettős etiológiájú kórformák. Ha jelentős alkoholfogyasztás is fennáll, kettős etiológiájúnak tekinthető a májbetegség. (Jelentős mennyiségnek számít nők esetén >2 ital/nap, férfiak esetén >3 ital/nap. Az európai irányelvek szerint 1 ital = 10 g, az USA-ban 1 ital 14 g alkoholnak felel meg). Ugyancsak kettős etiológiájú a betegség egyéb steatosist okozó kórképekkel, a steatosis ritka alternatív okaival való együttes előfordulás esetén is, amelyek tehát nem zárják ki a MAFLD diagnózist, pl. vírushepatitis, gyógyszer, cöliákia, a lipidanyagcsere örökletes zavarai, familiáris hypercholesterinaemia, lipodystrophia, Wilson-kór esetén.
A gyógyszerkutatási vizsgálatokban az említett diagnosztikus kritériumoknál a bevonási kritériumok szigorúbbak a homogén beteganyag biztosításához.
A javasolt egyszerű kritériumrendszer célja a személyre szabott betegellátás és a klinikai vizsgálatok támogatása. Mindezt a jövőben még szükségesnek tartják validálni mind a klinikai gyakorlatban mind pedig a kutatások során.
A „NAFLD vagy MAFLD” vita
Az új terminusszal szemben az első ellenvéleményt Younossi és munkatársai (12) fogalmazták meg. Bár egyetértettek abban, hogy MAFLD pontosabban és pozitívabban tükrözheti a betegség kockázati tényezőit, mint a NAFLD, mégis a változtatást idő előtti döntésnek tartották. Szerintük a NAFLD elnevezés épphogy tudatosulni kezd a belgyógyászok/kardiológusok között, most az új név csak zavart okozhat. A döntéshozók és a gyógyszerfejlesztők célpontjában ma a betegség súlyos formája, a NASH szerepel. Az új terminológiában a NASH diagnózis megszűnése veszélyezteti a gyógyszerkutatás és a biomarker-vizsgálatok jóváhagyását. Szükség lenne a betegség molekuláris alapjainak jobb megismerésére. A változtatások sokkal szélesebb körű társadalmi egyeztetést igényelnek, minden érdekelt bevonásával, így nemcsak a hepatológusok, hanem a betegegyesületek, gyógyszergyárak, hatóságok, orvostársaságok és a kutatásokat finanszírozók részvételét is.
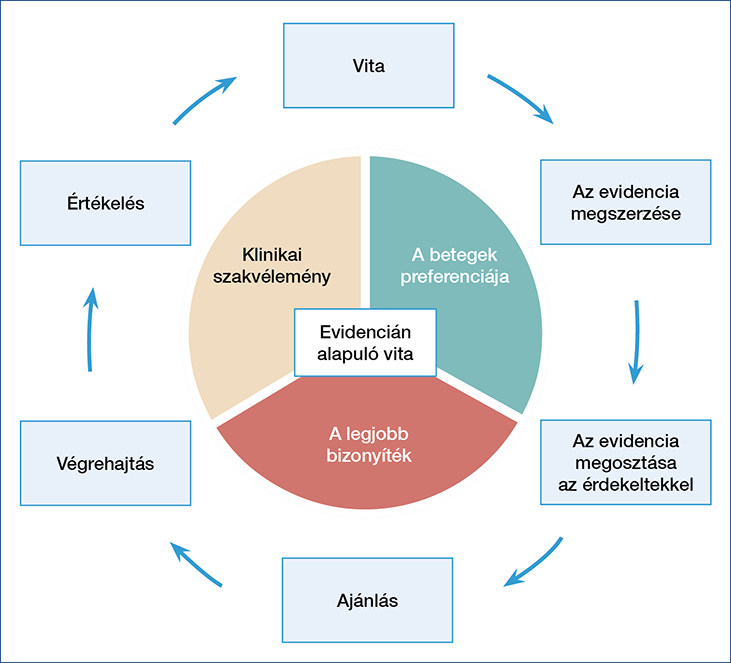
Fouad és munkatársai nagyra értékelték, hogy a „negatív kritériumokon”, az „antidefiníción” alapuló diagnózis helyett a MAFLD gyakorlati kritériumokat tartalmaz (13, 14). Fontos, hogy az alkohol és egyéb, steatosist okozó tényező kizárása nem követelmény, azzal együtt, hogy a betegségspektrum rendkívül heterogén a tiszta steatosistól a „kriptogén cirrózisig”. Eddig az egészségügyi stratégiákban a „nemmel kezdődő” NAFLD-terminus kevés figyelmet kapott, mintha nem lenne fontos a betegség (trivializáció). A patofiziológiát hangsúlyozó új elnevezés előrelépést hozhat e téren, növelheti az odafigyelést. Eddig a gyakorlat nagyon sokszor eltért a hivatalos ajánlásoktól, irányelvektől. Másrészt, az alkohol szó előfordulása a NAFLD diagnózisban stigmatizációt jelenthet. Ezenkívül a metabolikus májbetegség kockázatának kitett egyénekben igen alacsony fokú tudatosságot lehetett megállapítani. Kimutatták, hogy az ilyen egyéneknek csak 6%-a van tudatában az egészségi állapotával. De hasonlóképp, az alapellátást végzők között is alacsonynak (4%) találták a NAFLD ismertségét és a diagnózis lehetőségeit. Mindez pedig a betegség késői felismeréséhez és késői kezelésbe vételéhez vezethet. E téren az előrelépés még időt, a patogenezis további kutatását és vitákat igényel, csak így lehet számítani a változtatások fokozatos elfogadására (2. ábra).
2. ábra: A NAFLD/MAFLD – a bizonyítékon alapuló vita folyamata
Mantovani és Dalbeni (15) az új elnevezést fontosnak vélte, mivel az hangsúlyozza a metabolikus tényezők (az inzulinrezisztencia, az abdominalis obesitas és a diabétesz) szerepét, javítja a betegséghez társuló CV kockázatok identifikálását, és kizárja az alkohollal kapcsolatos túlzott leegyszerűsítést. Megjegyzik még, hogy a MAFLD dinamikus betegség, a kóroki metabolikus tényezők idővel változhatnak, az epigenetikai faktorok, az életkor, az etnikum, az életmód mind kölcsönhatásban vannak, és ezek a tényezők betegről betegre eltérhetnek. A MAFLD interdiszciplináris kezelést igénylő kórkép, ez pedig információcserét kíván a különböző specialisták, a hepatológusok, endokrinológusok, belgyógyászok, kardiológusok, nefrológusok és a patológusok között. A NAFLD növekvő pandémiájával együtt nőni fog a CV betegek száma, mindez szükségessé teszi e téren a nemzetközi szakértők és tudományos társaságok együttműködését a jövőben. Mantovani (16) újabb dolgozatában kiemeli, hogy számos kutató, legalább elméletileg megfelelőnek tartja a MAFLD koncepciót, amely jobban identifikálja azokat a zsírmájas egyéneket, akikben különösen nagy a szövődmények kockázata.
Tilg és Effenberger (17) egyetértett az új elnevezés indokoltságával, bár probléma a betegség heterogenitása, az altípusok és a kórlefolyás variabilitása, továbbá a „metabolikusan egészséges obesitas”, amit az elhízottak 45%-ában találtak. Kérdés, hogy ez az állapot benignus-e: jár-e CV kockázattal, és vezet-e fibrózisra? A metabolikus diszfunkció jele kétségtelenül a steatosis, de steatosist sok más tényező is okozhat, bizonyos gyógyszerektől a Wilson-kórig, fontos ezért az egyéb metabolikus kockázati tényezők figyelembevétele is. A szerzők szerint a MAFLD koncepciója közelebb hozza a betegséget a realitáshoz, nemcsak a patofiziológiához, hanem a 2-es típusú diabéteszhez is, és felhívja a figyelmet a diabetológusok és hepatológusok együttműködésére ezen a téren. Ugyanakkor hiányolják a metabolikus steatohepatitis fogalom beiktatását a MAFLD-koncepcióba.
Herman szerint az új elnevezés kevésbé pejoratív, a betegek jobban elfogadják az olyan diagnózist, amely jelzi az okot, és nem az ok hiányát (18). Zavart okozhat azonban az új kritériumrendszer a jelenleg folyó klinikai vizsgálatokban a betegség stádiummeghatározását illetően. A szerző tisztázni javasolja NAFLD heterogenitásának, kialakulásának és progressziójának molekuláris szintű alapjait egy új nómenklatúra bevezetése előtt.
Lin és munkatársai szerint az alkoholos májbetegség és a metabolikus zsírmájbetegség elkülönítésének problémája, hogy a MAFLD-betegek között is sok az alkoholt fogyasztó, ugyanakkor az alkoholos májbetegségben szenvedők között gyakori a metabolikus diszfunkció (19). Az együttes előfordulás tehát általános, nehéz a két csoportot az etiológia szerint megkülönböztetni. A szerzők e kérdéssel kapcsolatban populációszintű vizsgálatot végeztek. Az USA Nemzeti Egészségügyi és Táplálkozási szűrőprogramjában 1988–1994 között regisztrált 13 083 olyan egyén adatait dolgozták fel, akiknek volt ultrahang- és májpróbaleletük, illetve az alkoholfogyasztásra vonatkozó dokumentációjuk. A MAFLD diagnózisát az eredetileg javasolt követelmények szerint állították fel, az ún. nem MAFLD csoportot azok a zsírmájas egyének alkották, akik nem feleltek meg a MAFLD-kritériumoknak. A NAFLD-et a szokásos definíció szerint (a >20-30 g/nap alkoholfogyasztás és az egyéb okok kizárása alapján) állapítottak meg. MAFLD esetén az alkoholt fogyasztók (>28 g/nap) és nem fogyasztók alcsoportjait is elkülönítették. A vizsgált populációban 31,4% volt a MAFLD, és 33,2% a NAFLD prevalenciája. A MAFLD-betegek a NAFLD-hez képest idősebbek voltak, magasabb testtömegindexszel, gyakoribb metabolikus zavarral (diabétesz stb.), magasabb májenzim- és fibrózisscore-értékekkel. A MAFLD és az alkohol együttes előfordulása fiatalokban volt gyakori, ez magasabb enzimszintekkel, ritkább metabolikus diszfunkcióval, magasabb fibrózisscore-ral járt, jelezve a kettős károsító hatást és a cirróziskockázat növekedését. A szerzők arra következtetnek, hogy a MAFLD-kritériumrendszer a mindennapi gyakorlatban alkalmas a progresszió kockázatának kitett zsírmájbetegek kiszűrésére.
Lee és munkatársai a koreai nemzeti egészségügyi szűrőprogramban szereplő 9,5 millió egyén adata alapján meghatározták a NAFLD, illetve a MAFLD diagnózis prevalenciáját és a társuló CV események (infarktus, stroke, szívelégtelenség) kockázatát (20). A programban részt vevők 28%-ában igazoltak NAFLD-et, és 37,8%-ában MAFLD-et. A steatosisban nem szenvedő kontrollpopulációhoz képest a MAFLD-betegekben a CV kockázat (HR: 1,43) magasabb volt, mint a NAFLD diagnózisa esetén (HR: 1,09), vagyis a MAFLD-kritériumok alapján jobban kiszűrhetők a CV betegség szempontjából veszélyeztetettek (20).
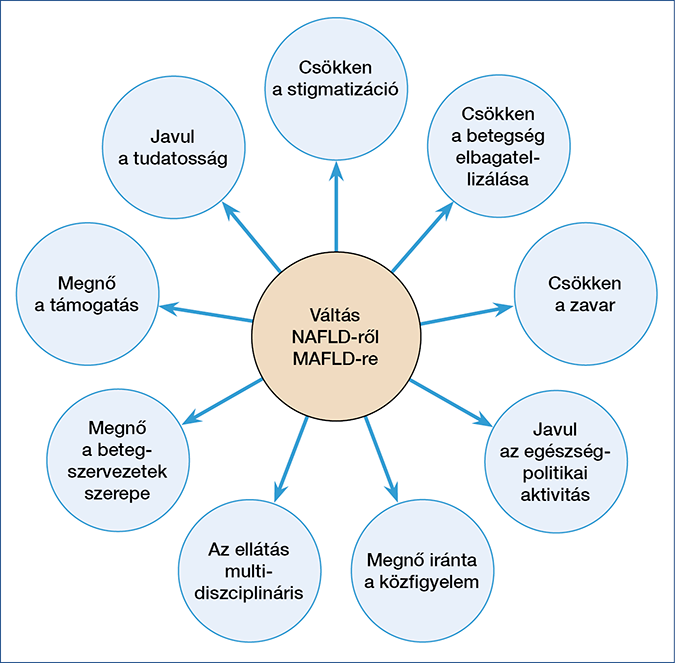
Shiba és munkatársai 23 ország 27 orvostársasága, illetve betegegyesülete képviseletében tették közzé azt az állásfoglalást, amely támogatja a NAFLD új elnevezését, különösen a betegek szempontjából (21). Kiemelik, hogy a névből az alkohol elhagyása javítani fogja az érintettek hozzáállását és a betegség tudatosulását, csökken a diagnózis általi stigmatizáció (3. ábra). Ez segíti a holisztikus betegellátást, a stigmatizáció ugyanis negatív hatású az önértékelésre és az életminőségre, a kezeléssel kapcsolatos együttműködésre. A kizáráson alapuló NAFLD diagnózis félreértésre vezet a betegség természetére vonatkozóan, elmarad annak felismerése, hogy a betegségben az anyagcserezavar a meghatározó. A trivializáció a betegség jelentőségének minimalizálása, elbagatellizálása. Emiatt a betegség nem kap prioriást az alapellátásban, a következmény pedig a betegség késői stádiumban (kriptogén cirrózis) való felfedezése. A NAFLD-betegek 95%-a nem tud a betegségéről, vagy nem tudatosul benne, hogy az obesitas májbetegséghez vezethet. Ez csökkentheti az adherenciát pl. a testsúlycsökkenő intervenciókhoz. A diagnózisban szereplő metabolikus jelző előmozdíthatja a többi anyagcsere-betegséggel foglalkozó specialisták, az obezitológusok, diabetológusok, endokrinológusok, kardiológusok, nefrológusok közötti együttműködést, ami előrelépést hozhat a multidiszciplináris betegellátásban.
3. ábra: A névváltoztatás feltételezett előnyei a betegek szempontjából
Megoldatlan a MAFLD terápiája, a nagy kockázatú csoportok szűrése, annak a széles körű felismerése, hogy a kórkép komoly közegészségügyi problémát jelent. A nómenklatúra változtatását eddig az ázsiai-óceániai (22), a latin-amerikai (23), a középkelet-észak-afrikai (24) és a kínai (25) hepatológiai társaságok fogadták el.
Egy évvel a MAFLD nómenklatúra ajánlása után Singh és munkatársai úgy vélik, hogy bár a javaslat sok támogató vélemény kapott, vitatható az új elnevezés tudományos megalapozottsága, nem segíti a haladást, a koncepció nem vesz figyelembe sok eddig bizonyított patofiziológiai tényezőt, és eltúlozza a metabolikus diszfunkció szerepét (26). A szerzők kiemelik, hogy a zsírmájnak többtényezős a patogenezise, beleértve a genetikai, epigenetikai faktorokat, az epesav-metabolizmust, a nukleáris hormonreceptorokat és a bélmikrobiótát is, ugyanakkor az esetek felében nincs metabolikus zavar vagy inzulinrezisztencia. A betegség az új kritérium révén nem lett kevésbé heterogén. A névben a nem jelző elfogadott a terminológiában (pl. non-Hodgkin-lymphoma, vagy nem kissejtes tüdőrák). Az alkohol tagadása inkább destigmatizál, a metabolikus pedig leegyszerűsít. A kutatásokat illetően probléma, hogy az eddigi protokollok a NAFLD-kritériumokon alapultak, a korábbi adatok így a MAFLD-vizsgálatokhoz nem használhatók, az új név inkább visszalépést eredményez. A megoldást a betegség patofiziológiájának a jobb megismerésében látják, semmint a terminológia megváltoztatásában.
Georg és munkatársai szerkesztőségi közleményben foglalták össze az új elnevezéssel kapcsolatos megnyilvánulásokat, hangsúlyozva, hogy a vitában integrálni kell a szakértői véleményeket és az evidenciákat (27). A vélemény megváltoztatható egyik vagy másik irányban – az evidenciák alapján. Az adatok és a bizonyítékok segítenek feloldani az ellentmondásokat, és ez a MAFLD jövőbeni elfogadására is érvényes. Az új kritérium nem zárja ki azokat a betegeket, akiknek egyidejűleg több kockázati tényezőjük is van, ugyanakkor fontos megkülönböztetni a CV kockázattal járó és az anélküli steatosis alcsoportot. A MAFLD-steatohepatitises betegek hisztológiai vizsgálata lényeges a fibrózisos és nem fibrózisos alcsoportok elkülönítése szempontjából. A szerzők szerint gyűjteni kell az adatokat az új definíció működéséről, és arról, hogy milyen szubtípusokat szükséges még elkülöníteni, de mindez időt vesz igénybe. Az evidencián alapuló vita fog dönteni az új név sorsáról.
Addig is a koncepció előrelépést jelenthet a metabolikus diszfunkcióval társult zsírmájas betegek stratifikációjában és kezelésében.
Újabban Foudad és munkatársai (28) is a fenti nézetet támogatják. Szükségesnek tartják még vizsgálni a változtatás egészségügyi-gazdasági hatásait a standard ellátással összehasonlítva.
Javasolják újragondolni a konszenzusra jutás mintáit, oly módon, hogy azok kritikusan tekintsék a bizonyítékokat – a vétózás helyett. A bizonyítékok mutassák az utat! – hangsúlyozzák.
Végül említendő, hogy 2022-ben szakértők multidiszciplináris csoportja (91 országból 218 résztvevővel) a Delfi-metódust alkalmazva konszenzust alakítottak ki abból a célból, hogy felhívják a figyelmet a NAFLD-re mint globális közegészségügyi problémára (29). Ebben ajánlásokat fogalmaztak meg az ügyben érintettek, a döntéshozók, az egészségügyi ellátók, a civilszervezetek és a kutatóintézetek számára a betegség epidemiológiájával, a betegséggel kapcsolatos tudatosság fokozásával és ellátásával kapcsolatban. Az állásfoglalásban kitérnek a NAFLD nómenklatúra kérdésére is.
Elismerve, hogy nagy regionális hepatológiai társaságok támogatják a változtatást, a vitát nem tartják lezártnak, és széles körű együttműködéssel további elemzéseket javasolnak a változtatás hatásainak tekintetbevételével.

Következtetés
A ma leggyakoribb májbetegségnek számító NAFLD elnevezéséről két évtizede folyó vita nem ért véget. A kórkép patogenezisére vonatkozó kutatások folytatása, a várható újabb eredmények és a minden érdekelt bevonásával tervezett konzultációk révén előrelépés történhet a döntésben a javasolt új terminológiát és a diagnosztikus kritériumokat illetően.
2. Adler M, Schaffner. Fatty liver hepatitis and cirrhosis in obese patients. Am J Med 1979; 67: 811–816.
3. Ludwig J, Viggiano TR, McGill DB, et al. Non-alcoholic steatohepatitis: Mayo Clinic experiences with a hitherto unnamed disease. Mayo Clin Proc 1980; 55: 434–438.
4. Schaffner F, Thaler H. Non-alcoholic fatty liver disease. Prog Liver Dis 1986; 8: 283–298.
5. Neuschwander-Tetri BA, Caldwell SH. Non-alcoholic Steatohepatitis: Summary of an AASLD Single Topic Conference. Hepatology 2003; 37: 1202–1219.
6. Loria P, Lonardo A, Carulli N. Should non-alcoholic fatty liver disease be renamed? Digest Dis 2005; 23: 72–82.
7. Ratziu V, Bellentani S, Cortez-Pinto H, et al. A position statement on NAFLD/NASH based on the EASL 2009 special conference. J Hepatol 2010; 53: 372–384.
8. Brunt EM. What is in a NAame. Hepatology 2009; 50: 663–667.
9. Eslam M, Sanyal AJ, George J. Toward more accurate nomenclature for fatty liver diseases. Gastroenterology 2019; 157: 590–593.
10. Eslam M, Newsome PN, Anstee QM. MAFLD: A consensus-driven proposed nomenclature for metabolic associated fatty liver disease. Gastroenterology 2020; 158: 1999–2014.
11. Eslam M, Newsome PN, Anstee QM, et al. A new definition for metabolic dysfunction- associated fatty liver disease: An international expert consensus statement. J Hepatol 2020; 73: 202–208.
12. Younossi ZM, Rinella ME, Sanyal AJ, et al. From NAFLD to MAFLD: Implications of a premature change in terminology. Hepatology 2020; 73: 1194–1198.
13. Fouad Y, Waked I, Bollipo S, et al. What is in a name? Renaming „NAFLD” to „MAFLD”. Liver Internat 2020; 40: 1254–1261.
14. Fouad Y, Elwakil R, Elsahhar M, et al. The NAFLD-MAFLD debate: eminence vs. evidence. Liver Internat 2021; 41: 255–260.
15. Mantovani A, Dalbeni A. NAFLD, MAFLD and DAFLD. Clin Liver Dis 2020; 14: 35.
16. Mantovani A. MAFLD vs. NAFLD Where we are? Dig Liv Dis 2021; 3: 9.
17. Tilg H, Effenberger M. From NAFLD to MAFLD. When pathophysiology succeeds. Nat Rev Gastroenterol Hepatol 2020; 17: 387–388.
18. Herman MA. Metabolic liver disease – What’s in a name? Nat Rev Endocrinol 2021; 17: 79–80.
19. Lin S, Huang J, Wang M. Comparison of MAFLD and NAFLD: diagnostic criteria in real world. Liver Internat 2020; 40: 2082–2089.
20. Lee H, Lee Y-h, Kim SU, et al. Metabolic dysfunction-associated fatty liver disease and incident cardiovascular disease risk: a nationwide cohort study. Clin Gastroenterol Hepatol 2021; 19: P2138–2147.
21. Shiba G, Korenjak M, Eskridge T, et al. Redefining fatty liver disease: an international patient perspective. Lancet Gastroenterol Hepatol 2021; 6: 73–79.
22. Eslam M, Sarin SK, Wong VWS, et al. The Asian Pacific Association for the Study of the Liver Clinical practice guidelines for the diagnosis and management of metabolic associated fatty liver disease. Hepatol Int 2020; 14: 889–919.
23. Menez-Sanchez N, Arrese M, Gadano A, et al. The Latin American Association for the Study of the Liver (ALEH) position statement on the redefinition of fatty liver disease. Lancet Gastroenterol Hepatol 2021; 6: 65–72.
24. Shiha G, Alswat K, Khatry MAI, et al. Nomenclature and definition of metabolic-associated fatty liver disease: a consensus from the Middle East and North Africa. Lancet Gastroenterol Hepatol 2021; 6: 57–64.
25. Nan Y, An J, Bao J, et al. The Chinese Society of Hepatology position statement on the redefinition of fatty liver disease. J Hepatol 2021; 75: 454–461.
26. Shingh SP, Anirvan P, Khanderwal R, et al. Non-alcoholic fatty liver disease (NAFLD) name change: requiem or reveille? J Clin Transl Hepatol 2021; 9: 931–938.
27. Georg J, Gish RG, Geiger A. MAFLD and cardiovascular events. What does the evidence show? Clin Gastroenterol Hepatol 2021; 15. March.
28. Fouad YM, Méndez-Sanchez N, Zheng M-H. One not like the other: The weakness of the blood sugar-MAFLD analogy. J Hepatol 2022; 76: 482., 484.
29. Lazarus JV, Mark HE, Anstee QM, et al. Advancing the global public health agenda for NAFLD: a consensus statement. Nat Rev Gastroenterol Hepatol 2022; 19: 67–71.
