Klinikai kérdések / Clinical questions
Efficacy and therapeutic mechanism of mesenchymal stem cell therapy in the management of perianal fistulizing Crohn’s Disease
Summary
Perianal fistula formation is common and therapy-resistant complication of Crohn's Disease with a lifetime prevalence of 21-23%. Biological treatment represents a great breakthrough in their treatment; however, the rate of complete fistula closure can be achieved in only 22-36% of cases during the one-year treatment. Mesenchymal stem cell transplantation is a new, complementary therapeutic alternative in the management of conventional combined surgical and drug resistant fistulas. Its most important advantage is that it not only inhibits the inflammation, but also directly promotes the regeneration process of damaged tissue. The allogeneic adipose tissue derived mesenchymal stem cells (darvadastrocel) therapy has become available in Hungary therefore, our review article aims to summarize the effectiveness and therapeutic mechanism of stem cell transplantation in the management of perianal fistulizing Crohn's Disease.
A perianalis sipolyképződés a Crohn-betegség gyakori, terápiarezisztens komplikációja, amelynek élettartam-prevalenciája 21-23%-ra tehető. A biológiai kezelés áttörést jelentett a kezelésükben, de a komplett fisztulazáródás aránya mindössze 22-36% az egyéves kezelés során. A mesenchymalis őssejt- transzplantáció új, kiegészítő terápiás alternatívát jelent a hagyományos kombinált sebészi és gyógyszeres kezelésre rezisztens sipolyok esetében. Előnye, hogy az immunszuppresszív hatás mellett direkt módon elősegíti a szöveti gyógyulást. Mivel Magyarországon is elérhetővé váltak a zsírszöveti eredetű allogén mesenchymalis őssejtek, azaz a darvadastrocel kezelés, az összefoglaló közleményünk célja áttekinteni az őssejtkezelés hatásmechanizmusát és eredményességét.
Bevezetés
A perianalis fisztulázó Crohn-betegség (Crohn’s disease, CD) a gyulladásos bélbetegség (inflammatory bowel disease, IBD) azon megjelenési formája, amelyre a vékony és a vastagbél krónikus, idiopátiás gyulladása mellett a perianalis régió területén megjelenő sipolyok és tályogok jellemzők (1). Élettartam prevalenciája 21-23%-ra tehető CD-ben, és előfordulási gyakorisága a betegségfennállással párhuzamosan emelkedik: a kumulatív incidenciája 1 éves betegségfennállás után 12%, 5 év után 15%, 10 év után 21%, míg 20 évet meghaladónál már minden negyedik beteg esetében észlelhető (2, 3, 4). A sipolyképződés pontos patomechanizmusa jelenleg nem teljesen ismert. Háttérben fontos szerepe lehet többek között a bélnyárkahártya környezeti tényezőkre adott abnormális immunválaszának, amely a proinflammatorikus citokinek túltermelődéséhez és az effektor T-sejtek aktivációjához vezet (5). A jelenleg alkalmazott kezelések célja ezért a túlzott immunreakció mérséklése, és ezáltal a klinikai remisszió és nyálkahártya-gyógyulás elérése. A terápiás áttörést jelentő biológiai terápiás készítmények a gyulladásos kaszkádban kulcsfontosságú szerepet játszó proinflammatorikus citokinek ellen termelt humán vagy humanizált monoklonáris antitestek. Ide tartozik a tumornekrózis-faktor-alfa (TNF-a) ellenes infliximab, adalimumab, golimumab, certolizumab és etanercept, valamint az integrin-inhibitor vadolizumab és natalizumab, illetve az interleukin-12 (IL-12) és IL-20 ellenes ustekinumab. A randomizált, kontrollált vizsgálatok megerősítették ezen készítményeknek hatékonyságát a luminalis és perianalis CD-ben egyaránt, ugyanakkor rávilágítottak arra, hogy az esetek 20-50%-ban a fenntartó kezelés során hatásvesztés következik be (6, 7, 8). Mindemellett a komplex sebészi (seton drenázs, tályogfeltárás) és gyógyszeres (antibiotikum, immunszuppresszáns, biológiai) kezelés ellenére a komplett fisztulazáródás aránya mindössze 22-36%-ra tehető az egyéves kezelés során, és magas fisztularekurrenciával kell számolni (9, 20, 11). A biológiai készítmények hátránya, hogy csak immunszuppresszív hatással bírnak, direkt módon nem támogatják a károsodott szövet gyógyulási folyamatát. Az új kezelési alternatívát jelentő mesenchymalis őssejt (mesenchymal stem/stromal cell, MSC) transzplantáció célja ennek a hiánynak a pótlása, mivel – azon túl, hogy gátolja a gyulladást – egyidejűleg a regenerációs folyamatokért felelős sejteket is aktiválja. Klinikai gyakorlati alkalmazása rövid múltra tekint vissza, tapasztalataink egyelőre a kis esetszámú klinikai vizsgálatokból származnak, amelyek többségét eltérő metodikával és végpontokkal végezték el, és főként a rövidtávú eredményesség megítélésre irányultak (12). Ennek ellenére a korai tapasztalatok igen ígéretesek, és azt sugallják, hogy szemben a biológiai kezeléssel, az MSC-kezeléssel elért sipolyzáródás tartós. A biztonságosság kérdésére továbbra is nagy figyelem szegeződik, de az eddigi tanulmányok súlyos adverz eseményt és daganatképződést nem észleltek.
Mesenchymalis őssejtek jellemzői
MSC-nek nevezzük a szövethez rugalmasan kötött multipotens, fibroblast-szerű sejteknek heterogén csoportját, amelyre az önmegújítási képesség mellett az epithelialis és mesenchymalis sejtvonalak irányába (chondroblast, osteoclast, adipocyta stb.) való differenciálódási képesség jellemző. Friedenstein és munkatársai tengerimalac csontvelőből izolálták elsőként ezeket a sejteket, és bizonyították magas replikációs és kolóniaformáló képességüket in vitro körülmények között (13, 14). Ezt követően az MSC-t sikerült azonosítani szinte az összes vaszkularizált szövetben és szerven, többek között a zsírszövetben, köldökzsinórban, fogbélben és kötőszövetben (15, 16, 17). A Nemzetközi Sejtterápiás Társaság (International Society for Cellular Therapy) az alábbi kritériumok alapján állította fel az MSC definícióját:
- laza kötődés a szövetkultúrákban;
- ≥95%-a MSC populációját áramlási citometriás vizsgálattal a CD105, CD73 és CD90 expresszió jellemzi, valamint a sejtepopuláció <2%-a expresszálja a CD45, CD34, CD14 vagy CD11b, CD79α vagy CD19 and HLA-DR sejtfelszíni molekulákat;
- differenciációs kapacitás osteoblast, adipocyte és chondroblast irányába in vitro körülmények között (18) (1. táblázat).
1. táblázat: Mesenchymalis őssejtek jellemzői a Nemzetközi Sejtterápiás Társaság (International Society for Cellular Therapy) definíciója alapján

Ennek ellenére az eltérő szövetből származó MSC-k között eltérés mutatkozik az immunfenotípus és funkció tekintetében (19). A klinikai vizsgálatokban az MSC két típusát, a csontvelői- (bone marrow MSC, BM-MSC), illetve a zsírszöveti (adipose-derived stem cells, ASC) eredetű őssejteket vizsgálták leggyakrabban (20). A hagyományos szervtranszplantációkkal összevetve az MSC-transzplantáció nagy előnye, hogy nincs szükség a donor-recipiens egyeztetésre és megelőző kondicionáló kezelésre a sejtek hipoimmunogenitása és alacsony antigén-prezentációs tulajdonsága miatt: a humán MSC felszínén nem találhatók II-es típusú major hisztokompatibilitási komplexek (MHC-II), kostimulációs molekulák (CD40, CD80, CD86), és I-es típusú humán leukocita antigének (HLA-I) (21, 22). Ennek köszönhetően nemcsak az autológ, hanem az allogén transzplantáció is egyszerűen és biztonságosan kivitelezhető. Ugyanakkor, az utóbbi időben publikált tanulmányok rávilágítottak arra, hogy gyenge immunválasz indulhat a sejtek ellen a dózistól/expozíciótól függően, de az ennek következtében létrejövő rejekció igen lassú a hagyományos allogén transzplantációval összevetve (23).
MSC-terápia hatásmechanizmusa IBD-ben
Az MSC hatása a veleszületett- és szerzett immunitásra sokrétű, amely elsősorban a gyulladásos reakció mérséklésére és a szövetgyógyulás elősegítésére irányul (1. ábra). Az MSC szerepének pontos megértéséhez szükséges az IBD kialakulásáért és progressziójáért felelős diszregulációs immunfolyamatok ismerete.
1. ábra: A mesenchymalis őssejtkezelés hatása a gyulladásos kaszkádra és a regenerációs folyamatra
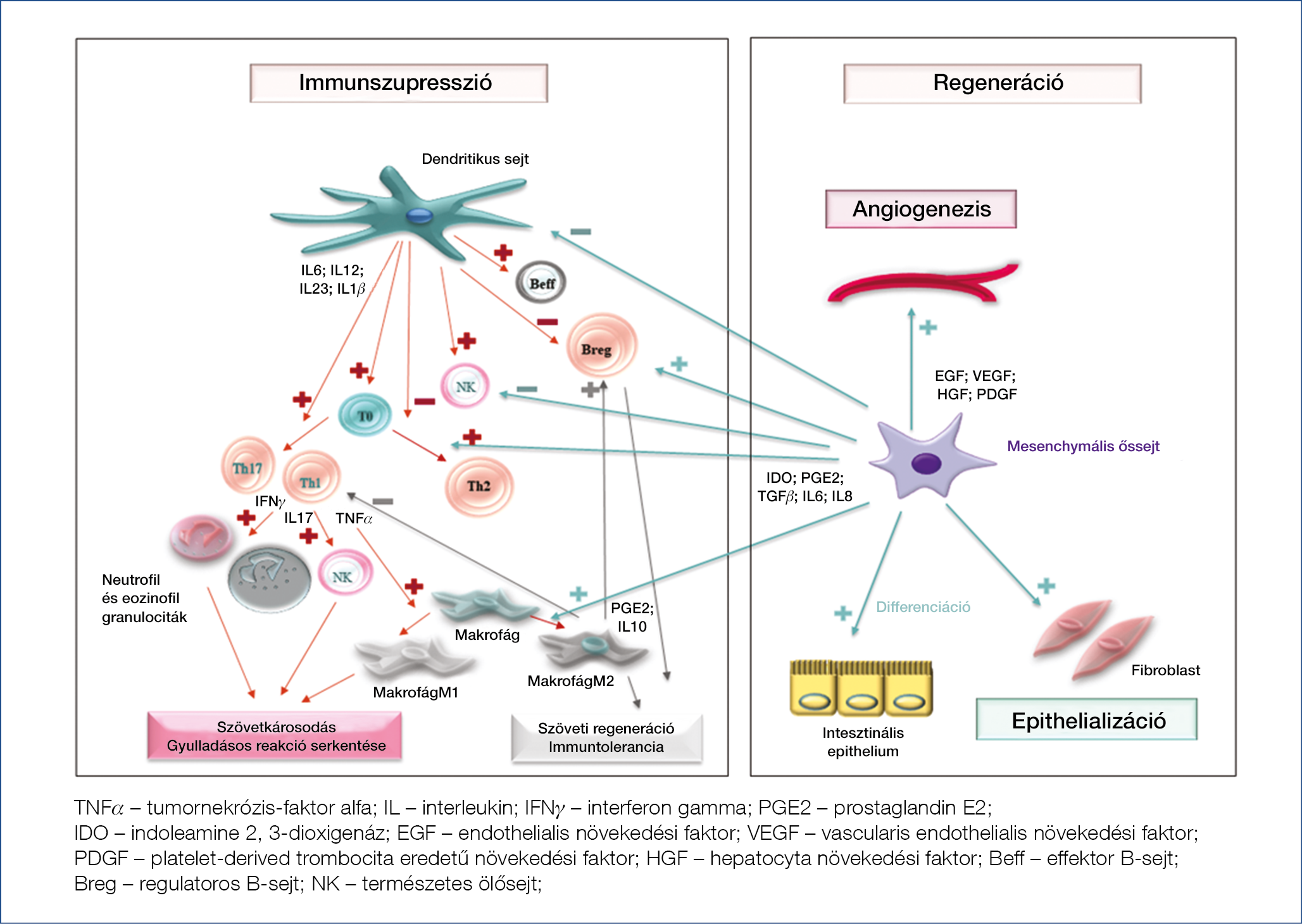
Az IBD immunológiai háttere
Az IBD-ben zajló kóros immunreakcióra jellemző az effektor, 1-es és 17-es típusú, CD4+ T-helper (Th1, Th17) sejtek akkumulációja és a regulátor T-sejtek (Treg) gátlása, amely a proinflammatorikus citokinek túlprodukciójához vezet (interferon [IFN]-g, TNF-a, IL-17, IL-22) (24, 25). Egészséges egyéneknél, a Th1-sejtek fontos szerepet töltenek be az adaptív immunválaszban, azaz a gazdaszervezet patogén ágensekkel szembeni védekezésében. A 2-es típusú toll-like receptorral (TLR-2) rendelkező dendritikus sejtek (dendritic cell, DC) és makrofágok észlelik a bél lumenében található antigéneket, majd bemutatják ezeket a többi immunsejtnek, amely citokin (IL-6, IL-12, IL-23, IL-1b) szekréciót indukál. Ez a jelátviteli út elősegíti a T0-sejtek differenciálódását Th1 és Th17 limfociták irányába, valamint az effektor B (Beff) sejtek aktivációját és proliferációját. A TNF-a, IFN-g és IL-17 szekréció elindítja a mononukleáris fagociták, neutrofil granulociták proliferációját, továbbá proinflammatorikus M1 típusú makofágok és természetes ölősejtek (natural killer cell, NK) érését, amely összességében a bélnyálkahártya károsodását eredményezi. Fiziológiás esetben azonban egyensúly áll fenn a pro- és antiinflammatorikus hatások között. Az M2 fenotípusú makrofágok és a regulátoros DC felelősek az immuntolerancia kialakulásáért. A prosztaglandin-E2 (PGE2) és IL10-expresszió a T0-sejtek Th2 irányú differenciációját és a regulátoros B-limfociták (Breg) proliferációját indítja el, ami csillapítja az immunreakciót és beindítja a szöveti regenerációt (26).
Az MSC immunmodulátoros hatása
Az MSC hatása vonatkozó ismereteink elsősorban állatkísérletes modellekből származnak, és még mindig számos nyitott kérdés maradt. Úgy tűnik az MSC hatása kifejezésre jut a sejtek közti interakciókon (sejtfelszíni molekulák kapcsolata) és parakrin hatásokon keresztül (citokin-
expresszió) egyaránt. IBD egérmodelljének vizsgálata során igazolták, hogy a proinflmmatorikus citokinek, IFN-g, TNF-a and IL1b magas koncentrációja elősegíti a humán eredetű autológ őssejtek migrációját a véráramból a sérült szövetbe, ahol megkezdik több immunregulátoros faktor termelését, amelyek közül kiemelt jelentőségű a PGE2, az IL10, a transzformáló növekedési faktor (transforming growth factor beta, TGF-b), nitrogén-monoxid (NO) és indolamin-2,3-dioxigenáz (IDO) (27, 28, 29). Ezek elősegítik a DC-nek és makrofágoknak a regulátoros fenotípusba való differenciálódását, gátolják továbbá a Th1- és Th17-sejtek proliferációját, aktivációját és citokintermelését. A TGFb stimulálja a Treg és Breg-limfocitákat, növeli azok IL10 expresszióját és csökkenti az IgE-termelést. Ezen folyamatok együttesen a szöveti homeosztázis helyreállásához vezetnek (30, 31).
Az MSC hatása a szöveti regenerációra
Az MSC hatása a szöveti regenerációra több mechanizmussal jön létre. Egyrész magyarázható ez a hatás az MSC más sejtvonal irányába való differenciációs képességével, másrészt a már korábban említett sejt-sejt interakcióval és citokintermeléssel. A parakrin növekedési faktorok (vaszkuláris endothelialis növekedési faktor [vascular endothelial growth factor, VEGFa], angiopoietin-1, TGF-b1, inzulinszerű növekedési faktor [insulin-like growth factor, IGF1]) serkentik a fibroblastok és makrofágok szöveti migrációját, fokozzák az angiogenezist, valamint gátolják a sejtek apoptosisát és a fibrosist.
Az MSC-kezelés alkalmazása Crohn-betegségben
Az MSC-kezelés technikai háttere, kivitelezése
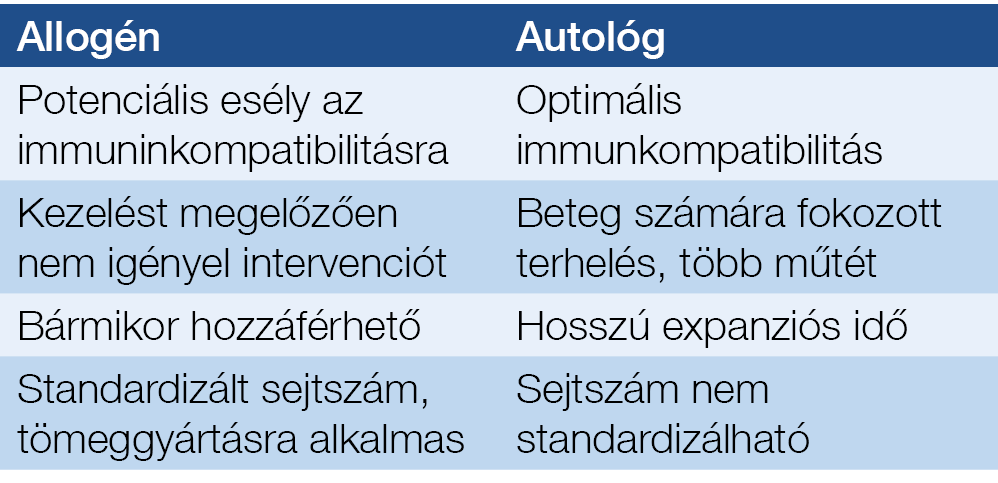
Bár az MSC változó koncentrációban az összes vaszkularizált szövetben és szervben kimutatható, terápiás alkalmazás céljából forrásként csak olyan szervek jönnek számításba, amely viszonylag „nélkülözhető”, nagy mennyiség extrahálható belőle a donor károsodása nélkül, és kellően magas benne az őssejtek koncentrációja (19). Ez alapján a zsírszövet, a csontvelő és köldökzsinórvér tűnik optimális választásnak. A csontvelőhöz képest a zsírszövet lényegesen alacsonyabb MSC-koncentrációval rendelkezik, ez mintegy 3-15×106/100 ml-re tehető, ugyanakkor ez az egyik legnélkülözhetőbb, nagy volumenben hozzáférhető és könnyen extrahálható szövetünk (17). Az MSC-vel szembeni immuntoleranciának köszönhetően az allogén és az autológ sejttranszplantáció egyaránt lehetséges. Az autológ MSC-kezelés legfontosabb limitációját az időigényes és beteg számára megterhelő sejtextrakció és feldolgozási folyamat képezi. Az allogén MSC-transzplantáció esetében lehetőség nyílik a tömegtermelésére, amellyel a beteg számára a felmerülő igény pillanatában, gyakorlatilag bármikor elérhetővé válik a standardizált sejtkoncentrációt tartalmazó készítmény (2. táblázat).
A perianalis CD-ben az őssejtek lokális bevitelére általános anesztéziában történő kisműtét kapcsán kerül sor. Első lépésben a sebész azonosítja a fisztulacsatornákat, eltávolítja a benthagyott setonfonalakat, kitisztítja a járatokat eltávolítva a sipolyok belsejében lévő gyulladásos szövettörmeléket. A sipolynyílás belső szájadékának felszívódó varrófonallal történő zárását követően a sejtszuszpenziót a belső szájadékot övező submucosába, valamint a fiszula teljes hosszában a járatmenti szövetbe injektálja.
2. táblázat: Az allogén és autológ mesenchymalis őssejt-transzplantáció előnyeinek és hátrányainak összevetése a gyulladásos bélbetegségben történő alkalmazás során
MSC-kezelés hatékonyságát értékelő klinikai vizsgálatok
A klinikai vizsgálatok direkt összehasonlítása az eltérő protokollok miatt nem egyszerű. A különbség megnyilvánul a vizsgálatok között az alkalmazott sejtek koncentrációjában, volumenében, forrásában és típusában egyaránt, valamint a beadási gyakoriság, ellenőrzés módja és a végpontok definíciója is eltérő. Minden vizsgálatban két terápiás végpont szerepel: a fisztulák számának csökkenése, valamint a komplett fisztulazáródási arány, ugyanakkor ezen fogalmak definíciója eltérő: néhány vizsgálat ezt fizikális vizsgálat alapján határozza meg, míg másoknál ezt MRI-vizsgálat kell, hogy megerősítse (3. táblázat).
3. táblázat: A mesenchymalis őssejt-transzplantáció perianalis fisztulázó Crohn-betegségben történő alkalmazására irányuló klinikai vizsgálatok eredményeinek összefoglalása.
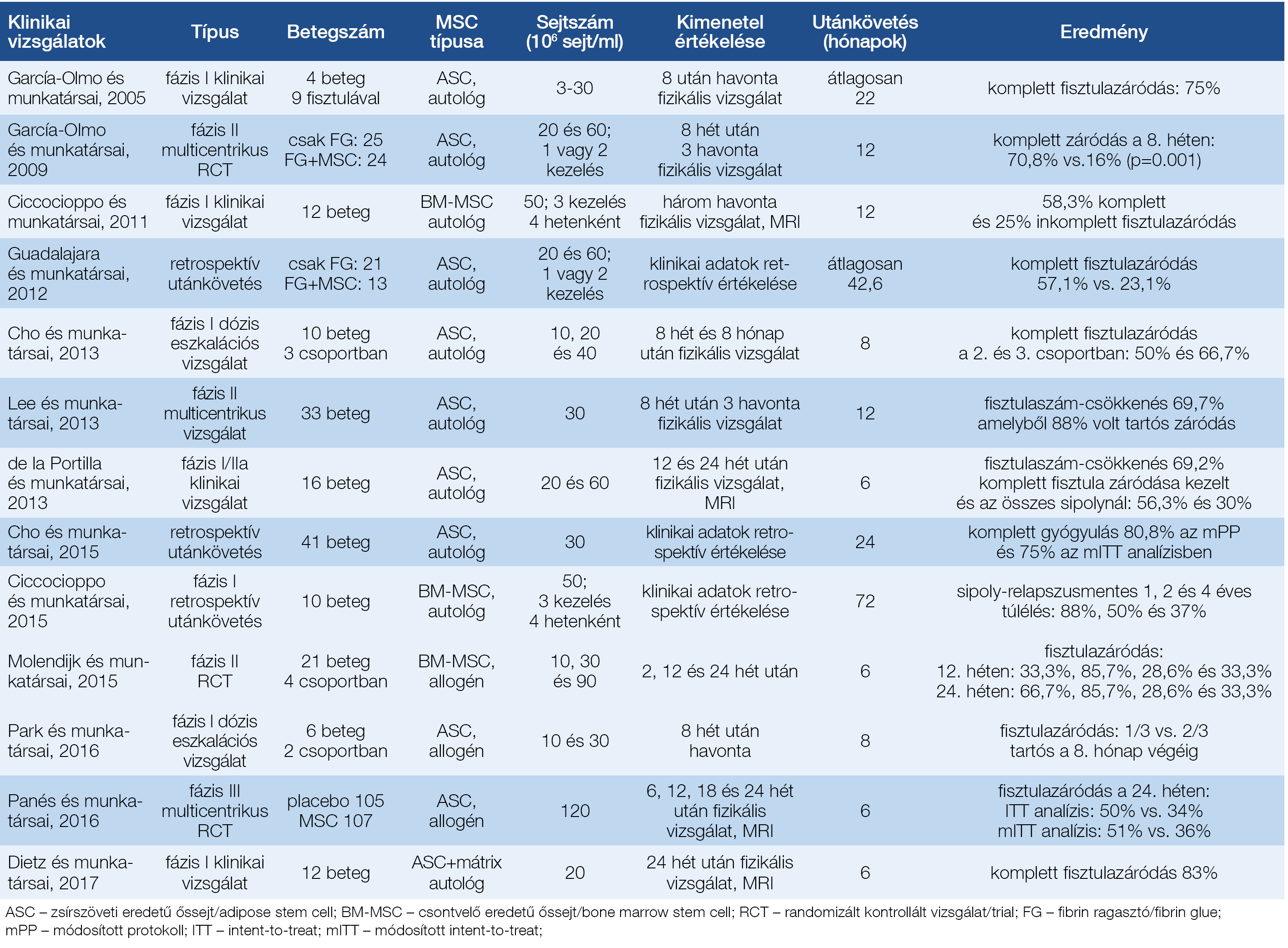
2003-ban García-Olmo és munkatársai publikálták az első sikeres MSC-kezelést, amely során egy fiatal Crohn-beteg nőnél értek el komplett sipolyzáródást szoliter, rekurrens, IFX-kezelésre rezisztens rectovaginalis fisztula autológ ASC transzplantációjával (32). Ezt követően a spanyol munkacsoport az I. fázis klinikai vizsgálatában 4 beteget vont be összesen 9 fisztulával, akiknél a 8 hetes utánkövetés végére 75%-os komplett fisztulazáródási arányt értek el a korábbi protokollt alkalmazva (33). A multicentrikus, randomizált placebokontrollált II. fázis vizsgálatukban hasonló eredményre jutottak. Ebben a kontrollcsoportba sorolt 25 betegnél fibrinragasztót injektáltak a fisztula lumenébe, míg a 24 terápiás karon lévő betegnél ezt ASC-szuszpenzióval kombinálták. A komplett fisztulazáródás aránya a 8. hét végén a terápiás csoportban szignifikánsan magasabb volt: 70,8% vs. 16% (p=0,001) (34). Ezekkel szemben, Ciccocioppo és munkatársa, valamint Portilla és munkatársai alacsonyabb komplett és parciális sipolyzáródásról számoltak be: (58,3% vs. 25% és 56,3% vs. 30%), viszont ezekben a tanulmányokban a terápiás választ MRI-vizsgálat alapján határozták meg (35, 36). Dietz és munkatársai valamint Lee és munkatársai az előzőekkel ellentétben csontvelői eredetű MSC-t alkalmaztak a kezelés során, amellyel hasonlóan magas záródási arányt tapasztaltak (83% és 68,7%), amelyekből 88% tartósnak bizonyult (37, 38).
Az optimális terápiás és maximálisan tolerálható MSC-dózis minden újonnan bevezetett készítmény esetén kulcsfontosságú kérdés. 2013-ban Cho és munkatársai publikálták az első dózis eszkalációs vizsgálatot, amely az ASC-kezelés hatékonyságának és biztonságosságának értékelését tűzte ki célul a dózistól függően. A 10 bevont beteget 3 terápiás csoportba sorolták, amelyben 10, 20 vagy 40×106/ml ASC lokális beadására került sor, és bizonyították, hogy mindhárom dózis egyformán biztonságosan alkalmazható, de komplett fisztulazáródás csak magas sejtkoncentráció esetén volt elérhető (39). Azonos eredményre jutottak 2016-ban Park és munkatársai is, akik 10 és 30×106/ml ASC-dózist alkalmazva nem észleltek súlyos adverz eseméyt, ugyanakkor a hatékonyság tekintetében szignifikánsan magasabb sipolyzáródási arányt értéke el a magasabb sejtkoncentráció alkalmazásával (40). A csontvelői eredetű MSC alkalmazásakor a 30×106/ml sejtszám alkalmazásával, a placebóval összevetve szignifikánsan magasabb volt a sipolyzáródási arány, de ez a különbséget nem észlelték a magasabb (90×106/ml) és alacsonyabb (10×106/ml) dózisok esetén (41). Mivel a magas sejtkoncentráció alkalmazásakor a bejuttatott őssejtek élettartama és/vagy biológiai funkciója alacsonyabb volt, a szerzők arra a következtetésre jutottak, hogy a háttérben az MSC-sejtekkel szembeni immuntolerancia elvesztése állhat, amely a sejtek inaktivációjához és gyorsult clearance-hez vezet (42).
A korai vizsgálatok hátránya, hogy döntő többségükben prospektív módon a kezelés rövidtávú hatékonyságát értékelték, kevesebb, mint 24 hetet a beadást követően, és a hosszú távú, 6 hónapot meghaladó eredményességre vonatkozóan elsősorban retrospektív elemzések állnak rendelkezésre a korábban kezelt betegek klinikai adatainak elemzésével. Guadalajara és munkatársai nem észleltek adverz eseményt a korábban már említett randomizált II. fázis klinikai vizsgálatukban szereplő beteg közel 4 éves utánkövetése során (43). Cho és munkatársai igazolták, hogy a sipolyzáródás az esetek 83%-ában tartós (44). Ciccocioppo és munkatársai retrospektív értékelése alapján fisztula relapszusmentes túlélés az MSC-kezelés után 88% és 100% az első év végén, 50% és 75% a második év során, míg 37% és 63% a 4 éves utánkövetés végén (45).
A jelenleg elérhető, legnagyobb esetszámú, multicentrikus, kettős vak placebokontrollált klinikai vizsgálatban 3 sipoly kezelésénél összesen 120×106 allogén ASC transzplantációjára került a bevont 49 európai vagy izraeli kórház egyikében. Az elsődleges végpont a sipolyzáródás aránya volt, amelynek elérését fizikális vizsgálattal és MRI-vizsgálattal együttesen kellett megerősíteni. Mindkét csoportban a beteg báziskezelését, amely a biológiai terápiát is magában foglalta, változatlan dózisban folytatták. A placebocsoportban a sebészi beavatkozás során a fisztulajártok tisztítására került csak sor, és környezetét sóoldattal infiltrálták, míg a terápiás csoportban a fent említett sejtdózist juttatták be elosztva a belső szájadék és a fisztulacsatorna környezetében a fisztula „felfrissítése” után. A belső szájadékot felszívódó öltéssel zárták. Szignifikáns különbséget észleltek a terápiás és placebocsoport között a komplett remisszió tekintetében a 24. héten az intent-to-treat (ITT) populációban (51% vs. 36%), és ez az érték érdemi csökkenést nem mutatott az egyéves utánkövetés során (56,3% vs. 38,6%) (46).
Az MSC-kezelés biztonságossága
Az MSC-kezeléssel kapcsolatban egyetlen tanulmány sem számolt be súlyos adverz eseményről. A randomizált vizsgálatok metaanalízise nem talált összefüggést a komplikációk (láz, lokális infekció, tályogképződés, malignitás stb.) és az őssejtkezelés között, azaz a tapasztalt, döntően enyhe tünetek gyakoriságában nem mutatkozott eltérést a kontrollcsoport és a terápiás csoportok között (47). A teoretikusan felvetett emelkedett malignus transzformációs kockázat ellenére, az eddig publikált tanulmányokba bevont betegek egyikénél sem jelentkezett daganat (48, 49).
MSC magyarországi alkalmazása
Magyarországon a zsírszöveti eredetű allogén MSC-kezelésre előállított darvadastrocel készítményt Alofisel néven törzskönyvezték. A készítmény finanszírozására vonatkozóan jelenleg még zajlanak a tárgyalások. A szakmai kollégium azon betegek esetében javasolja a kezelést, akinél
- igazolható a biológiai terápiával elért, 3 hónapon belüli ileokolonoszkópiával alátámasztott luminális remisszió, fekélymentesség (SES CD <3) ellenére perzisztálnak az aktivitást mutató, MRI-vel dokumentált komplex fisztulák, de
- ezek legfeljebb 2 belső és/vagy maximum 3 külső fisztula nyílással rendelkeznek, és
- az esetleges társuló tályog sebészeti szanálása megtörtént.
Az őssejtterápia az adott kezelés kiegészítéseként, legalább 6 hónapja megkezdett biológiai kezelést követően alkalmazható az érintett betegeknél egy alkalommal. Ismételt kezelésre vonatkozó vizsgálatok, tapasztalatok jelenleg nem állnak rendelkezésre, de Pan és munkatársai prospektív vizsgálata azt sugallja, hogy a terápia egy éven belüli ismétlésére nincs szükség. A kezelés egyedi engedélyezéshez kötött, kérvény beadását követően alkalmazható az arra dedikált egészségügyi intézményekben.
Következtetések
A prospektív klinikai vizsgálatok igazolták, hogy az MSC-transzplantáció eredményes és biztonságosan alkalmazható kiegészítő eljárás a konzervatív kezelésre rezisztens perianalis fisztulázó CD-kezelésében a biológiai terápia mellett. Szemben a biológiai kezelésekkel, az MSC-kezelés direkt módon támogatja a szöveti regenerációt és hatása nem csökken a hosszú távú utánkövetés alapján. Hátránya azonban, hogy bevitele invazív, a perianalis kisműtét során a sejtek infiltrációja mellett szükséges a fisztulajáratok megfelelő tisztítása, felfrissítése. A többi perianalis műtéttel összevetve azonban minimális invazivitása miatt nem növeli az analis sphincter sérülésének kockázatát.
Az autológ és allogén MSC-transzplantáció, illetve az eltérő forrásból származó őssejtek (zsírszöveti, csontvelői) között a hatékonyság és biztonságosság tekintetében nem találtak különbséget. Az autológ transzplantáció komplikáltabb eljárás és nagyobb megterhelést jelent a beteg számára, ugyanakkor a sejtek immunkompatibilitása optimális. Itt a beteg első lépésben csontvelő-aspiráción vagy zsírleszíváson esik át. Az eltávolított mintából izolálják az MSC-sejteket, majd több hetes expanziós időszak következik a kívánt sejtszám eléréséig. Ez azon túlmenően, hogy időigényes, igen költséges eljárás is, és nem bizonyult hatékonyabbnak az allogén kezeléssel összevetve. Az optimális MSC-kezelési út ezért úgy tűnik az allogén transzplantáció lesz, mivel lehetőséget biztosít standardizált sejtszámmal rendelkező készítmények előállítására, amely később a kívánt időpontban használható fel.
A korai klinikai vizsgálatok adatait elemző metaanalízis igazolta, hogy a közepes, 20-40×106 MSC/ml sejtkoncentráció eredményezte a legmagasabb fisztulazáródási arányt (80,07%) és legalacsonyabb rekurrenciát (13,98%) (42). Ennek megfelelően a legnagyobb esetszámú vizsgálat 120×106 MSC/ml dózist alkalmaz, amely 3 sipolyjárat egyidejű kezelésére elegendő (46). Ez a tanulmány azonban rávilágított arra, hogy a fisztulák adekvát tisztítása, felfrissítése önmagában elősegítheti a gyógyulást, amit a placebokaron a 24. héten tapasztalt 36%-os komplett sipolyzáródási ráta bizonyít. Bár egy betegnél sem tapasztaltak daganatot az utánkövetés során, a teoretikus kockázat ellenére javasolt figyelmet szentelni a beteg kórelőzményének és társbetegségeinek a kezelés indikációjának felállítása előtt. Súlyos adverz eseményt egy esetben sem észleltek a tanulmányok, az észlelt komplikációk döntően lokális reakciók voltak, amelyek szignifikáns különbséget nem mutattak a terápiás és placebocsoportok között.
2. Van Assche G, et al. “The second European evidence-based Consensus on the diagnosis and management of Crohn’s disease: Special situations.” J Crohns Colitis 2010 May; 4(1): 63–101. https://doi.org/10.1016/j.crohns.2009.09.009
3. Tang LY, Rawsthorne P, Bernstein CN. “Are perineal and luminal fistulas associated in Crohn’s disease? A population-based study.” Clin Gastroenterol Hepatol 2006; 4(9): 1130–4. https://doi.org/10.1016/j.cgh.2006.06.021
4. Peyrin-Biroulet L, Loftus EV, Colombe J-F, Sandborn WJ. “The natural history of adult Crohn’s disease in population-based cohorts.” Am J Gastroenterol 2010 Feb; 105(2): 289–97. https://doi.org/10.1038/ajg.2009.579
5. Baumgart DC, Sandborn WJ. “Crohn’s disease.” Lancet 2012 Nov; 380(9853): 1590–1605. https://doi.org/10.1016/s0140-6736(12)60026-9
6. Hanauer SB, et al. “Maintenance infliximab for Crohn’s disease: the ACCENT I randomised trial.” Lancet 2002; 359(9317): 1541–1549. https://doi.org/10.1016/s0140-6736(02)08512-4
7. Colombel J-F, et al. “Adalimumab for maintenance of clinical response and remission in patients with Crohn’s disease: the CHARM trial.” Gastroenterology 2007 Jan; 132(1): 52–65. https://doi.org/10.1053/j.gastro.2006.11.041
8. Molnár T, Farkas K, Nyári T, Szepes Z, Nagy F, Wittmann T. “Frequency and predictors of loss of response to infliximab or adalimumab in Crohn’s disease after one-year treatment period – a single center experience.” J Gastrointestin Liver Dis 2012 Sep; 21(3): 265–9.
9. Bouguen G, et al. “Long-term Outcome of Perianal Fistulizing Crohn’s Disease Treated With Infliximab.” Clin Gastroenterol Hepatol 2013 Jan. https://doi.org/10.3410/f.718052623.793485258
10. Sands BE, et al. “Infliximab maintenance therapy for fistulizing Crohn’s disease.” N Engl J Med 2004 Feb; 350(9): 876–85. https://doi.org/10.1056/nejmoa030815
11. Feagan BG, et al. “Vedolizumab as Induction and Maintenance Therapy for Ulcerative Colitis.” N Engl J Med 2013 Aug; 369(8): 699–710. https://doi.org/10.1056/nejmoa1215734
12. Dothel D, Raschi E, Rimondini R, De Ponti F. “Mesenchymal stromal cell-based therapy: Regulatory and translational aspects in gastroenterology.” World J Gastroenterol 2016 Nov; 22(41): 9057–9068. https://doi.org/10.3748/wjg.v22.i41.9057
13. Friedenstein AJ, Chailakhyan RK, Latsinik NV, Panasyuk A, Keiliss-Borok IV. “Stromal cells responsible for transferring the microenvironment of the hemopoietic tissues. Cloning in vitro and retransplantation in vivo.” Transplantation 1974 Apr; 17(4): 331–40. https://doi.org/10.1097/00007890-197404000-00001
14. Friedenstein AJ, Chailakhjan RK, Lalykina KS. “The development of fibroblast colonies in monolayer cultures of guinea-pig bone marrow and spleen cells.” Cell Tissue Kinet 1970 Oct; 3(4): 393–403. https://doi.org/10.1111/j.1365-2184.1970.tb00347.x
15. De Francesco F, et al. “The role of adipose stem cells in inflammatory bowel disease: From biology to novel therapeutic strategies.” Cancer Biol Ther 2016 Sep; 17(9): 889–98. https://doi.org/10.1080/15384047.2016.1210741
16. Deans RJ, Moseley AB. “Mesenchymal stem cells: biology and potential clinical uses.” Exp Hematol 2000 Aug; 28(8): 875–84. https://doi.org/10.1016/s0301-472x(00)00482-3
17. Mao F, et al. “Mesenchymal stem cells and their therapeutic applications in inflammatory bowel disease.” Oncotarget 2017 Jun; 8(23): 38008–38021. https://doi.org/10.18632/oncotarget.16682
18. Dominici M, et al. “Minimal criteria for defining multipotent mesenchymal stromal cells. The International Society for Cellular Therapy position statement.” Cytotherapy 2006; 8(4): 315–7. https://doi.org/10.1080/14653240600855905
19. Mo M, Wang S, Zhou Y, Li H, Wu Y. “Mesenchymal stem cell subpopulations: phenotype, property and therapeutic potential.” Cell Mol Life Sci 2016 Sep; 73(17): 3311–21. https://doi.org/10.1007/s00018-016-2229-7
20. Tsuchiya A, et al. “Clinical trials using mesenchymal stem cells in liver diseases and inflammatory bowel diseases.” Inflamm Regen 2017 Dec; 37(1): 16. https://doi.org/10.1186/s41232-017-0045-6
21. Klyushnenkova E, et al. “T cell responses to allogeneic human mesenchymal stem cells: immunogenicity, tolerance, and suppression.” J Biomed Sci 2005 Jan; 12(1): 47–57. https://doi.org/10.1007/s11373-004-8183-7
22. Le Blanc K, Tammik C, Rosendahl K, Zetterberg E, Ringdén O. “HLA expression and immunologic properties of differentiated and undifferentiated mesenchymal stem cells.” Exp Hematol 2003 Oct; 31(10): 890–6. https://doi.org/10.1016/s0301-472x(03)00110-3
23. Zangi L, et al. “Direct imaging of immune rejection and memory induction by allogeneic mesenchymal stromal cells.” Stem Cells 2009 Nov; 27(11): 2865–74. https://doi.org/10.1002/stem.217
24. Zundler S, Neurath MF. “Immunopathogenesis of inflammatory bowel diseases: functional role of T cells and T cell homing.” Clin Exp Rheumatol 33(4 Suppl 92): S19–28. https://doi.org/10.1097/00054725-200002000-00004
25. Stefanelli T, Malesci A, Repici A, Vetrano S, Danese S. “New insights into inflammatory bowel disease pathophysiology: paving the way for novel therapeutic targets.” Curr Drug Targets 2008 May; 9(5): 413–8. https://doi.org/10.2174/138945008784221170
26. Becker F, Yi P, Al-Kofahi M, Ganta VC, Morris J, Alexander JS. “Lymphatic dysregulation in intestinal inflammation: new insights into inflammatory bowel disease pathomechanisms.” Lymphology 2014 Mar; 47(1): 3–27. https://doi.org/10.5772/65380
27. He X-W, He X-S, Lian L, Wu X-J, Lan P. “Systemic Infusion of Bone Marrow-Derived Mesenchymal Stem Cells for Treatment of Experimental Colitis in Mice.” Dig Dis Sci 2012 Dec; 57(12): 3136–3144. https://doi.org/10.1007/s10620-012-2290-5
28. González MA, Gonzalez-Rey E, Rico L, Büscher D, Delgado M. “Adipose-derived mesenchymal stem cells alleviate experimental colitis by inhibiting inflammatory and autoimmune responses.” Gastroenterology 2009 Mar; 136(3): 978–89. https://doi.org/10.1053/j.gastro.2008.11.041
29. Ren G, et al. “Mesenchymal stem cell-mediated immunosuppression occurs via concerted action of chemokines and nitric oxide.” Cell Stem Cell 2008 Feb; 2(2): 141–50. https://doi.org/10.1016/j.stem.2007.11.014
30. Shi Y, Su J, Roberts AI, Shou P, Rabson AB, Ren G. “How mesenchymal stem cells interact with tissue immune responses.” Trends Immunol 2012 Mar; 33(3): 136–143. https://doi.org/10.1016/j.it.2011.11.004
31. Hawkey CJ, Hommes DW. “Is Stem Cell Therapy Ready for Prime Time in Treatment of Inflammatory Bowel Diseases?” Gastroenterology 2017 Jan; 152(2): 389–397.e2. https://doi.org/10.1053/j.gastro.2016.11.003
32. García-Olmo D, et al. “Autologous stem cell transplantation for treatment of rectovaginal fistula in perianal Crohn’s disease: a new cell-based therapy.” Int J Colorectal Dis 2003 Sep; 18(5): 451–4. https://doi.org/10.1007/s00384-003-0490-3
33. García-Olmo D, García-Arranz M, Herreros D, Pascual I, Peiro C, Rodríguez-Montes JA. “A Phase I Clinical Trial of the Treatment of Crohn’s Fistula by Adipose Mesenchymal Stem Cell Transplantation.” Dis Colon Rectum 2005 Jul; 48(7): 1416–1423. https://doi.org/10.1007/s10350-005-0052-6
34. Garcia-Olmo D, et al. “Expanded Adipose-Derived Stem Cells for the Treatment of Complex Perianal Fistula.” Dis Colon Rectum 2009 Jan; 52(1): 79–86.
35. Ciccocioppo R, et al. “Autologous bone marrow-derived mesenchymal stromal cells in the treatment of fistulising Crohn’s disease.” Gut 2011 Jun; 60(6): 788–798. https://doi.org/10.1007/dcr.0b013e3181973487
36. de la Portilla F, Alba F, García-Olmo D, Herrerías JM, González FX, Galindo A. “Expanded allogeneic adipose-derived stem cells (eASCs) for the treatment of complex perianal fistula in Crohn’s disease: results from a multicenter phase I/IIa clinical trial.” Int J Colorectal Dis 2013 Mar; 28(3): 313–23. https://doi.org/10.1007/s00384-012-1581-9
37. Dietz AB, et al. “Autologous Mesenchymal Stem Cells, Applied in a Bioabsorbable Matrix, for Treatment of Perianal Fistulas in Patients With Crohn’s Disease.” Gastroenterology 2017 Jul; 153(1): 59–62.e2. https://doi.org/10.1053/j.gastro.2017.04.001
38. Lee WY, et al. “Autologous adipose tissue-derived stem cells treatment demonstrated favorable and sustainable therapeutic effect for Crohn’s fistula.” Stem Cells 2013 Nov; 31(11): 2575–81. https://doi.org/10.1002/stem.1357
39. Cho YB, Lee WY, Park KJ, Kim M, Yoo H-W, Yu CS. “Autologous Adipose Tissue-Derived Stem Cells for the Treatment of Crohn’s Fistula: A Phase I Clinical Study.” Cell Transplant 2013 Feb; 22(2): 279–285. https://doi.org/10.3727/096368912×656045
40. Park KJ, et al. “Allogeneic adipose-derived stem cells for the treatment of perianal fistula in Crohn’s disease: a pilot clinical trial.” Colorectal Dis 2016 May; 8(5): 468–76. https://doi.org/10.3727/096368912×656045
41. Molendijk I, et al, “Allogeneic Bone Marrow-Derived Mesenchymal Stromal Cells Promote Healing of Refractory Perianal Fistulas in Patients With Crohn’s Disease.” Gastroenterology 2015 Oct; 149(4): 918–27. e6. https://doi.org/10.1053/j.gastro.2015.06.014
42. Cao Y, Ding Z, Han C, Shi H, Cui L, Lin R. “Efficacy of Mesenchymal Stromal Cells for Fistula Treatment of Crohn’s Disease: A Systematic Review and Meta-Analysis.” Dig Dis Sci 2017 Apr; 62(4): 851–860. https://doi.org/10.1007/s10620-017-4453-x
43. Guadalajara H, Herreros D, De-La-Quintana P, Trebol J, Garcia-Arranz M, Garcia-Olmo D. “Long-term follow-up of patients undergoing adipose-derived adult stem cell administration to treat complex perianal fistulas.” Int J Colorectal Dis 2012 May; 27(5): 595–600.
44. Cho YB, et al. “Long-Term Results of Adipose-Derived Stem Cell Therapy for the Treatment of Crohn’s Fistula.” Stem Cells Transl Med 2015 May; 4(5): 532–537.
45. Ciccocioppo R, Gallia A, Sgarella A, Kruzliak P, Gobbi PG, Corazza GR. “Long-Term Follow-Up of Crohn Disease Fistulas After Local Injections of Bone Marrow-Derived Mesenchymal Stem Cells.” Mayo Clin Proc 2015 Jun; 90(6): 747–55.
46. Panés J, et al. “Expanded allogeneic adipose-derived mesenchymal stem cells (Cx601) for complex perianal fistulas in Crohn’s disease: a phase 3 randomised, double-blind controlled trial.” Lancet (London, England) 2016 Sep; 388(10051): 1281–90.
47. Lalu MM, et al. “Safety of cell therapy with mesenchymal stromal cells (SafeCell): a systematic review and meta-analysis of clinical trials.” PLoS One 2012 Oct; 7(10): e47559.
48. Prockop DJ, et al. “Defining the risks of mesenchymal stromal cell therapy.” Cytotherapy 2010 Sep; 12(5): 576–578.
49. Dhere T, et al. “The safety of autologous and metabolically fit bone marrow mesenchymal stromal cells in medically refractory Crohn’s disease – a phase 1 trial with three doses.” Aliment Pharmacol Ther 2016 Sep; 44(5): 471–481.
