Összefoglaló közlemények / Review
Molecular links between the oncobiome and pancreatic adenocarcinoma
Summary
Adenocarcinoma of the pancreas is one of the tumors with the highest mortality. Its’ median five year survival is only 7-8%. Pancreatic adenocarcinoma is often advanced upon diagnosis, thus its early detection is an unmet medical need. Microbiome dysbiosis, termed oncobiosis can often be revealed in malignancies, likewise in pancreatic adenocarcinoma, where the oral, duodenal, ductal, and fecal microbiome converts to dysbiotic. Colonization by Helicobacter pylori and Malassezia, among others in the dysbiotic pancreas can be frequently observed. The pancreatic adenocarcinoma oncobiomes differ in long and short-term survivors. Survival is extended in pancreatic adenocarcinoma animal models when long-survivor oncobiomes were transplanted. In pancreatic adenocarcinoma, the inflammation plays an important role in carcinogenesis. Pancreatic oncobiome is shown to modulate the inflammatory cascades behind cancerization. This review is a brief summary of the studies about the oncobiotic processes in the pathogenesis of pancreatic adenocarcinoma. Changes in the metabolome during the neoplastic process are also mentioned along with some important types of bacterial metabolites (e.g. short chain fatty acids, secondary bile acids, polyamines, indole-derivatives). More diagnostically and therapeutically relevant metabolites and metabolic pathways are to be revealed in the near future.
A hasnyálmirigy-adenocarcinoma az egyik legmagasabb halálozású daganat, medián ötéves túlélése 7-8%, korai diagnosztikája, eredményes kezelése kihívást jelent. A daganatos betegségekhez, így a pancreasrákhoz is gyakran társul a mikrobiom összetételének megváltozása (dysbiosis), amelyet onkobiózisnak nevezünk. Maga a pancreas is gyakran kolonizálódik (pl. többek között Helicobacter pylorival és Malassezia-fajokkal). Az onkobiomok összetétele eltér a rövid és hosszú túlélők esetén. Amennyiben pancreas-adenocarcinomás hosszú túlélők mikrobiomját ültetik hasnyálmirigy-adenocarcinoma állatmodellbe, az egerek túlélése meghosszabbodik. Az onkobiom modulálja a daganatos elfajuláshoz vezető gyulladásos folyamatot pancreas-adenocarcinomában. Az összefoglalóban a bakteriális metabolitok (rövid láncú zsírsavak, másodlagos epesavak, poliaminok, indolszármazékok) szerepét mutatjuk be a pancreas-adenocarcinoma patogenezisében, kitérve arra, hogy a betegségben a bakteriális metabolizmus és a bakteriális metabolom szabályozása is felborul. További metabolitok és anyagcsere-útvonalak felfedezése várható a közeljövőben, tovább bővítve ezen patogenetikai útvonal nyújtotta diagnosztikus és terápiás lehetőségeket hasnyálmirigy-adenocarcinomában.
1. Pancreas-adenocarcinoma, a terápiás kihívás
A pancreas-adenocarcinoma (PA) főként a ductusokból ered, gyakrabban a pancreasfejben alakul ki. Halálozási rátája mindkét nemben a legmagasabb (1), előfordulási gyakorisága emelkedik (2). A PA ötéves túlélése körülbelül 7-8%. Mivel a daganat tünetmentesen progrediál a helyileg előrehaladott és metasztatikus stádiumba, gyakran későn születik diagnózis, a kuratív sebészi reszekciót a betegek 15-25 százalékában lehet elvégezni, a szisztémás kezelés is kevésbé eredményes az előrehaladott esetekben (1). A PA mind diagnosztikai, mind terápiás szempontból kihívást („unmet medical need”) jelent.
A kuratív sebészi eltávolításra nem alkalmas esetekben szisztémás kemoterápiát alkalmazhatunk monoterápia vagy kombinált kezelés formájában (3). Új ígéretes terápiás szerekkel – pl. PARP- (poli[ADP-ribóz] polimeráz) inhibitorokkal – folynak kísérletek (4). A szisztémás kemoterápia radioterápiával való kiegészítéséről kevés olyan bizonyíték áll rendelkezésre, amely alkalmazását támogatná. A PA kezelésének multidiszciplináris szemléletben kell megvalósulnia (5).
A PA környezeti rizikófaktorai közé tartozik a dohányzás, az alkoholizmus, a krónikus vagy visszatérő pancreatitis, az elhízás és a diabetes mellitus (6). A PA-hoz társuló genetikai mutációkat is kimutattak (7). A PA esetek 80 százalékában KRAS-mutációkat találtak (8). Közelmúltbeli kutatások egyéb, PA-hoz köthető mutációkat azonosítottak, beleértve a BRCA1 (breast cancer type 1 susceptibility gén), TP53 (p53 tumorszuppresszor gén), és számos egyéb DNS-hibajavításban szerepet játszó enzimek génjeiben (7).
2. A mikrobiom onkobiotikus transzformációja
Daganatos betegségekben a mikrobiom sajátos módon megváltozik, amelyet onkobiomnak nevezünk (9). Ismereteink szerint az onkobiomnak patogenetikai szerepe van a daganat kialakulásában. A gazdaszervezet és a mikrobiom között bonyolult, nem teljesen feltárt kölcsönhatás alakul ki: a gazdaszervezet magatartásával, táplálkozásával, immunrendszerével befolyásolhatja a mikrobiom összetételét, tömegét; a mikrobiom metabolitokat termel, jelenléte aktiválhatja az immunrendszert, visszahat a gazdaszervezetre (10).
Hanahan és Weinberg (11, 12) megalkotta a „cancer hallmark” („ daganat védjegy”) kifejezést, amely mindazon biológiai folyamatok összességét jelenti, amely elindítja a daganatos elfajulást, és elősegíti a daganatos sejtek megállíthatatlan szaporodását. Az onkobiom közvetlen vagy érintőleges szerepet játszik minden „cancer hallmark” szabályzásában. Az onkobiom fokozza a genominstabilitást és -mutációkat, a sejtek energetikai rendszerének szabályozási zavarát, a tumorigén gyulladás kialakulását, az immundestrukció elkerülését, a tumorsejtek mozgását, invázióját, a metasztázisképződést, elősegíti az érújdonképződést (10).
A hosszan fennálló gyulladás az oxidatív stressz révén DNS-károsodáshoz és genominstabilitáshoz vezet. A mutációk halmozódása növeli a daganatos átalakulás rizikóját (13–15). A diszbiotikus mikrobiom hatására helyi gyulladások alakulhatnak ki, ez PA esetén a karcinogenezis előmozdítója (16–20). Az oxidatív stressz fokozódása viszont citosztatikus is lehet bizonyos neopláziákban, így pl. emlőrákban (15, 21). Az onkobiózis okozta oxidatív stressz hozzájárulhat a daganatos betegségek iniciációjához, de később citosztatikus hatása is lehet.
Az onkobiom immunológiai tulajdonságai különböznek a normál mikrobiométól (eubiom); az onkobiózis megváltoztatja az immunrendszert (22). Az immunrendszer tolerogén viselkedése meggátolja a daganatsejtek korai eliminációját (22). Immunogénebb mikrobiom mellett hatásosabb lehet az immunterápia/célzott kezelés (23), azonban a tartós, erős gyulladás fokozhatja a karcinogenezist (16–20, 24). A baktériumok fizikai jelenléte kulcsfontosságú a folyamatban, az immunmoduláns hatású bakteriális metabolitok szintén lényegesek (25).
Az onkobiotikus transzformáció elősegíti a daganatsejtek proliferációját, invázióját és a metasztázisképződést (10, 15). Az onkobiózis megváltoztatja a vascularis endothelialis növekedési faktor (VEGF) expresszióját, befolyásolja a tumorvaszkularizációt (25). Ezek az onkobiózis és onkobiotikus bakteriális metabolitok által befolyásolt legfontosabb folyamatok.
A bakteriális metabolitok hatnak a daganatsejtek redox egyensúlyára és metabolizmusára (21, 25). Egyensúlyi helyzetben cytostasis alakul ki, amely az epithelialis-mesenchymalis átmenet újraprogramozásával csökkenti a daganatos őssejtképződést (10). Ezen lépések befolyásolják daganatsejt-növekedést, -vándorlást és az áttétképződést (10).
Az onkobiózis okai között az életmódbeli tényezők, a dohányzás, az étrend, az elhízás, a diurnális ritmus megváltozása, az öregedés, a 2-es típusú diabétesz vagy a testmozgás hiánya kiemelkedőek. Ezen tényezők némelyike a pancreas-adenocarcinoma önálló rizikófaktora is. Más daganatokban az antibiotikum- és probiotikumhasználat szintén összefügg a karcinogenezissel (26).
3. Onkobiom pancreas-adenocarcinomában
1. táblázat: A humán onkobiom vizsgálatának főbb eredményei pancreas-adenocarcinomában
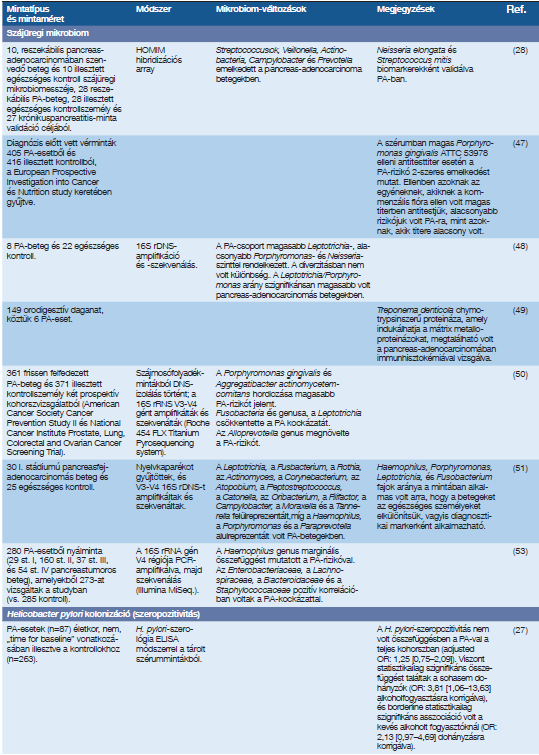
1. táblázat folytatása
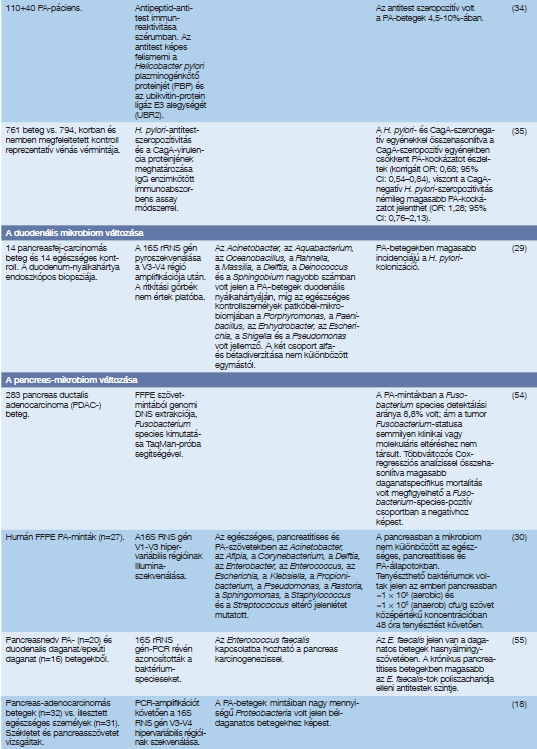
1. táblázat folytatása
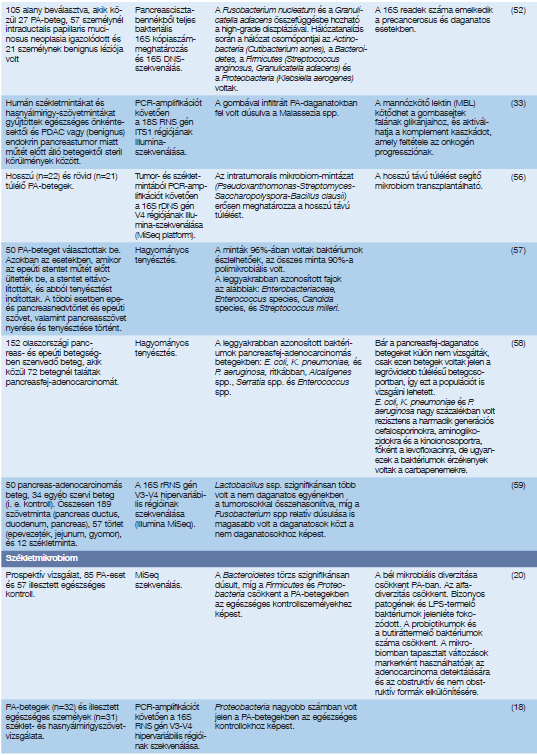
1. táblázat folytatása

A mikrobiom és a PA közötti kapcsolat ötlete először akkor merült fel, amikor felfedezték, hogy a Helicobacter pylori-kolonizáció pancreatitishez társul (27). Azóta több hasonló összefüggést mutattak ki a szájüreg (28), a bélrendszer (29), a pancreas (18, 30, 31) és a széklet (20,32) mikrobiomja, a mycobiom (33) és a PA között.
Jelenlegi ismereteink szerint a szájüregi-, gyomor- és bélmikrobiom alkotórészei gyulladást kelthetnek. A gyulladás a karcinogenezis rizikófaktora a pancreasban. Az állat- és humán kísérletsorozatok alapján a szájüregi, a gasztrikus és a duodenális flóra kolonizálhatja az epevezetéket, a ductus pancreaticust és a pancreast (16, 29, 31, 34–45). PA-ban jellegzetesen megváltozik a szájüregi (28, 46–53) és a duodenális mikrobiom (29). Az epeutak kolonizációja Enterobacter, Enterococcus, E. coli fajokkal (43) vagy a pancreas kolonizációja (18, 30, 33, 54–59) kockázati tényezők PA szempontjából. A hepatotróp vírusok (Hepatitis B, C; transzfúzióval átvitt torque teno vírus) PA-ban játszott onkogén szerepét klinikai körülmények között megfigyelték, bár a pontos molekuláris mechanizmusok jelenleg még ismeretlenek (43).
A mycobiom onkogén szerepet játszik a PA-ban. Egérmodellben megfigyelték, hogy a gombák a bél lumenéből a pancreasba képesek vándorolni. Pancreas-szövetmintákat vizsgálva megállapították, hogy a PA-mintákban 3000-szer több gomba van jelen, mint nem tumoros hasnyálmirigyszövetben. A PA-mintákban a gombák faji összetétele is eltér; kiemelkedő a Malasseziák magas száma. A Malassezia fajok praoteoglikán falához kötődő mannózkötő lektin (MBL) aktiválja a komplement kaszkádot, a létrejövő gyulladás pedig elősegíti a daganatos elfajulást (33).
Kras-mutáns (Tp53) egérmodellben a táplálék-mikrobiom be tud jutni a hasnyálmirigybe (18). A pancreas elleni bakteriális invázió patogenetikai szerepét alátámasztja a PA-incidencia csökkenése gnotobiotikus (ismert mikrobiom-összetételű) és antibiotikumkezelt egerekben (30).
Egy ausztrál kutatócsoport pancreatoduodenectomián átesett PA-betegek perioperatív antibiotikumprofilaxisát vizsgálta. A kis esetszámon végzett tanulmányban számos baktérium kolonizációját tudták kimutatni a műtéti területen és a korábban behelyezett epeúti stentekből, főként Enterobacter, Enterococcus, és Candida specieseket. Eredményeik alapján 5 napig tartó kombinált antibiotikus és antimikotikus (amoxicillin/klavulánsav + aminoglikozid + fluorokinolon) profilaxist javasoltak, ám a kis betegszám miatt az egyes fajok és a műtéti infekciók, valamint a túlélés vonatkozásában következtetést levonni nem tudtak (57). Az egyes antibiotikumok szerepe eltérő lehet. Humán adatbázis adatainak elemzése alapján a rekurrens penicillin alkalmazása megnövelte a PA kockázatát (60). Más antibiotikumok, kombinációk (streptomycin, gentamicin, bacitracin és ciprofloxacin [30], ampicillin, vancomycin, neomycin és metronidazol [61]) védő hatásúak voltak egérmodellekben (62). A székletmikrobiom-transzplantáció tovább módosítja a betegségre való fogékonyságot (18, 56).
A PA-onkobiomra vonatkozó főbb megállapításokat az 1. táblázatban foglaltuk össze. Nincs egyetértés abban, hogy a mikrobiom diverzitása hogyan változik PA-ban. Az alfa-diverzitás (Shannon-index) a nyelvmikrobiomban növekszik (51). A nyálmikrobiom alfa-diverzitása nem változik, a béta-diverzitás PA-betegek és kontrollok között eltérő volt (53). A PA-betegek duodenumában alacsonyabb alfa-index (OTU diverzitás) felé mutató tendenciát figyeltek meg (29). A PA-betegek és kontrollok mikrobiomjának alfa-diverzitása (Chao1, Shannon) különbözött, de a változás nem volt konzekvens (18, 52, 30). A hasnyálmirigy-mycobiom alfa-diverzitása (OTU, Shannon) csökkent PA esetén (33). A hosszú túlélők alfa-diverzitás-indexe magasabb a rövid túlélőkénél (56). A székletmikrobiom alfa-diverzitása a PA-betegekben két vizsgálatban is alacsonyabb (20, 59).
Néhány baktériumfaj erősen asszociálható PA-hoz. A szájüregi mikrobiomban található Porphyromonas gingivalis (29, 47, 48, 50, 63), Helicobacter pylori (27, 34, 35), Enterobacter, Enterococcus (29, 55, 57, 58), Fusobacteria (54, 59, 64), E. coli (29, 58) állománya növekszik PA-betegekben. Egy, ezernél is több betegben intratumoralis DNS-t és a szérumban található szabad DNS-t vizsgáló klinikai vizsgálatban a tumorokban magasabb számú Fusobacteriumot észleltek az egészséges szövetekhez képest (64). Gombafajok (pl. Malassezia) szintén magasabb arányban észlelhetőek betegekben (33). A nyálmikrobiom összetétele megváltozik pancreas-adenocarcinomában, jellegzetes bakteriális mintázatok alakulnak ki (pl. Neisseria elongata és Streptococcus mitis), bizonyos baktériumcsoportok dúsulása és mások eltűnése a későbbiekben diagnosztikai eszköz lehet (28). Különböző PA-rizikótényezők a mikrobiom megváltozásával járnak, mint a dohányzás, a rossz szájhigiéné vagy a fogak elvesztése (43), valamint a visszatérő pancreatitis. A pancreatitisben észlelt baktériummennyiség kevesebb, mint PA-ban.
A hasnyálmirigy bakteriális inváziója leginkább tartós gyulladást idéz elő. A természetes és az adaptív immunitás részt vesz a baktériumok felismerésében és a gyulladásos reakció levezényelésében (16, 17). A Th1, a Th2 és a Th17 válaszokat egyaránt kimutatták (18, 19). PA-ban a lipopoliszacharid- (LPS-) termelő baktériumok (pl. Prevotella, Hallella és Enterobacter [20]) aránya emelkedik. Az LPS kötődhet toll-like receptorokhoz; TLR2-höz, TLR4-hez és TLR9-hez PA-ban (65). A TLR-aktiváció beindítja a tumorigén STAT3 és NF-κB útvonalakat, amelyek serkentik a sejtproliferációt, és gátolják az apoptosist (16).
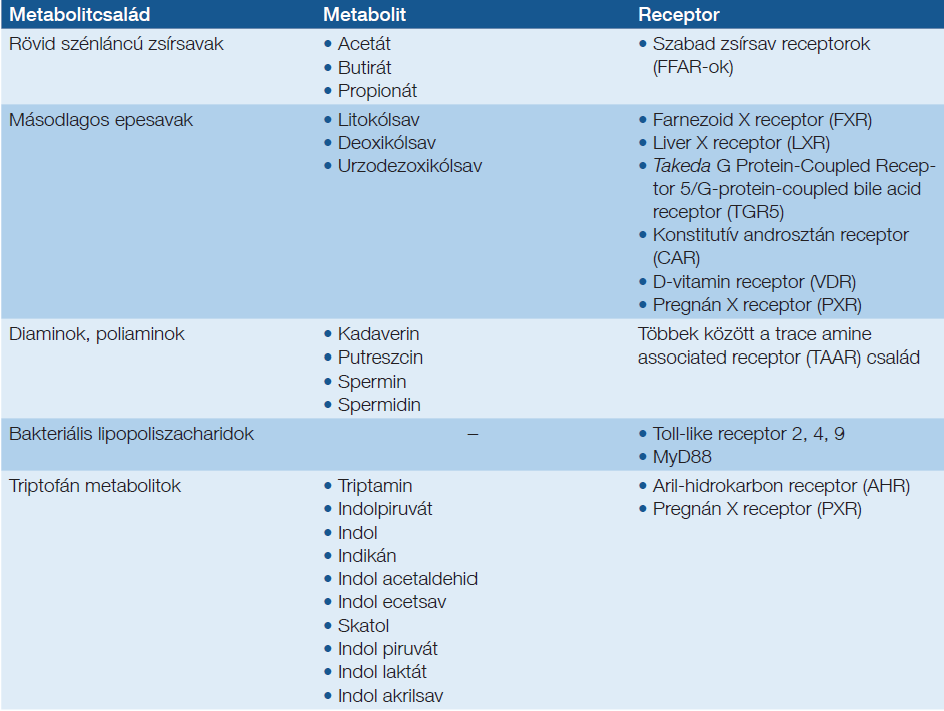
A mikrobiom direkt immunogenitása mellett endokrinszerű funkcióját is leírták daganatokban (26, 66–68), így PA-ban is. A baktériumok által termelt bakteriális metabolitok bejutnak a szisztémás keringésbe, és távoli daganatsejteken fejtik ki a hatásukat (26, 69, 70). Az onkobiom anyagcseréje jelentősen megváltozik PA-ban (20), és a szekretált bakteriális metabolitok mennyisége, a szekretom összetétele is átalakul. Több bakteriális metabolit szekréciója és receptorokon keresztüli jelátvitele megváltozik PA-ban, ezt részletesen az alábbi összefoglaló közlemény (71), illetve a 2. táblázat tárgyalja.
4. Klinikai döntéstámogatás, diagnosztikus felhasználás
A szájüregi (28, 47, 51, 53, 73), bél- (20), hasnyálmirigy- (64) és széklet- (72) onkobiomok összetétele eltér a megfelelő egészséges mikrobiomoktól PA-ban, mely diagnosztikára használható. A szájüregi mikrobiom esetében a Neisseria elongata (28), a Streptococcus mitis (28), a Haemophilus (51), a Porphyromonas (51), a Leptotrichia (51) és a Fusobacterium (51) fajok validált biomarkerei a PA-nak (28). A PA-rizikóval összefüggést mutat a szájüregben a Haemophilus, az Enterobacteriaceae, a Lachnospiraceae, a Bacteroidaceae és a Staphylococcaceae genusok pozitív korrelációt mutattak a PA-kockázattal (53). Segítségükkel meg lehet becsülni a daganat kialakulásának esélyét (47) és a túlélést (18, 56). Az etiológia vizsgálata (72), a mortalitás predikciója (54), az obstruktív/non obstruktív forma (20) elkülönítése is lehetséges.
A legtöbb klinikai vizsgálat alacsony betegszámmal történt (néhány tíztől néhány száz betegig), és emiatt az eredmények interpretációja nagyobb populáción korlátozott értékű. Több ezer tumor bakteriális DNS-adatait elemezve a tumorokban detektált baktériumszám különbözött a nem tumorosan átalakult szövetekétől, ráadásul jellegzetes, jövőbeni diagnosztikára alkalmas eltérésmintázatokat azonosítottak (64). A mintázatokat a szérumban is kimutatták szabad DNS formájában, tehát a szérumot is lehetne használni diagnosztikus célra (64). A könnyen hozzáférhető szájtörlet vagy székletminta is alkalmas lehet a PA korai diagnosztikájára (47, 53, 72).
A PA diagnosztikája a kurábilis stádiumban igen nehéz, azonban az onkobiotikus transzformáció kimutatása révén a hasnyálmirigy-adenocarcinoma korán diagnosztizálható, ami jelentős előnnyel jár a betegek számára. A sebészi eltávolítás előtti premedikáció során használt antibiotikumokat a pancreasmikrobiom alapján is meg lehet választani, amely szintén befolyásolja a betegség lefolyását (57).
2. táblázat: PA-ban azonosított bakteriális szignálmetabolitok
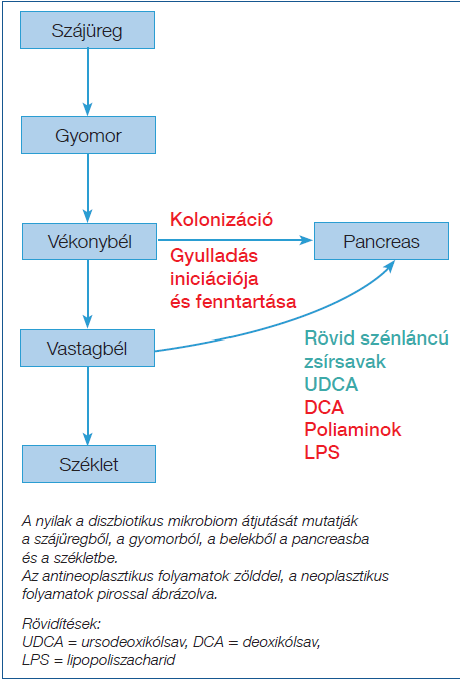
1. ábra: Az onkobiózis szerepe pancreas-adenocarcinomában (vázlat)
5. Jövőbeni irányok
Az onkobiózis komplex folyamat PA-ban, amely több mikrobiom-kompartmentet érint, beleértve a szájüregi, a gyomor-, a duodenalis, a ductalis, a hasnyálmirigy-, a bél- és a székletmikrobiomokat. A pancreas bakteriális kolonizációja gyulladást kelt, és valószínűsíthetően megkönnyíti a tumoriniciációt, a progressziót, valamint befolyásolja a tumor agresszivitását, grádusát. Nagyszámú, sokféle bakteriális metabolit kerül a keringésbe, a tumor mikrokörnyezetébe, amelyek direkt hatást fejtenek ki a PA-sejtek viselkedésére ( 1. ábra, 2. táblázat).
A bakteriális metabolitok szerepe a közelmúltban lett hangsúlyos a mikrobiomkutatások területén. Egyéb daganatokban a mikrobiom szerepe gyorsan teret nyert, és új kezelési lehetőségeket nyitott meg (74). A mikrobiom metabolizmusának in silico rekonstrukciója és vizsgálata, és egyéb közvetett adat alapján a bakteriális metabolom jelentős változáson megy keresztül. Valószínűsíthető, hogy a jövőben további metabolitokat azonosítanak és jellemeznek.
Az onkobiózis oki szerepet játszik a PA kialakulásában. Más betegségek kapcsán végzett tanulmányok igazolják, hogy a pre-, a pro- és az antibiotikumok hatnak az adott betegség lefolyására. Ezek miatt feltételezhető, hogy ha az onkobiomot prebiotikumokkal, probiotikumokkal és antibiotikumokkal megváltoztatjuk, az a PA lefolyását is befolyásolhatja: a jövőben egyénre szabhatjuk a diétát és az orvosi beavatkozásokat. A PA-ban létrejövő onkobiom mélyebb megismerésével megnyújthatjuk a betegek túlélését.

Munkánkat támogatta: NKFIH (K123975; PD124110; FK128387; GINOP-2.3.2-15-2016-00006; EFOP-3.6.2-16-2017-0006; K120669; Magyar Tudományos Akadémia: Bolyai-ösztöndíj; NKFIH-1150-6/2019; ÚNKP-19-4-DE-79. A tanulmány alapjául szolgáló kutatást az Innovációs és Technológiai Minisztérium által meghirdetett Tématerületi Kiválósági Program (TKP2020-IKA-04) támogatta.
1. Ducreux M, Cuhna AS, Caramella C. et al. Cancer of the pancreas: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Ann Oncol. 2015; 26: v56–68.
2. Pei X, Song F, Wang Z. Emerging incidence trends and application of curative treatments of pancreatic cancer in the USA. Medicine (Baltimore). 2019; 98: e17175.
3. Chun YS, Pawlik TM, Vauthey JN. 8th Edition of the AJCC Cancer Staging Manual: Pancreas and Hepatobiliary Cancers. Ann Surg Oncol. 2018; 25: 845–847.
4. Lowery MA, Kelsen DP, Capanu M, et al. Phase II trial of veliparib in patients with previously treated BRCA-mutated pancreas ductal adenocarcinoma. Eur J Cancer. 2018; 89: 19–26.
5. Silvestris N, Longo V, Cellini F, et al. Neoadjuvant multimodal treatment of pancreatic ductal adenocarcinoma. Crit Rev Oncol Hematol 2016; 98: 309–324. doi:10.1016/j.critrevonc.2015.11.016.
6. Yeo TP. Demographics, epidemiology, and inheritance of pancreatic ductal adenocarcinoma. Semin Oncol. 2015; 42: 8–18.
7. Waddell N, Pajic M, Patch AM, et al. Whole genomes redefine the mutational landscape of pancreatic cancer. Nature. 2015; 518: 495–501.
8. Hashimoto D, Arima K, Yokoyama N, et al. Heterogeneity of KRAS Mutations in Pancreatic Ductal Adenocarcinoma. Pancreas. 2016; 45: 1111–1114.
9. Schwabe RF, Jobin C. The microbiome and cancer. Nat Rev Cancer 2013; 13: 800–812.
10. Kovacs T, Miko E, Ujlaki G et al. The Microbiome as a Component of the Tumor Microenvironment. Adv Exp Med Biol 2020; 1225: 137–153.
11. Hanahan D, Weinberg RA. Hallmarks of cancer: the next generation. Cell 2011; 144: 646–674.
12. Hanahan D, Weinberg RA. The hallmarks of cancer. Cell. 2000; 100: 57–70.
13. Lau A, Villeneuve NF, Sun Z et al. Dual roles of Nrf2 in cancer. Pharmacol Res 2008; 58: 262–270. doi:10.1016/j.phrs.2008.09.003.
14. Jezierska-Drutel A, Rosenzweig SA, Neumann CA. Role of oxidative stress and the microenvironment in breast cancer development and progression. Adv Cancer Res 2013; 119: 107–125.
15. Smolková K, Mikó E, Kovács T et al. NRF2 in regulating cancer metabolism. Antioxid Redox Signal 2020; 33: 966–997. doi: 10.1089/ars.2020.8024.
16. Pagliari D, Saviano A, Newton EE, et al. Gut Microbiota-Immune System Crosstalk and Pancreatic Disorders. Mediators Inflamm. 2018; 2018: 7946431.
17. Ochi A, Nguyen AH, Bedrosian AS et al. MyD88 inhibition amplifies dendritic cell capacity to promote pancreatic carcinogenesis via Th2 cells. J Exp Med. 2012; 209: 1671–1687.
18. Pushalkar S, Hundeyin M, Daley D, et al. The Pancreatic Cancer Microbiome Promotes Oncogenesis by Induction of Innate and Adaptive Immune Suppression. Cancer Discov. 2018; 8: 403–416.
19. Sethi V, Kurtom S, Tarique M, et al. Gut Microbiota Promotes Tumor Growth in Mice by Modulating Immune Response. Gastroenterology. 2018; 155: 33–37.
20. Ren Z, Jiang J, Xie H et al. Gut microbial profile analysis by MiSeq sequencing of pancreatic carcinoma patients in China. Oncotarget. 2017; 8: 95176–95191.
21. Kovács P, Csonka T, Kovács T et al. Lithocholic acid, a metabolite of the microbiome, increases oxidative stress in breast cancer. Cancers (Basel) 2019; doi: 10.3390/cancers11091255.
22. Zitvogel L, Ayyoub M, Routy B, et al. Microbiome and Anticancer Immunosurveillance. Cell. 2016; 165: 276–287.
23. Gopalakrishnan V, Spencer CN, Nezi L et al. Gut microbiome modulates response to anti-PD-1 immunotherapy in melanoma patients. Science. 2018; 359: 97–103.
24. Buchta Rosean C, Bostic RR, Ferey JCM, et al. Preexisting Commensal Dysbiosis Is a Host-Intrinsic Regulator of Tissue Inflammation and Tumor Cell Dissemination in Hormone Receptor-Positive Breast Cancer. Cancer Res. 2019; 79: 3662–3675.
25. Miko E, Vida A, Kovacs T, et al. Lithocholic acid, a bacterial metabolite reduces breast cancer cell proliferation and aggressiveness. Biochim Biophys Acta 2018; 1859: 958–974.
26. Miko E, Kovacs T, Sebo E, et al. Microbiome-Microbial Metabolome-Cancer Cell Interactions in Breast Cancer-Familiar, but Unexplored. Cells. 2019; 8(4): E293.
27. Lindkvist B, Johansen D, Borgstrom A, et al. A prospective study of Helicobacter pylori in relation to the risk for pancreatic cancer. BMC Cancer. 2008; doi: 10.1186/1471-2407-1188-1321.
28. Farrell JJ, Zhang L, Zhou H, et al. Variations of oral microbiota are associated with pancreatic diseases including pancreatic cancer. Gut. 2012; 61: 582–588.
29. Mei QX, Huang CL, Luo SZ, et al. Characterization of the duodenal bacterial microbiota in patients with pancreatic head cancer vs. healthy controls. Pancreatology. 2018; 18: 438–445.
30. Thomas RM, Gharaibeh RZ, Gauthier J, et al. Intestinal microbiota enhances pancreatic carcinogenesis in preclinical models. Carcinogenesis. 2018; 39: 1068–1078.
31. tic Cancer: An Evidence-based Association? J Clin Gastroenterol 2018; 52 Suppl 1, Proceedings from the 9th Probiotics, Prebiotics and New Foods, Nutraceuticals and Botanicals for Nutrition & Human and Microbiota Health Meeting, held in Rome, Italy from September 10 to 12, 2017; S82–S85, doi:10.1097/MCG.0000000000001092.
32. Mendez R, Kesh K, Arora N, et al. Microbial dysbiosis and polyamine metabolism as predictive markers for early detection of pancreatic cancer. Carcinogenesis 2019; 1.
33. Aykut B, Pushalkar S, Chen R, et al. The fungal mycobiome promotes pancreatic oncogenesis via activation of MBL. Nature. 2019; 574: 264–267.
34. Frulloni L, Lunardi C, Simone R, et al. Identification of a novel antibody associated with autoimmune pancreatitis. N Engl J Med. 2009; 361: 2135–2142.
35. Risch HA, Lu L, Kidd MS, et al. Helicobacter pylori seropositivities and risk of pancreatic carcinoma. Cancer Epidemiol Biomarkers Prev. 2014; 23: 172–178.
36. Wang Y, Zhang FC, Wang YJ. Helicobacter pylori and pancreatic cancer risk: a meta- analysis based on 2,049 cases and 2,861 controls. Asian Pac J Cancer Prev 2014; 15: 4449–4454.
37. Rabelo-Goncalves EM, Roesler BM, Zeitune JM. Extragastric manifestations of Helicobacter pylori infection: Possible role of bacterium in liver and pancreas diseases. World J Hepatol. 2015; 7: 2968–2979.
38. Chen XZ, Wang R, Chen HN et al. Cytotoxin-Associated Gene A-Negative Strains of Helicobacter pylori as a Potential Risk Factor of Pancreatic Cancer: A Meta-Analysis Based on Nested Case-Control Studies. Pancreas. 2015; 44: 1340–1344.
39. Maisonneuve P, Lowenfels AB. Risk factors for pancreatic cancer: a summary review of meta-analytical studies. Int J Epidemiol. 2015; 44: 186–198.
40. Ertz-Archambault N, Keim P, Von Hoff D. Microbiome and pancreatic cancer: A comprehensive topic review of literature. World J Gastroenterol. 2017; 23: 1899–1908.
41. Tenti P, Aguzzi A, Riva C. Ovarian mucinous tumors frequently express markers of gastric, intestinal, and pancreatobiliary epithelial cells. Cancer. 1992; 69: 2131–2142.
42. Ogrendik M. Periodontal Pathogens in the Etiology of Pancreatic Cancer. Gastrointest Tumors. 2017; 3: 125–127.
43. Wei MY, Shi S, Liang C, et al. The microbiota and microbiome in pancreatic cancer: more influential than expected. Mol Cancer 2019; 18: 97. doi:10.1186/s12943-019-1008-0.
44. Zambirinis CP, Pushalkar S, Saxena D, et al. Pancreatic cancer, inflammation, and microbiome. Cancer J 2014; 20: 195–202. doi:10.1097/PPO.0000000000000045.
45. Mima K, Nakagawa S, Sawayama H, et al. The microbiome and hepatobiliary-pancreatic cancers. Cancer Lett. 2017; 402: 9–15.
46. Hujoel PP, Drangsholt M, Spiekerman C, et al. An exploration of the periodontitis-cancer association. Ann Epidemiol. 2003; 13: 312–316.
47. Michaud DS, Izard J, Wilhelm-Benartzi CS, et al. Plasma antibodies to oral bacteria and risk of pancreatic cancer in a large European prospective cohort study. Gut. 2013; 62: 1764–1770.
48. Torres PJ, Fletcher EM, Gibbons SM, et al. Characterization of the salivary microbiome in patients with pancreatic cancer. PeerJ. 2015; 3: e1373.
49. Nieminen MT, Listyarifah D, Hagstrom J, et al. Treponema denticola chymotrypsin-like proteinase may contribute to orodigestive carcinogenesis through immunomodulation. Br J Cancer. 2018; 118: 428–434.
50. Fan X, Alekseyenko AV, Wu J, et al. Human oral microbiome and prospective risk for pancreatic cancer: a population-based nested case-control study. Gut. 2018; 67: 120–127.
51. Lu H, Ren Z, Li A, et al. Tongue coating microbiome data distinguish patients with pancreatic head cancer from healthy controls. J Oral Microbiol 2019; 11: 1563409, doi:10.1080/20002297.2018.1563409.
52. Gaiser RA, Halimi A, Alkharaan H, et al. Enrichment of oral microbiota in early cystic precursors to invasive pancreatic cancer. Gut. 2019; 68: 2186–2194.
53. Vogtmann E, Han Y, Caporaso JG, et al. Oral microbial community composition is associated with pancreatic cancer: A case-control study in Iran. Cancer Med. 2020; 9: 797–806.
54. Mitsuhashi K, Nosho K, Sukawa Y, et al. Association of Fusobacterium species in pancreatic cancer tissues with molecular features and prognosis. Oncotarget. 2015; 6: 7209–7220.
55. Maekawa T, Fukaya R, Takamatsu S, et al. Possible involvement of Enterococcus infection in the pathogenesis of chronic pancreatitis and cancer. Biochem Biophys Res Commun. 2018; 506: 962–969.
56. Riquelme E, Zhang Y, Zhang L, et al. Tumor Microbiome Diversity and Composition Influence Pancreatic Cancer Outcomes. Cell. 2019; 178: 795–806.
57. Swan CD, Nahm C, Samra JS, et al. Microbiology of pancreatoduodenectomy and recommendations for antimicrobial prophylaxis. ANZ J Surg 2019; 19: 15560.
58. Di Carlo P, Serra N, D’Arpa F, et al. The microbiota of the bilio-pancreatic system: a cohort, STROBE-compliant study. Infect Drug Resist. 2019; 12: 1513–1527.
59. Del Castillo E, Meier R, Chung M, et al. The Microbiomes of Pancreatic and Duodenum Tissue Overlap and Are Highly Subject Specific but Differ between Pancreatic Cancer and Noncancer Subjects. Cancer Epidemiol Biomarkers Prev. 2019; 28: 370–383.
60. Boursi B, Mamtani R, Haynes K, et al. Recurrent antibiotic exposure may promote cancer formation – Another step in understanding the role of the human microbiota? Eur J Cancer 2015; 51: 2655–2664. doi:10.1016/j.ejca.2015.08.015.
61. Tsuji Y, Watanabe T. Kudo M, et al. Sensing of commensal organisms by the intracellular sensor NOD1 mediates experimental pancreatitis. Immunity. 2012; 37: 326–338.
62. Leal-Lopes C, Velloso FJ, Campopiano JC, et al. Roles of Commensal Microbiota in Pancreas Homeostasis and Pancreatic Pathologies. J Diabetes Res, 2015; 2015: 284680.
A további irodalom megtalálható a szerkesztőségben, valamint
a www.gastronews.hu weboldalon.
63. Michaud DS. Role of bacterial infections in pancreatic cancer. Carcinogenesis. 2013; 34: 2193–2197.
64. Poore GD, Kopylova E, Zhu Q, et al. Microbiome analyses of blood and tissues suggest cancer diagnostic approach. Nature 2020; 579: 567–574. doi:10.1038/s41586-020-2095-1.
65. Grimmig T, Moench R, Kreckel J, et al. Toll Like Receptor 2, 4, and 9 Signaling Promotes Autoregulative Tumor Cell Growth and VEGF/PDGF Expression in Human Pancreatic Cancer. Int J Mol Sci. 2016; 17(12): ijms17122060.
66. Yoshimoto S, Loo TM, Atarashi K, et al. Obesity-induced gut microbial metabolite promotes liver cancer through senescence secretome. Nature. 2013; 499: 97–101. doi:10.1038/nature12347.
67. Ridlon JM, Bajaj JS. The human gut sterolbiome: bile acid-microbiome endocrine aspects and therapeutics. Acta Pharm Sin B. 2015; 5: 99–105.
68. Zeng H, Umar S, Rust B, et al. Secondary Bile Acids and Short Chain Fatty Acids in the Colon: A Focus on Colonic Microbiome, Cell Proliferation, Inflammation, and Cancer. Int J Mol Sci. 2019; 20(5): doi: 10.3390/ijms20051214.
69. Sittipo P, Shim JW, Lee YK. Microbial Metabolites Determine Host Health and the Status of Some Diseases. Int J Mol Sci. 2019; 20: E5296.
70. Miko E, Vida A, Bai P. Translational aspects of the microbiome-to be exploited. Cell Biol Toxicol. 2016; 32: 153–156.
71. Kiss B, Mikó E, Sebő É, et al. Oncobiosis and Microbial Metabolite Signaling in Pancreatic Adenocarcinoma. Cancers (Basel) 2020; 12: E1068. doi:10.3390/cancers12051068.
72. Half E, Keren N, Reshef L, et al. Fecal microbiome signatures of pancreatic cancer patients. Sci Rep. 2019; 9: 16801.
73. Ansari D, Toren W, Zhou Q, et al. Proteomic and genomic profiling of pancreatic cancer. Cell Biol Toxicol. 2019; 35: 333–343.
74. Descamps HC, Herrmann B, Wiredu D, et al. The path toward using microbial metabolites as therapies. EBioMedicine. 2019; 44: 747–754.
