Reviews
Endoscopic full-thickness resection (EFTR) – Where do we stand?
Summary
The FTRD device, which provides endoscopic full-thickness resection, has been available since 2018 in Hungary. The indications include the removal of submucosal lesions, non-lifting adenomas and early carcinomas (also providing the accurate staging), however its role in the everyday practice is not yet fully determined due to the limited evidence of its practical application. Its use is restricted by licence, and applying for individual funding can compensate for the relatively high cost of the device.
Összefoglalás
Hazánkban 2018 óta érhető el az endoszkópos, teljes falvastagságú reszekcióra lehetőséget biztosító FTRD eszköz. Indikációs köre magában foglalja a submucosus terimék, nem elemelkedő adenomák és korai karcinómák eltávolítását (utóbbiaknál pontos stádiummeghatározást biztosítva), azonban az alkalmazásával kapcsolatos limitált evidenciák miatt a mindennapi gyakorlatban betöltött szerepe még nem kiforrott. Alkalmazása a gyártó cég által szervezett képzéshez kötött, szélesebb körben való elterjedését az eszköz magas költsége is hátráltatja, ezt enyhítendő a beavatkozás elvégzését hazánkban jelenleg egyedi méltányossági rendszer támogatja.
Bevezetés
Az endoszkópos teljes falvastagságú reszekciót (EFTR) a subepithelialis léziók eltávolításának minimálinvazív alternatívájaként fejlesztették ki az 1990-es évek végén. Bár az eljárással kapcsolatos első sikeres eredményekről subepithelialis léziók esetén már 2001-ben beszámoltak, az eszköz Európában 2014 óta érhető el, hazánkban pedig 2018 óta (1, 2, 3). A kimondottan felső tápcsatornai, gasztroduodenális FTRD-t (full thickness resection device, teljes falvastagságú reszekciós eszköz) Európában 2021, hazánkban 2022-ben vezették be. A minimálinvazív módon történő teljes falvastagságú reszekció nem csupán a subepithelialis eltérések eltávolítására biztosít lehetőséget, hanem a premalignus és korai, alacsony metasztatikus potenciállal rendelkező malignus eltérések esetén is alternatívát jelenthet nagy műtéti kockázatú betegcsoportok esetén. Ennek köszönhetően a módszer indikációs köre az elmúlt évtizedekben jelentősen bővült, nemzeti és európai szakmai irányelvekben is fokozatosan megjelenik a használata. Az FTRD alkalmazása külön képzéshez kötött, igazolás megszerzése után végezhető a beavatkozás.
Az elv
Az EFTR során az endoszkópos mucosareszekcióval és az endoszkópos submucosadisszekcióval ellentétben (amelyek kizárólag nyálkahártya és felszínes submucosa lokalizációjú eltérések eltávolítását teszik lehetővé) lehetőség van elvileg akár a muszkuláris propriából kiinduló léziók komplett eltávolítására minimálinvazív módon. Az eljárás során egy speciális, teljes vastagságú reszekciós eszköz, az ún. FTRD (full thickness resection device) alkalmazásával történik a kívánt lézió teljes falvastagású kimetszése. Az FTRD a zárás és reszekálás elvét követi. Az FTRD egy, a hagyományos endoszkóp végére felszerelhető átlátszó applikátor feltétet, egy módosított, az endoszkópra kívülről felhelyezhető OTSC (over-the-scope) klippet és egy rendszerint 13 mm-es monofilament hurkot foglal magában (1. ábra).

A hagyományosnál mélyebb kialakítású feltét több szövet befogadását teszi lehetővé (4). Az FTRD része továbbá egy jelölőszonda, illetve egy fogó, amelyek a munkacsatornán keresztül könnyítik meg az eltávolítani kívánt lézió körbejelölését és mobilizálását (3). Az FTRD alkalmazáskor a vizsgálat során az első lépés az eltávolítani kívánt lézió körbejelölése. Ez után az FTRD szettel felszerelt endoszkóppal, speciális fogóval a kupakba történő célterület behúzása (szívással történő rásegítése kerülendő az esetleges célterület mögötti szervek behúzásának és sérülésének veszélye miatt) – ügyelve arra, hogy az előzetes jelölések a feltéten belülre kerüljenek –, majd az over-the-scope klipp oldásával összhangban, közvetlenül utána történik meg a hurkolás, majd az elektrokoaguláció (a feltétbe gyárilag beépítve), és a lézió eltávolítása. Az eltávolított specimen kitűzve továbbítandó szövettani vizsgálatra (2., 3. ábra).
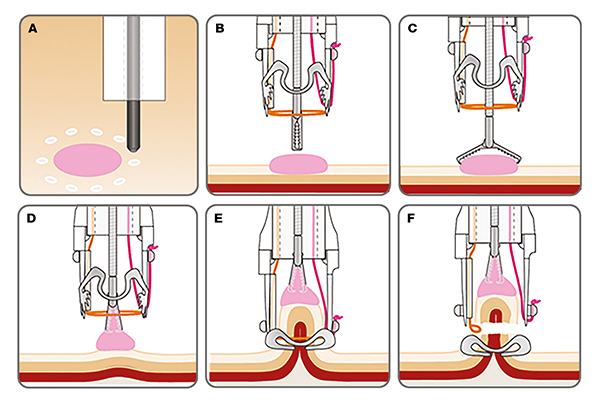
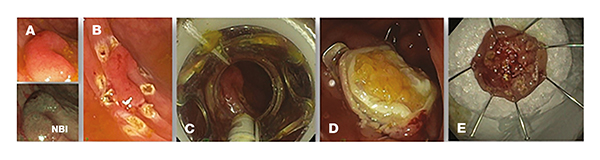
Ezen lépéssor nagy összhangot igényel a beavatkozást végző orvos és asszisztenciája között, az eszköz alkalmazásához szükséges képzés során erre nagy hangsúly helyeződik.
Az alsó és felső tápcsatornai EFTR technikai kivitelezése nem tér el egymástól, köztük az egyetlen lényegi eltérést az FTRD mérete jelenti (standard alsó tápcsatornai FTRD esetén az átmérője 21 mm, gasztroduodenális esetén 19,5 mm). Ezenfelül a gasztroduodenális FTRD részét képezi egy, a nyelőcsőbe lejutást és a pyloruson való átjutást elősegítő ballon és vezetődrót. Nemrégiben egy harmadik FTRD fejlesztésére is sor került, amely diagnosztikus céllal alkalmazható az alsó tápcsatornában, mind reszekció, mind teljes falvastagságú biopszia elvégzésére, mivel kisebb mérete miatt kevesebb szövet kivételével jár (3).
Indikációk és bővülésük
Az ETFR indikációi az 1. táblázatban szerepelnek (5).

Subepithelialis terimék eltávolítása
A felső tápcsatornai subepithelialis léziók esetén a kezdeti vizsgálatok többsége relatíve kicsi, 30-nál kisebb esetszámról számolt be, amelyek többnyire a hagyományos (jelenleg mérete miatt már csak alsó tápcsatornai indikációkkal alkalmazott) FTRD-vel történtek. A gyomor subepithelialis lézióinak gasztroduodenális FTRD-vel történő eltávolításával kapcsolatos, első prospektív, multicentrikus tanulmány (RESET trial) eredményeit Meier és munkatársai tették közzé 2020-ban: a módszer technikai sikerességét közel 90%-nak találtak, az R0 reszekciós arány ezzel szemben 75%-nak bizonyult (6). Egy friss, 2023-ban megjelent japán, multicentrikus, prospektív tanulmány 46 submucosus gyomorterime eltávolításának kimenetelét vizsgálta. Azt találták, hogy a teljes falvastagság reszekciójára az esetek 93%-ában került sor, a submucosus léziók hisztológiailag megerősíthető R0 reszekciójára pedig az esetek 77%-ában (7). Egy, a közelmúltban megjelent, retrospektív, összehasonlító tanulmány alapján az EFTR a cardia lokalizációjú, subepithelialis léziók eltávolításának is ígéretes minimálinvazív alternatívája lehet. A modalitással 100%-os en bloc reszekciós arányt értek el, 96,1%-os komplett reszekcióval, ami a sebészeti eredményeket és egyéb endoszkópos módszereket messze felülmúlja (8). Az egyéb lokalizációban (nyelőcső, duodenum, rectum) subepithelialis léziók eltávolítására végzett EFTR-ről többnyire esettanulmányok állnak rendelkezésünkre, amelyekből messzemenő következtetést levonni nem lehetséges.
Premalignus és korai malignus léziók eltávolítása
A legtöbb, EFTR-rel foglalkozó tanulmány a recidív kolorektális adenomák indikációjával végzett vizsgálatokat vette górcső alá, amelyekben azt találták, hogy ebben az esetben lesz a legnagyobb az R0 reszekciós arány az EMR-rel és ESD-vel összehasonlítva (9, 10, 11), azonban ki kell hangsúlyoznunk azt is, hogy előzőleg EMR-en átesett lézióknál a hegesedés az EFTR esetén is gondot jelenthet. Ugyanakkor egy, korai kolorektális malignus léziók EFTR-eltávolítását vizsgáló német tanulmány alapján magasabb R0 reszekciós arányról számoltak be az előzőleg már endoszkópos eltávolításon átesett, reziduális vagy recidív léziók esetén, mint a korábban nem kezelt, nem előemelkedő lézióknál (87,5% vs. 60,9%) (12).
A T1 stádiumú kolorektális daganatoknak a submucosainvázió mélységétől függően eltérő metasztatikus potenciálja miatt az optimális kezelés megválasztásához elengedhetetlen a mélységi invázió, valamint az egyéb hisztológiai prognosztikus jellemzők (pl. tumordifferenciáltság, limfovaszkuláris invázió, tumorbudding [„bimbózás”]) ismerete. Az EMR és ESD limitációját jelenti, hogy ezen módszerek alkalmazása esetén nem a teljes submucosát távolítják el, így nincs lehetőség annak megítélésére, hogy a submucosa milyen arányban érintett a tumoros folyamat által. A teljes falvastagságú reszekció biztosításával az EFTR megoldást kínálhat erre a problémára, hiszen pontos stádiummeghatározást tesz lehetővé, ráadásul felszínes submucosainvázió (sm1) esetén – ha az egyéb hisztológiai prognosztikus jellemzők is kedvezőek – kuratív megoldást is jelenthet (13) (4. ábra).
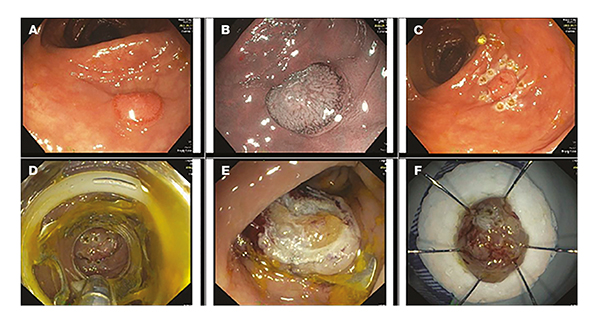
F) kitűzött specimen
A korai kolorektális karcinómák esetén készült a legtöbb tanulmány az EFTR sikerességét illetően. Kuellmer és munkatársai 71,8%-ban végeztek R0 reszekciót T1 stádiumú tumorok esetén (12). Egy holland multicentrikus tanulmány, amely összesen 330, T1 CRC miatt történt EFTR kimenetelét vizsgálta, a technikai sikerrátát 87%-nak, az R0 reszekció arányát 86%-nak találta, a kuratív reszekció arányát pedig
60%-nak. Első kezelésként végzett beavatkozás esetén a kuratív reszekció aránya 32% volt, míg egy korábbi, inkomplett reszekció után sokkal magasabb, 79%-os arányban volt kivitelezhető a komplettálás (9). Egy metaanalízis, amely 1936, EFTR-rel kezelt beteg adatait dolgozta fel (az esetek 57,7%-ában adenoma, 21,2%-ában T1 tumor indikációval történt az intervenció), 87,6%-os technikai sikerrátát és 78,8%-os R0 reszekciós rátát igazolt (14).
Ezek alapján az Európai Gasztroenterológiai Endoszkópos Társaság (European Society for Gastrointestinal Endoscopy, ESGE) legújabb, 2024-es ajánlásában az EFTR már felszínes submucosainváziót mutató, T1 kolorektális karcinóma eltávolítása után a reziduális vagy rekurráló lézió esetén is választható alternatívaként szerepel, ha az eltávolított adenokarcinóma szövettani vizsgálata en bloc R0 reszekciót igazol, az adenokarcinóma jól differenciált, a submucosainfiltráció kisebb, mint 1 mm, és nem észlelhető limfovaszkuláris invázió és tumorbudding, ezzel is bővítve annak indikációs körét az alsó tápcsatornában (15).
Az alsó tápcsatornával ellentétben a felső tápcsatornai premalignus és korai malignus, nyálkahártya-kiindulású daganatok EFTR-rel történő eltávolításáról sokkal kevesebb, főként esettanulmányokból származó adat áll rendelkezésre. A legtöbb, gasztroduodenális FTRD-t vizsgáló tanulmány nem kezelte külön a különböző indikációkat (submucosus képletek, premalignus/korai malignus léziók), így ezek alapján messzemenő következtetés ezen indikációban való alkalmazásról ez idáig nem vonható le (3) (5. ábra).
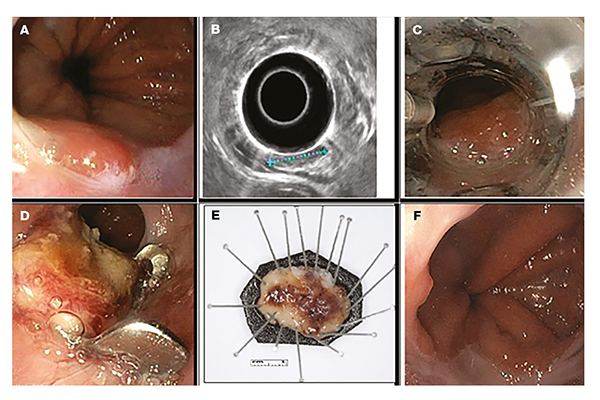
Fenti adatok is rámutatnak arra, hogy a cég által meghatározott indikációk és az irányelvekbe foglaltak között diszkrepancia tapasztalható, amely abból fakad, hogy submucosus terimék esetén kisebb tapasztalat áll rendelkezésünkre, a körbejelölésük nehezebb feladat, mint egy elő nem emelkedő lézió esetén. Ahogy az EFTR elterjedtebbé válik, várható, hogy az irányelvekben is bővülni fog majd az indikációs köre.
Az EFTR szövődményrátája
Az összesített szövődményráta kolorektális léziók esetén 2,2–17%, átlagosan 10-12% közötti. A holland és a német EFTR-regiszter alapján ez az arány 11,3%-nak bizonyult, amelyből súlyos szövődményt, amely műtéti beavatkozást igényelt, az esetek 2,2%-ában detektáltak (16). Szövődménynek tekintették még a vérzést, amely transzfúziót igényelt. A vizsgálat leggyakoribb szövődménye a vérzés vagy perforáció, amelyet az észlelés pillanatában el kell látni endoszkópos úton, ha lehetséges. Vérzés esetén a koagulálás választandó, illetve nagyobb erek esetén, vagy ha koagulációval nem uralható a vérzés, akkor a klippelés (13). A súlyos szövődményeket tekintve a kolorektális léziók esetén 2,2–17% közötti arányokat találhatunk különböző tanulmányokban, míg a felső tápcsatornában ez az arány 21–31% között helyezkedik el, a különbség abból is fakad, hogy az egyes tanulmányok miként határozták meg a súlyos szövődményeket (3).
Az EFTR limitációi és helye a mindennapi klinikai gyakorlatban
Az FTRD egyik legfőbb limitációja az eltávolítható lézió mérete, amely a feltét dimenziójából fakad: általánosságban elmondható, hogy 20-25 mm-nél nagyobb lézió esetén kérdéses a biztonságos szegéllyel történő R0 reszekció kivitelezhetősége. Bár a szakirodalomban egyes expert vizsgálóktól származó közleményekben beszámolnak 35 mm-es duodenális, illetve 30 mm-es kolorektális lézió sikeres EFTR-eltávolításáról is, ezek a mindennapi gyakorlatban továbbra is kihívást jelentenek (9, 17). Az ún. hibrid EFTR megoldást jelenthet a fentieknél nagyobb kiterjedésű, részlegesen előemelkedő kolorektális adenomák esetén, amelyeknél a nem elemelkedő részen felmerül invazív malignitás lehetősége. Hibrid EFTR során az előemelkedő részeket hagyományos EMR segítségével eltávolítva, a nem előemelkedő résznél EFTR alkalmazható. Az ígéretes szakirodalmi adatok ellenére erről szakmai állásfoglalás még nem született (18, 19). További limitációt jelenthet, hogy az eltávolítani kívánt léziók többsége – egy korábbi endoszkópos reszekció után – heges környezetben található, amely a mobilizációjukat teszi nehézkéssé.
A módszer hétköznapi alkalmazhatóságát meghatározó limitációja, amelyet az irányelvekben is említenek, az FTRD magas költsége. Az utóbbi években hazánkban is elérhetővé vált EFTR alkalmazását jelenleg az egyedi méltányossági rendszer támogatja. Malignus, illetve malignitásra gyanús léziók esetén a kérelemhez onkoteam véleményezése is szükséges. Az EFTR-rel szerzett eddigi tapasztalatokról a Magyar Gasztroenterológiai Társaság 66. Nagygyűlésén számoltak be először, országos szinten 36 eset adatait feldolgozva (20).
Alapvetően az EFTR kontraindikációját képezik a 30 mm-nél nagyobb léziók, hiszen ebben az esetben nem fér az FTRD-be a teljes lézió, ezáltal az R0 reszekció nem kivitelezhető. Korai invazív, T1 stádiumú kolorektális karcinóma esetén mély submucosainvázió (legalább sm2) gyanúja, illetve nyirokcsomó-érintettség esetén kuratív reszekció EFTR-rel nem kivitelezhető. Technikai kivitelezhetőség szempontjából kontraindikációt jelentenek továbbá az FTRD-vel felszerelt endoszkóp számára át nem járható tápcsatornai szűkületek a célterület előtt (21).
Az ETFR végzése licencvizsgához kötött, amely a felső és alsó tápcsatornai EFTR esetén külön végzendő. Ezzel együtt az EFTR-nek minimálinvazív jellegéből adódóan egyre kiemeltebb szerep jut a mindennapokban, hiszen az invazív endoszkópos szervvesztés nélkül, a nagyobb műtéti megterhelés elkerülésével tud a beteg segítségére lenni. Habár az EFTR alkalmazása már az irányelvekben is megjelent, a diagnosztikus és terápiás algoritmusba való tényleges alternatívaként való bekerülése előtt további, nagy esetszámot feldolgozó, lehetőség szerint prospektív, valós életbeli adatokat feldolgozó klinikai vizsgálatok szükségesek, amelyek a hosszú távú követést és a késői szövődményeket is magukba foglalják. Ennek elősegítésére hazánkban a szegedi munkacsoport (jelen cikk szerzői) EFTR-regiszter létrehozásán dolgozik.
Irodalom
Reached the Limit? Endoscopy 1998; 30(06): 578–578.
https://doi.org/10.1055/s-2007-1001348
2. Suzuki H, Ikeda K. Endoscopic mucosal resection and full thickness resection with complete defect closure for early gastrointestinal malignancies. Endoscopy 2001; 33(5): 437–439. https://doi.org/10.1055/s-2001-14269
3. Mun EJ, Wagh MS. Recent advances and current challenges in endoscopic resection with the full-thickness resection device. World J Gastroenterol 2023; 29(25): 4009–4020. https://doi.org/10.3748/wjg.v29.i25.4009
4. Aslanian HR, Sethi A, Bhutani MS, et al. ASGE guideline for endoscopic full-thickness resection and submucosal tunnel endoscopic resection. VideoGIE 2019; 4(8): 343–350. https://doi.org/10.1016/j.vgie.2019.03.010
5. Emberi Erőforrások Minisztériuma Egészségügyi Szakmai Kollégium. Egészségügyi Szakmai Irányelv – Az Endoszkópos Polipektómia, Mukozektómia, Endoszkópos Submucosa Disszekció, Endoszkópos Teljes Rétegvastagságú Reszekcióról. 2021. https://kollegium.aeek.hu
6. Meier B, Schmidt A, Glaser N, et al. Endoscopic full-thickness resection of gastric subepithelial tumors with the gFTRD-system: a prospective pilot study (RESET trial). Surg Endosc 2020; 34(2): 853–860.
https://doi.org/10.1007/s00464-019-06839-2
7. Shichijo S, Uedo N, Sawada A, et al. Endoscopic full-thickness resection for gastric submucosal tumors: Japanese multicenter prospective study. Digestive Endoscopy. Published online 2023.
https://doi.org/10.1111/den.14717
8. Xu EP, Qi ZP, Li B, et al. The efficacy of full-thickness endoscopic resection of subepithelial tumors in the gastric cardia. World J Gastrointest Oncol 2023; 15(12): 2111–2119. https://doi.org/10.4251/WJGO.V15.I12.2111
9. Zwager LW, Bastiaansen BAJ, Bronzwaer MES, et al. Endoscopic full-thickness resection (eFTR) of colorectal lesions: Results from the Dutch colorectal eFTR registry. Endoscopy 2020; 52(11): 1014–1023.
https://doi.org/10.1055/a-1176-1107
10. Falt P, Zapletalová J, Urban O. Endoscopic full-thickness resection versus endoscopic submucosal dissection in the treatment of colonic neoplastic lesions ≤30 mm – A single-center experience. Surg Endosc 2022; 36(3): 2062–2069. https://doi.org/10.1007/s00464-021-08492-0
11. Schmidt A, Beyna T, Schumacher B, et al. Colonoscopic full-thickness resection using an over-the-scope device: A prospective multicentre study in various indications. Gut 2018; 67(7): 1280–1289.
https://doi.org/10.1136/gutjnl-2016-313677
12. Kuellmer A, Mueller J, Caca K, et al. Endoscopic full-thickness resection for early colorectal cancer. Gastrointest Endosc 2019; 89(6): 1180–1189.
https://doi.org/10.1016/j.gie.2018.12.025
13. Wu ZW, Ding CH, Song YD, Cui ZC, Bi XQ, Cheng B. Colon Sparing Endoscopic Full-Thickness Resection for Advanced Colorectal Lesions: Is It Time for Global Adoption? Front Oncol 2022; 12: 967100.
https://doi.org/10.3389/fonc.2022.967100
14. Dolan RD, Bazarbashi AN, McCarty TR, Thompson CC, Aihara H. Endoscopic full-thickness resection of colorectal lesions: a systematic review and meta-analysis. Gastrointest Endosc 2022; 95(2): 216-224.e18.
https://doi.org/10.1016/j.gie.2021.09.039
15. Ferlitsch M, Hassan C, Bisschops R, et al. Colorectal polypectomy and endoscopic mucosal resection: European Society of Gastrointestinal Endoscopy (ESGE) Guideline – Update 2024. Endoscopy. Published online 2024. https://doi.org/10.1055/a-2304-3219
16. Zwager LW, Mueller J, Stritzke B, et al. Adverse events of endoscopic full-thickness resection: results from the German and Dutch nationwide colorectal FTRD registry. Gastrointest Endosc 2023; 97(4): 780-789.e4.
https://doi.org/10.1016/j.gie.2022.11.005
17. Bauder M, Schmidt A, Caca K. Endoscopic full-thickness resection of duodenal lesions – A retrospective analysis of 20 FTRD cases. United European Gastroenterol J 2018; 6(7): 1015–1021.
https://doi.org/10.1177/2050640618773517
18. Fakhoury B, Alabdul Razzak I, Morin R, Krishnan S, Mahmood S. Combined endoscopic mucosal resection and full-thickness resection for large colorectal polyps: a systematic review and meta-analysis. Scand J Gastroenterol 2024 Jul; 59(7): 798–807.
https://doi.org/10.1080/00365521.2024.2349641
19. Meier B, Elsayed I, Seitz N, Wannhoff A, Caca K. Efficacy and safety of combined EMR and endoscopic full-thickness resection (hybrid EFTR) for large non-lifting colorectal adenomas. Gastrointest Endosc 2023; 98(3): 405–411. https://doi.org/10.1016/j.gie.2023.03.020
20. Gyökeres T, Farkas T, Virányi Z, Palatka K, Horváth M, Hritz I, et al. Endoscopic full thickness resection in GI tract – Hungarian experiences, the first 36 cases, Central European Journal of Gastroenterology and Hepatology, 2024; 10(Suppl 1): 93.
21. Dellatore P, Bhagat V, Kahaleh M. Endoscopic full thickness resection versus submucosal tunneling endoscopic resection for removal of submucosal tumors: A review article. Transl Gastroenterol Hepatol 2019; 4(June).
https://doi.org/10.21037/tgh.2019.05.03
