Reviews
The importance of sarcopenia and malnutritio in chronic liver diseases
Summary
A common complication of liver cirrhosis is malnutrition or malnutritio, which is associated with the progression of liver failure and a higher rate of complications of liver damage, including infections, hepatic encephalopathy, and ascites. Malnutrition and sarcopenia can worsen the prognosis of patients with cirrhosis hepatis and reduce their survival. Therefore, nutritional monitoring and therapeutic intervention are crucial in patients with chronic liver disease.
A májcirrózis gyakori szövődménye az alultápláltság vagy a malnutríció, amely a májelégtelenség előrehaladtával és a májkárosodás szövődményeinek magasabb arányával jár, beleértve a fertőzéseket, a hepatikus encephalopathiát és az ascitest. Az alultápláltság és a sarcopenia ronthatja a májzsugorodásban szenvedő betegek prognózisát, és csökkentheti a túlélésüket. A táplálkozás nyomon követése és a terápiás beavatkozás ezért kulcsfontosságú a krónikus májbetegségben szenvedők esetében.
Terminológia és definíciók
A malnutríció egy táplálkozással összefüggő rendellenesség, amely a táplálék bevitelének vagy felvételének hiányából ered, és a testösszetétel megváltozásához vezet: csökken a zsírtartalom, a zsírmentes testtömeg, illetve a sejtek tömege. Mindez csökkenti a fizikai és a mentális funkciókat, valamint rontja a betegségek klinikai kimenetelét. A sarcopenia során az izomtömeg és az izomfunkció általános csökkenése lép fel az öregedés (elsődleges sarcopenia), illetve akut vagy krónikus betegség (másodlagos sarcopenia) miatt. Az alultápláltság gyakran jelenik meg a májcirrózisos betegeknél. Az orvosi szaknyelvben a törékenység a funkcionális, a kognitív és a fiziológiai tartalékok elvesztését jelenti, ami sérülékeny állapothoz vezet. A törékenység a táplálkozással összefüggő rendellenességek egyik formájának tekintendő. Az immuntáplálás során speciális tápanyagokat használnak az immunrendszer működésének modulálására az egészségi állapot javítása céljából (nem feltétlenül alultápláltság esetén). Ilyen speciális tápanyagok például az omega-3 zsírsavak, az arginin, a glutamin és a nukleotidok. A kondícióvesztés az izomfunkciós kapacitás romlását jelenti, amely mozdulatlanság és krónikus legyengítő betegség miatt alakul ki (3).
A malnutríció előfordulása
A malnutríció előfordulási gyakorisága alábecsült. Egy felmérés során német gasztroenterológusok a malnutríció előfordulási gyakoriságát a cirrózisos betegeknél a valós 50–60%-hoz képest 23%-nak vélték. Az egyszerű, betegágy mellett alkalmazható diagnosztikai módszereket nem ismerték széles körben (1).
Egy Ausztráliában végzett retrospektív vizsgálat során 24 hónap alatt 231 cirrózisos beteget vizsgáltak, és a betegek 56%-nál észleltek malnutríciót. A kalória- (p=0,0003) és a proteinbevitel (p=0,0003) szignifikánsan alacsonyabb volt a malnutríciós betegeknél. A malnutríciós csoport 16%-a részesült enterális táplálásban a hospitalizáció alatt, és csak 8%-uk kapott folyamatos dietetikai ellátást a hospitalizáció alatt és útmutatót a távozáskor. Az összmortalitás 51%-os volt, és szignifikánsan magasabbnak bizonyult a malnutríciós csoportban, mint azoknál, akik nem voltak alultápláltak (HR=5,29; 95% CI: 2,31–12,1; p <0,001). Arra a megállapításra jutottak, hogy a cirrózisos betegek táplálása inadekvát, továbbá a részletes tápláltsági felmérés kiemelt jelentőségű (2).
Az alultápláltság progressziója együtt jár a májelégtelenséggel. Az alultápláltság a kompenzált cirrózisban szenvedő betegeknél kevésbé nyilvánvaló, de a dekompenzált cirrózis esetén már könnyen felismerhető. A kompenzált cirrózisban szenvedők 20%-ánál, a dekompenzált cirrózisban szenvedők több mint 50%-ánál jelentettek malnutríciót. Az izom- és a zsírszövet is csökkenhet; nők esetében gyakrabban a zsírszövet csökken, míg férfiak esetében az izomszövet csökken gyorsabban. Amint a klinikai irányelvek is részletezik, malnutríció és sarcopenia esetén magasabb a májcirrózis szövődményeinek aránya (infekciók, hepatikus encephalopathia, ascites), ami rontja az érintett betegek túlélését. A malnutríció és a sarcopenia felismeréséhez használható egyszerű, betegágy mellett alkalmazható diagnosztikai módszerek nem ismertek széles körben, illetve a napi fehérje- és energiabevitelre vonatkozó ajánlások megfelelő ismeretének hiánya is igazolódott (1, 3).
A malnutríció szűrése
A tápláltsági állapot felismerésére alkalmas módszerek közül a következők a legfontosabbak: az antropometriai vizsgálatok (testtömeg, testtömegindex [normál BMI: 15,5–24,9 kg/m2], bőrredővastagság [a bicepsz, a tricepsz, a subscapularis és a suprailiacalis izom feletti bőrredő vastagságából], derékkörfogat [férfiak: 94 cm, nők: 80 cm felett fokozott kockázat]), a marokerőpróba (a statikus izomerő mérésére) és a biokémiai módszerek (szérumalbumin, szérumösszfehérje, szérumkoleszterin, szérumtriglicerid, transzferrin, CRP).
Ezenkívül fontos a tápláltsági állapotot mérő tesztek ismerete is (1. táblázat).
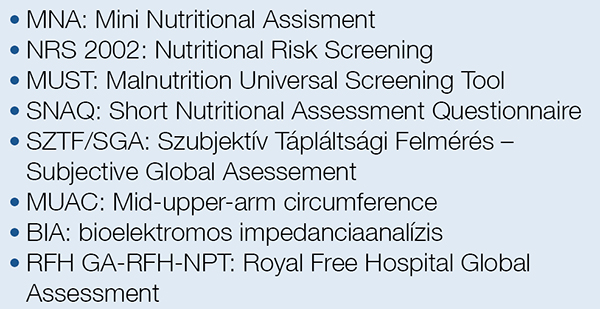
Az MNA (Mini Nutritional Assessment) egy négy részből álló teszt: antropometriai, általános, táplálkozási és szubjektív megítéléssel kapcsolatos kérdéseket tartalmaz. A teljes MNA kitöltése kevesebb mint tizenöt percet igényel, és meghatározható vele, hogy a beteg alultáplált, alultápláltság szempontjából veszélyeztetett, vagy jól táplált. A klinikai állapothoz viszonyított szenzitivitása 95%, specificitása 98%, pozitív prediktív értéke 97%. Az ESPEN ajánlása szerint az MNA az idős népesség körében használandó teszt.
Az NRS2002 (Nutritional Risk Screening) hasonló kritériumokat tartalmaz, mint a MUST (Malnutrition Universal Screening Tool), de értékeli a betegség súlyosságát is, amely a tápanyagszükséglet-növekedés oka. Az ESPEN irányelvei szerint kórházban az NRS2002 a kiemelten választandó módszer. Előnye, hogy nem feltétlenül kell
BMI-t számolni, elegendő a fogyás mértéke, ám a betegség súlyosságának megítélése szubjektív. A módszer könnyű alkalmazhatóságát jelzi, hogy egy hétszázötven, újonnan felvett beteget magában foglaló vizsgálatban a betegek 99%-át sikerült szűrni az NRS2002-vel. Fontos kiemelni, hogy az NRS2002 azokat szűri, akik valószínűleg profitálni fognak a táplálásterápiából, és nem kifejezetten magát az alultápláltságot.
A SNAQ (Short Nutritional Assessment Questionnaire) szintén egy négy kérdésből álló teszt; könnyen alkalmazható szűrőmódszer, amelyet ápolók általi kitöltésre szántak.
A három leginkább meghatározó kérdés:
- Fogyott-e a saját akaratán kívül?
- Rosszabb volt-e az étvágya az utóbbi hónapban?
- Részesült-e kiegészítő táplálásban az utóbbi hónapban?
A fogyással kapcsolatos kérdés pontozása a fogyás mértékétől függ; szenzitivitása >75%-os, specificitása 83%-os. A végeredmény függvényében kezelési tervet is nyújt. A javasolt kezelési terv alkalmazása további 600 kcal és 12 g fehérje felvételét jelentette. A módszerrel kiszűrt alultáplált betegek hamarabb jutottak dietetikusi segítséghez, mint a normál kórházi eljárásrenden keresztül.
Az MST (Malnutrition Screening Tool) egy három kérdésből álló módszer, amely alapjaiban hasonló az SNAQ-hoz. Az akaratlan fogyás és a kevesebb étel elfogyasztása volt a legspecifikusabb ([92,5/83,1]%) és legszenzitívebb ([86,6/98,4]%) kérdés. A fogyás mértékét is megtartották a pontozást szenzitívebbé tevő kérdésként. A kérdőív pozitív prediktív értéke 98,4%, negatív prediktív értéke pedig 72,7% volt. A kérdőívet kitöltők között nagyon jó egyezési mutatókat kaptak. Az MST-vel alultápláltnak értékelt betegek ápolási ideje szignifikánsan hosszabb volt, mint a jól táplált betegeké. A módszer kidolgozói a kórházi felvételkor javasolják a használatát, és a rizikós betegek esetében hetente javasolt a szűrés megismétlése. Az SGT (Subjective Global Assessment) néven ismert tesztet az 1980-as évek közepén, illetve végén az Egyesült Államokban dolgozták ki az anamnézist és a fizikális vizsgálatot alapul véve. Ezek alapján e módszer a betegeket súlyosan alultáplált, mérsékelten alultáplált, feltételezetten alultáplált és jól táplált kategóriába sorolja be.
Az RFH GA (Royal Free Hospital Global Assessment), illetve a módosított, specifikusan cirrózis esetén használt RFH-NPT (Royal Free Hospital Nutrition Proiritizing Tool) során a BMI és a középkarizom-körfogat (MAMC) méréseit kombinálták algoritmikus konstrukcióban a táplálékfelvételre vonatkozó adatokkal. Tartalmazza az alkoholos hepatitis változóit, a folyadékvisszatartást, az ascitest, a táplálékbevitelre gyakorolt hatást, a BMI-t, a nem tervezett fogyást és a csökkent táplálékfelvételt. Értékelése lehet: megfelelően táplált, mérsékelten, illetve súlyosan alultáplált.
Funkcionális vizsgálatok
Számos tanulmány kimutatta, hogy az izomerő gyorsabban romlik, mint az izomtömeg, ezért érzékenyebb indikátora lehet az „izom egészségének”. A cirrózisban szenvedő betegeknél a funkcionális mérések (pl. kézfogás, 6 perces séta, fizikai gyengeség, oxigénszaturáció) összefüggenek a dekompenzáció mértékével. Ezeket a méréseket ki kell egészíteni a testösszetétel értékelésével annak érdekében, hogy jobban megértsük az izom metabolikus integritását és működőképességét (9). A kéz szorítóereje a test izomerejét jól jellemző érték, de fontos, hogy az erősebb (domináns) kézen kell mérni. Egy erre szolgáló eszközzel három egymás utáni mérés eredményét kell rögzíteni, majd azok átlagát venni. Az esendőség-szindróma („frailty syndrome”) elemeinek vizsgálata szintén alkalmazható a cirrózisos betegek tápláltsági állapotának felmérése során; ezek az elemek a következők: a beteg különféle stresszorokra mutatott fokozott érzékenysége, csökkent élettani tartalékok és a funkcionális állapot hiányosságai. Lai és munkatársai egy új esendőségi indexet (ún. liver frailty index) dolgoztak ki a cirrózisos betegek számára, amelyről bebizonyosodott, hogy jelentősen javította a mortalitás előrejelzését májtranszplantációs várólistán lévő betegek körében, akár a szubjektív klinikai megítéléshez, akár a betegség súlyosságát jelző MELD-Na-pontszámhoz képest. A liver frailty index a beteg nemét figyelembe véve 3 teljesítményalapú funkcionális tesztből áll:
- székről felállás 5 alkalommal,
- egyensúlytartási képességet mérő feladat és
- a domináns kéz szorítóerejének mérése 3 alkalommal. Egy online kalkulátor segítségével könnyen értékelhető (https://liverfrailtyindex. ucsf.edu) (4).
Az EASL 2019-es irányelve foglalja össze a tápláltság szűrését és értékelését májcirrózisos betegeknél, illetve az ehhez kapcsolódó ajánlásait (1. ábra) (3).
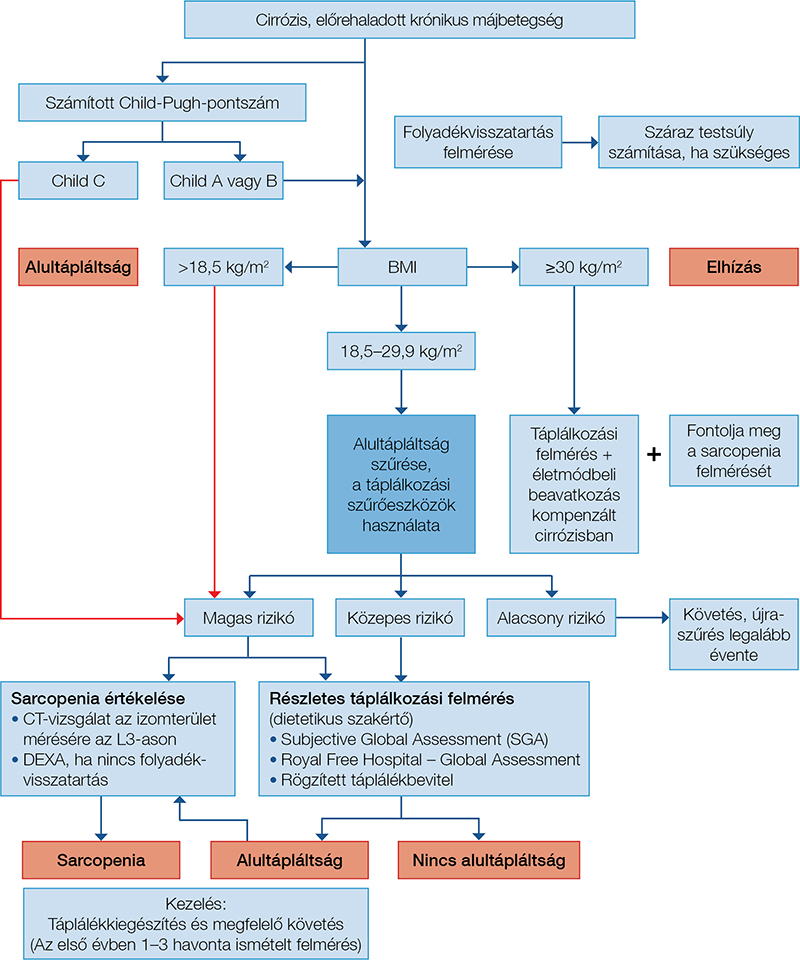
Ajánlások
Előrehaladott májcirrózisban, protein-energia malnutríció esetén gyakoribb a szövődmények előfordulása, hosszabb a hospitalizációs idő, fokozottabb a mortalitás, illetve magasabbak az ellátási költségek. Az ESPEN 2020-as ajánlása foglalja össze májbetegségek esetén a klinikai táplálási irányelveket. Fontos kiemelni a refeeding-szindrómát, amely során legalább 5 napon keresztül éhezett a páciens, majd agresszív feltáplálásba kezdünk (enterális vagy parenterális táplálásba). Az akut neurológiai elváltozások alapján a szindróma fennáll, ha legalább egy tünet jelen van az alábbiak közül: apátia, dezorientált viselkedés, nystagmus, szemizombénulás, szemmozgási zavarok, ataxia, rövid távú memória romlása confabulatióval. Ezért a táplálás első két napján a tápanyagmennyiség maximum 50%-a vihető be.
Az enterális és a parenterális táplálás szerepe
Májcirrózisban szenvedő betegeknél az SGA vagy más antropometriai módszer használata javasolt a malnutríció által veszélyeztetett betegek identifikálására.
Idült májbetegségben, nem sürgős állapot esetén napi 35–40 kcal/ideális testsúlykilogramm energia, és napi 1,2–1,5 g/ideális testsúlykilogramm fehérje bevitele javasolt. Az ajánlott napi rostbevitelt 25–45 grammban állapították meg. Továbbá napi többszöri, kis étkezés, zöldségekben és tejtermékekben gazdag, valamint vörös húsokban szegény étrend javasolt.
A parenterális kezelést akkor kell elindítani a középsúlyos/súlyos malnutrícióban szenvedő cirrózisos betegnél, ha nem kielégítő az orális vagy az enterális táplálás.
2–3 g/kg/nap iv. glükóz adása szükséges, ha több mint 12 órája nem tud táplálkozni a beteg. Parenterális kezelés megkezdése javasolt, ha több mint 72 órája tart az éhezés. Parenterális táplálást kell indítani akkor is, ha a légutak nem szabadak és hepatikus encephalopathia áll fenn, valamint köhögés és lassú reflexek fordulnak elő. A cirrózisos betegeknél korai posztoperatív (kiegészítő) parenterális táplálást kell kezdeni a műtét után, ha a beteget nem lehet megfelelően táplálni orális/enterális úton. Cirrózisos betegeknél az energiaigény az alapanyagigény (REE) 1,3-szorosa. Fontos, hogy adjunk glükózt a nem fehérje jellegű energiaigény 50–60%-nak fedezésére. Hyperglikaemia esetén csökkentsük a glükózt tartalmazó infúzió sebességét 2–3 g/ttkg/nap dózisra, és alkalmazzunk intravénás inzulint. Használjunk n-6 telítetlen zsírsavat tartalmazó lipidemulziót, amely fedezi az energiaigény 40–50%-át. A betegeknek 1,2–1,5 g/ttkg/nap aminosav adása javasolt, illetve III. vagy IV. stádiumú encephalopathiában a BCAA (elágazó szénláncú aminosav) gazdag és kevés AAA (aromás aminosav: metionin és triptofán) tartalmazó táplálékpótlás ajánlott. Májcirrózisban a vízben oldódó és zsírban oldódó vitaminokat, valamint az ásványi anyagokat és a nyomelemeket naponta kell pótolni a parenterális táplálás kezdetétől. Alkoholos cirrózisban glükózinfúzió beadása előtt B1-vitamin adása szükséges a Wernicke-encephalopathia kockázatának csökkentése érdekében. Végül fontos monitorozni a vércukorszintet, illetve figyelni a foszfát-, a kálium- és magnéziumszinteket a malnutríciós betegek újratáplálásakor (5–7). Cirrózisos betegeknél magas prevalenciában várható a malnutríció, a proteindepléció és a nyomelemhiány (8).
Az ESPEN legfontosabb ajánlásait a májcirrózisos betegek részére a 2. táblázat tartalmazza (5).

Összegzés
A tápláltsági állapot és a májcirrózis kimenetele közötti kapcsolat indokolttá teszi, hogy azt megfelelő módon felmérjük, és időben megkezdjük a malnutríció kezelését, vagyis a táplálásterápiát. Idült májbetegeknél eredményesebb az SGA, az antropometriai módszerek használata, illetve a többféle teszt kombinálása. Rizikóbecslésre a cirrózisos betegeknél az RFH-NPT a választandó teszt. Az ESPEN 2009-es és 2020-as, az EASL 2019-es, valamint az AASD 2018-as ajánlásainak megfelelően a malnutríció és a májbetegség stádiumától függően az enterális vagy a parenterális táplálást időben kell indítani. Az idült májbetegek gondozásának fontos része a tápláltsági állapot rendszeres felmérése és a dietetikai követés. Child B és Child C stádiumban a malnutríció magas előfordulási aránya miatt a táplálásterápia automatikus megkezdése lenne kívánatos, a Child A stádiumú betegeknél pedig alapos szűrővizsgálat szükséges, hogy a táplálásterápia megfelelő időben elindulhasson.nek előrejelzésére, illetve hogyan lehet optimalizálni a terápiás beavatkozásokat a betegek életminőségének javítása érdekében.
Irodalom
1. Gundling F, et al. How close do gastroneterologists follow specific guidelines for nutrition recommendations in liver cirrhosis? A survey of current practice. Eur J Gastroenterol and Hepatol 2009; 21:(7) 756–61.
https://doi.org/10.1097/MEG.0b013e328311f281
2. Huynh DK, et al. Nutritional care in hospitalized patients with chronic liver disease. World J Gastroeneterol 2015; 21(45): 12835–12842.
3. European Association for the Study of the Liver. EASL Clinical Practice Guidelines on nutrition in chronic liver disease. J Hepatol 2019; 70(1): 172–193. https://doi.org/10.1016/j.jhep.2018.06.024
4. Vitális Zs, Balogh B, Villám B, Papp M. A tápláltsági állapot szűrésének és értékelésének gyakorlati megközelítése májcirrhosisos betegekben. Magy Belorv Arch 2020; 73(6): 277–293.
5. Bischof SC, et al. ESPEN practical guideline: Clinical nutrition in liver disease. Clin Nutr 2020; 39(12): 3533–3562.
https://doi.org/10.1016/j.clnu.2020.09.001
6. Sam J, Nguyen CG. Protein-calorie malnutrition as a prognostic indicator of mortality among patients hospitalized with cirrhosis and portal hypertension. Liver Int 2009; 29(9): 1396–402.
https://doi.org/10.1111/j.1478-3231.2009.02077.x
7. Plauth M, et al. ESPEN Guidelines on Parenteral Nutrition: Hepatology. Clin Nutr 2009; 28(4): 436–44. https://doi.org/10.1016/j.clnu.2009.04.019
8. Plauth M, et al. ESPEN guideline on clinical nutrition in liver disease. Clin Nutr 2019; 38(2): 485–521. https://doi.org/10.1016/j.clnu.2018.12.022
9. Raman T, et al. A Practical Approach to Nutritional Screening and Assessment in Cirrhosis. Hepatology 2017; 65(3): 1044–1057.
https://doi.org/10.1002/hep.29003
