Original publication
Groove pancreatitis: diagnostic challenges and clinical experiences
Summary
Groove pancreatitis (GP) is a rare paraduodenal form of chronic pancreatitis that often mimics pancreatic head malignancies or autoimmune pancreatitis based on clinical and imaging findings. In this retrospective study, we analyzed the data of ten patients (6 males, 4 females; mean age: 54 ± 3.9 years) treated at the Gastroenterology Center of the University of Szeged between 2016 and 2025. Sixty percent of the patients reported regular alcohol consumption (mean: 9.3 standard drinks/day) and an equal proportion had a history of smoking (mean: 24.6 pack-years). The leading symptoms were epigastric pain (81.8%) and vomiting (72.7%), while jaundice was observed in one case (9.1%). Laboratory tests revealed elevated lipase levels in 87.5% of cases, amylase elevation in 66.7%, increased CRP in 66.7%, and leukocytosis in 55.6%. Tumor markers (CEA, CA 19-9) remained within normal ranges in all patients. The median length of hospital stay was 14.5 days (IQR: 28 days). Conservative treatment led to remission in 2 cases, while 5 patients required endoscopic interventions (ERCP with debris extraction, stenting, EUS-guided drainage). Surgical management became necessary in 3 patients (including Frey procedure, abscess drainage, and biliary reconstruction). Complications occurred in 2 cases but they were successfully managed by endoscopic means. Our results confirm that the diagnosis of GP requires a multidisciplinary approach, careful differential diagnostic evaluation, and individualized therapeutic strategies to avoid unnecessary surgical procedures.
Összefoglaló
A groove pancreatitis (GP) a krónikus pancreatitis ritka, paraduodenalis formája, amely klinikailag és a képalkotó vizsgálatok alapján gyakran a pancreasfejet érintő malignitást vagy autoimmun pancreatitist utánoz. Retrospektív vizsgálatunkban 2016 és 2025 között tíz beteg (6 férfi, 4 nő, átlagéletkor:
54 ± 3,9 év) adatait elemeztük a Szegedi Tudományegyetem Gasztroenterológiai Centrumának beteganyagából. A betegek 60%-a rendszeresen fogyasztott alkoholt (átlagosan 9,3 standard ital/nap), és ugyanilyen arányuk dohányzott (átlag: 24,6 dobozév). A vezető tünetek az epigastrialis fájdalom (81,8%) és a hányás (72,7%) voltak; icterust 1 esetben (9,1%) észleltünk. A laborvizsgálatok során kóros lipázszint 87,5%-ban, amilázemelkedés 66,7%-ban, CRP-emelkedés 66,7%-ban, leukocytosis
55,6%-ban fordult elő. Tumormarker-emelkedést (CEA, CA 19-9) egyik esetben sem találtunk. A kórházi tartózkodás medián időtartama 14,5 nap volt (IQR: 28 nap). A konzervatív kezelés 2 esetben vezetett remisszióhoz, 5 betegnél endoszkópos intervenció (ERCP, stentelés, EUS-vezérelt drenázs) eredményezett javulást, míg 3 esetben sebészi beavatkozás vált szükségessé (pl. Frey-műtét, tályogfeltárás, epeúti rekonstrukció). Szövődmény 2 esetben alakult ki, amelyek endoszkópos úton kontrollálhatók voltak. Eredményeink megerősítik, hogy a GP diagnózisa multidiszciplináris megközelítést, gondos differenciáldiagnosztikai mérlegelést és individualizált terápiás stratégiát igényel a felesleges sebészi beavatkozások elkerülése érdekében.
Bevezetés
Definíció és klinikai megjelenési formák
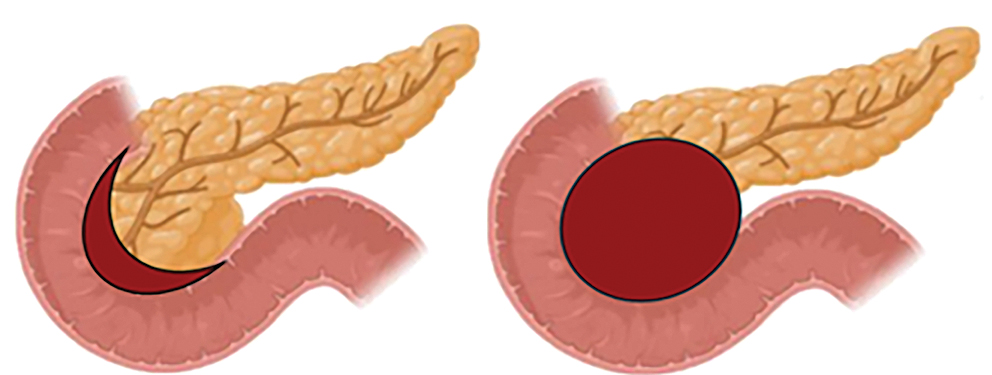
A groove pancreatitis (GP) a krónikus pancreatitis egy ritka, anatómiailag lokalizált formája, amely a pancreasfej, a duodenum és a közös epevezeték közötti területet, az ún. „groove” (vályú) régiót érinti (1. ábra). A kórképet először Becker és Mischke írták le 1973-ban, fibrotikus pszeudotumor formájában ezen anatómiai területen (1). Két fő morfológiai megjelenés különíthető el: a pure („tiszta”) típus, amely során a gyulladás kizárólag a groove régióra korlátozódik, és a szegmentális típus, ahol a gyulladás a pancreasfejet is érinti (2). A krónikus pancreatitis ezen paraduodenalis formája elsősorban a 60 év feletti, alkoholt rendszeresen fogyasztó férfiaknál jelentkezik (3, 4).
Patomechanizmus
A GP patogenezise jelenleg nem teljesen tisztázott, ugyanakkor több, egymással átfedő mechanizmust is feltételeznek, amelyek hozzájárulhatnak a betegség kialakulásához. Az egyik leginkább elfogadott elmélet szerint a fő problémát a papilla duodeni minor bármilyen etiológiájú obstrukciója jelenti: ennek következtében a pancreasnedv nem képes kiürülni, és a groove régióban reked, ahol gyulladást indít el (5). Bizonyos esetekben észlelhető a duodenumban heterotopiás pancreasszövet (6), amely megfelelő drenázs hiányában cystosus átalakuláson megy keresztül, majd benne gyulladás alakul ki. Továbbá ezen érzékeny ectopiás szövet bármilyen lokális, krónikus irritáció hatására képes proliferálni, cisztás eltéréseket létrehozni, illetve begyulladni, amely klinikailag GP-nek imponál. Etiológiai szempontból az alkohol és a dohányzás patogenetikai szerepe szintén jelentős: krónikus alkoholizmus során a pancreasnedv viszkozitása fokozódik (7), növekszik a proteolitikus aktivitás, ami a ductalis rendszer mikroszkopikus elzáródásához, intraparenchymás nyomásnövekedéshez és gyulladáshoz vezet. A szekrétum pangását okozhatja a Brunner-mirigyek hyperplasiája is, illetve bármilyen duodenalis motilitászavar is hozzájárulhat a groove régiót érintő nyomásfokozódáshoz, ezáltal a gyulladáshoz. A lokálisan kialakuló fibrosis, myofibroblast-proliferáció szűkíti a duodenumot, növeli a groove struktúrák rigiditását, előrehaladott állapotban még a pancreasfejet is deformálhatja; így a betegség progrediál, circulus vitiosus alakulhat ki (8).
Metodika
Vizsgált populáció, etikai vonatkozások
Retrospektív, obszervációs vizsgálatunkba 2016. január elseje és 2025. január elseje között kezelt 10 beteget vontunk be a Szegedi Tudományegyetem Belgyógyászati Klinika Gasztroenterológiai Centrumának betegállományából. A kizárási kritériumok a következők voltak:
- 18 év alatti életkor;
- groove pancreatitis hiánya;
- az egyénről nem érhető el teljeskörű betegdokumentáció;
- az egyén állapotát nem a groove pancreatitis határozta meg (pl.: disszeminált tumoros, rendkívül rossz általános állapotban lévő beteg).
Adatgyűjtés
A vizsgálathoz szükséges adatokat a kórházi Medsol-adatbázisból gyűjtöttük össze, amely magában foglalta a betegek nemét, életkorát, a kórházi tartózkodás idejét, az utánkövetés hosszát és az élvezeti szerek használatát. Az anamnesztikus adatok közül a láz, a hasfájás, a fogyás, a hányás és az icterus került vizsgálatunk fókuszába. Elemeztük továbbá a konzervatív, az endoszkópos és a sebészi terápia sikerességét, illetve a szövődmények kialakulását.
Statisztika
Az adatokat a kórházi elektronikus dokumentációs rendszerből nyertük, és retrospektív módon elemeztük. A változók eloszlását Shapiro–Wilk-próbával vizsgáltuk. Normál eloszlást mutató adatok esetén az eredményeket átlag ± standard hiba (standard error of the mean, SEM) formájában adtuk meg, míg nem normál eloszlás esetén medián és interkvartilis tartományt (IQR) közöltünk. Kategorikus változók esetén abszolút esetszámot és százalékos arányt tüntettünk fel. Az adatfeldolgozást Microsoft Excel 365 és IBM SPSS Statistics 28 szoftverekkel végeztük.
Eredmények
Általános és anamnesztikus adatok jellemzése
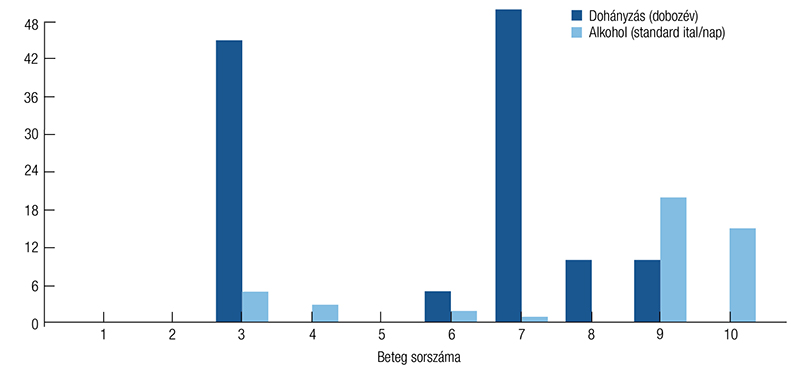
A betegek átlagéletkora 54 ± 3,9 év volt, a kórházban töltött napok számának mediánja 14,5 nap (IQR: 28 nap). A betegek közt hat férfi és 4 nő volt. Hat beteg fogyasztott rendszeresen alkoholt, és azonos hányaduk dohányzott. Az alkoholt fogyasztó páciensek átlagosan napi 9,3 standard ital (1 standard ital = 10 g tiszta etanolt tartalmazó ital) mennyiséget fogyasztottak, míg a dohányosok átlagos dohányzási előzménye 24,6 doboz/évnek adódott (2. ábra). A tápláltsági állapotot jellemző BMI kategóriákat a Centers for Disease Control and Prevention (CDC) ajánlásai szerint határoztuk meg: ennek alapján 4 beteg az obez, 5 a normál, 1 pedig a cachexiás tápláltsági tartományba esett. Láz csupán egy esetben lépett fel, további két esetben hőemelkedés jelent meg, ezenfelül két beteg jelzett hidegrázást. Hasi fájdalom 81,8%-ban jelentkezett; hányás 72,7%-ban; icterus 9,1%-ban; mindezek ellenére fogyásról egy beteg sem számolt be. A groove pancreatitis megjelenési formája 2 esetben pure volt, a többi személynél szegmentális. A vizsgált populáció felénél történt fájdalomszint-felmérés a felvétel időpontjában, a vizuális analóg skála (VAS) alkalmazásával; a betegek átlagosan 8-as értéket jelöltek meg.
Laboradatok közlése
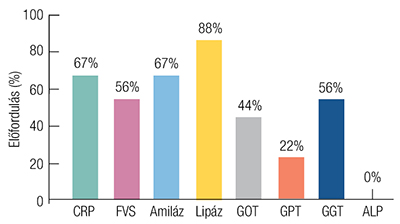
A teljes kórházi tartózkodás idején a vizsgálati populáció 54,5%-ánál igazolódott dyslipidaemia; emelkedett amilázszint az esetek 66,67%-ában, kórosan magas lipázérték 87,5%-ban fordult elő. A C-reaktív protein (CRP) szintje a betegek 66,67%-ánál haladta meg a fiziológiás határértéket. Emelkedett leukocytaszámot az esetek 55,56%-ában észleltünk. A májfunkciós paraméterek közül a γ-glutamil-transzferáz (GGT) 55,56%-ban, a glutamát-oxálacetát-transzamináz (GOT) 44,44%-ban, míg a glutamát-piruvát-transzamináz (GPT) két esetben mutatott a normálértéket meghaladó szintet (3. ábra). Egyik vizsgált beteg esetében sem volt kimutatható emelkedett tumormarkerszint, a CA 19-9 és a CEA értékei valamennyi esetben a referenciatartományon belül maradtak. A szérumból mért albumin, kalcium, lymphocyta- és neutrofilszám, valamint az alkalikus foszfatáz és a glükóz szintje szintén normálisnak bizonyult.
Radiológiai dokumentációk alapján jellemző eltérések
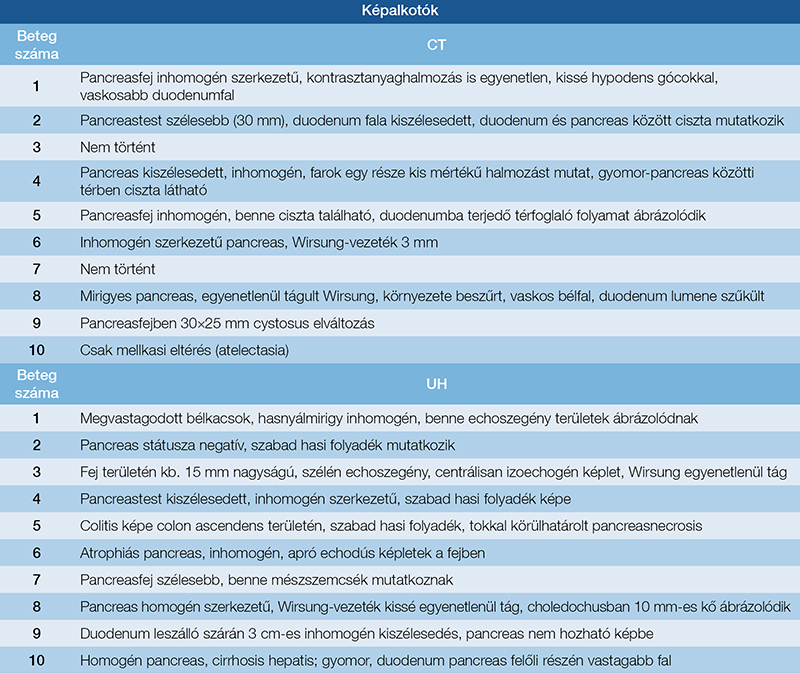
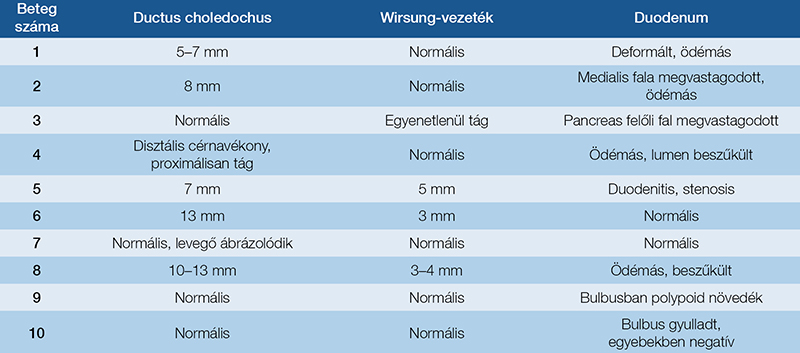
MRI-vizsgálat csupán egy esetben állt rendelkezésre (4. ábra), amely során a pancreas 10–13 mm vastagságúnak imponált, a Wirsung-vezeték teljes hosszában tágult, a duodenum falának megvastagodása pedig szintén megfigyelhető volt. Vizsgálataink során az ultrahang (UH) és a komputertomográfia (CT) bizonyultak a leginformatívabb képalkotó eljárásoknak (1. táblázat); ezek szolgáltatták a legtöbb releváns morfológiai információt a diagnosztikai döntéshozatalhoz (5. és 6. ábra).
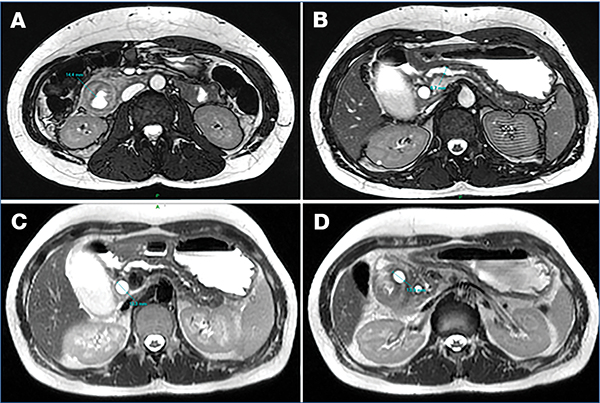
(A) A duodenum leszálló szárán egyenetlen falmegvastagodás figyelhető meg (14,4 mm); (B) A Wirsung-vezeték a fej-test határon 6,7 mm, kaliberingadozással végig tág; (C) Tágult ductus choledochus (13 mm); (D) Cystosus 13,9 mm átmérőjű képlet a pancreas medialis falán, amely a duodenum felé boltosul
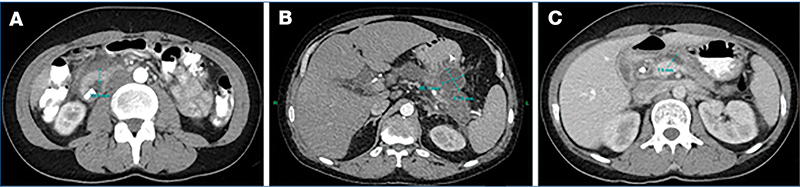
(A) Megvastagodott falú duodenum (12 mm); (B) A gyomor és a pancreas teste között elhelyezkedő ciszta (36×41mm); (C) Tágult Wirsung-vezeték (7 mm)
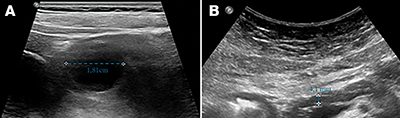
(A) A pancreastestben egy 18 mm nagyságú cystosus képlet látszik; (B) A Wirsung-vezeték egyenetlenül 4 mm tág
Különböző terápiás lehetőségek összevetése és a szövődmények kezelése
A konzervatív gyógyszeres terápia két esetben vezetett teljes klinikai remisszióhoz. A konzervatív kezelés részeként carentiát, parenterális táplálást, adekvát fájdalomcsillapítást, valamint empirikus antibiotikus terápiát alkalmaztak. A fennmaradó nyolc esetben a gyógyszeres kezelés önmagában nem eredményezett szignifikáns javulást, így endoszkópos intervenciók váltak szükségessé (2. táblázat).
Az endoszkópos kezelések öt esetben jártak terápiás sikerrel; több betegnél különböző típusú endoszkópos eljárás kombinációjára volt szükség. A terápiás eszköztárban szerepelt az endoszkópos retrográd kolangiopankreatográfia (ERCP) során végzett törmelékextrakció, ballonos epeúti dilatáció és stentimplantáció (7. ábra). Ezenfelül endoszkópos ultrahang (EUS) által vezérelt tályogdrenázs is történt.
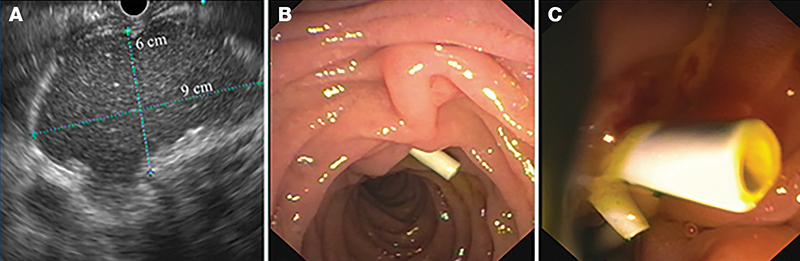
(A) A gyomor mögött 3 mm-es falú WON (60×90 mm); (B–C) Műanyag stentek a Vater-papillában
Három betegnél sebészi beavatkozás vált elkerülhetetlenné. Az egyik páciens ismétlődő recidív pancreatitises epizódokat követően kuratív célú Frey-műtéten esett át. Egy másik esetben endoszkóposan nem drenálható peripancreaticus tályogokat észleltünk, amelyeket sebészi feltárással sikeresen evakuáltak; a beteg ezután panaszmentessé vált. A harmadik betegnél az epeúti szűkület szekvenciális stentelése nem volt eredményes, ezért sebészi beavatkozásra került sor.
A terápiás beavatkozások után összesen két esetben észleltünk szövődményt. Az egyik beteg esetében choledochusszűkület következtében kialakult epepangás volt jelen, amelyet egy egyszerűen kivitelezett, 7 cm hosszúságú, 10 Fr méretű stent implantációjával hatékonyan szanáltunk. A második esetben az endoszkópos tályogdrenázst követően újabb ciszta képződött, azonban a későbbiekben végzett ismételt drenálást követően további recidíva nem lépett fel. Az alapbetegséggel vagy az alkalmazott terápiákkal összefüggésbe hozható egyéb szövődményt nem észleltünk egyik beteg esetében sem.
Diszkusszió
A groove pancreatitis diagnosztizálása továbbra is jelentős kihívást jelent a gasztroenterológiai és a radiológiai gyakorlatban, különösen annak fényében, hogy klinikailag és morfológiailag egyaránt utánozhatja a pancreasfej malignitásait (9). Vizsgálatunk retrospektív adatai megerősítik a korábbi szakirodalmi megfigyeléseket, miszerint a groove pancreatitis elsősorban középkorú, alkoholt és nikotint fogyasztó férfiakat érint (10), akiknél gyakran jelentkeznek nem specifikus gasztrointesztinális panaszok, így epigastrialis fájdalom, hányás, esetenként icterus. A differenciáldiagnosztika során a legnagyobb klinikai kihívást a pancreasfejet érintő adenocarcinomától, valamint az autoimmun pancreatitistől (AIP) való elkülönítés jelenti. A tünettan, a képalkotó eltérések és bizonyos esetekben még a szövettani minták is jelentős átfedést mutathatnak. A groove régióban megjelenő hypodens vagy hypointens elváltozás, a duodenum medialis falának megvastagodása, valamint a submucosalis ciszták irányíthatják a diagnózist GP felé, ugyanakkor ezek az eltérések utánozhatják a pancreasfeji adenocarcinomát is (11). A karcinómák gyakrabban érintik a Wirsung-vezetéket, valamint infiltrálhatják a vascularis struktúrákat (12), amelyek GP esetében nem jellemzők, így differenciáldiagnosztikai támpontot adhatnak. Az AIP elkülönítése további nehézséget jelenthet, különösen a fokális formában, amely szintén térfoglaló eltéréssel, pancreasfeji tömegdúsulással és epeúti szűkülettel járhat. AIP-ben azonban jellemző a diffúz pancreasmegnagyobbodás („kolbászpancreas”), a fő pancreasvezeték szűkülete vagy eltűnése, valamint a szérum IgG4-szintjének emelkedése (13). Emellett extrapancreaticus manifesztációk (mint a retroperitonealis fibrosis vagy az autoimmun cholangitis) szintén az AIP diagnózisát támogatják a GP-vel szemben (14). Kiemelendő, hogy bár a tumormarkerek (CEA, CA19-9) minden esetben a normális tartományban voltak, ez önmagában nem zárja ki a malignitás lehetőségét (15), ezért a differenciáldiagnózis során továbbra is kulcsfontosságú marad a képalkotók használata és az esetleges szövettani mintavétel (16). A CT-vizsgálat sok támpontot ad a helyes diagnózishoz (17), míg válogatott esetekben az EUH és az MR pontosíthatja a strukturális eltéréseket, különösen a duodenalis és cisztás komponensek azonosításában. Terápiás szempontból a kezelési stratégia elsősorban a tünetek súlyosságától, a szövődmények meglététől, valamint a malignitás kizárásának sikerességétől függ. Nem komplikált esetekben a konzervatív kezelés (zsírszegény diéta, alkohol- és dohányzásmegvonás, kis volumenű étkezések, analgetikumok, enzimpótlás, protonpumpa-gátlók és szükség esetén nasojejunalis táplálás) elegendő lehet (18). Amennyiben szövődmények alakulnak ki, endoszkópos intervenciók (például epe- és pancreasvezeték stentelése, a ciszta drenázsa vagy a duodenumszűkület ballonos tágítása) nyújthatnak hatékony terápiás megoldást (19). Terápiarezisztens esetekben vagy malignitás gyanúja esetén sebészi beavatkozásra lehet szükség, leggyakrabban pancreatoduodenectomiára (Whipple-műtét), de súlyos szűkületek esetén bypassműtétek is szóba jöhetnek (20). Az általunk tapasztalt kezelési eredmények rávilágítanak arra, hogy bár a konzervatív terápia bizonyos esetekben elegendő, a betegek többsége invazív beavatkozást igényel, amelyek közül az endoszkópos eljárások egyre nagyobb teret nyernek (21). A szövődmények száma alacsony volt és minden esetben jól kontrollálható maradt.
Konklúzió
Összegzésként elmondható, hogy a groove pancreatitis ritka, de klinikailag és diagnosztikailag nagy kihívást jelentő kórkép, amelynek korai felismerése és megfelelő kezelése elengedhetetlen a felesleges sebészi beavatkozások elkerülése és a progresszió előrehaladásának csökkentése érdekében. Tanulmányunk megerősíti, hogy a diagnózis felállításához multidiszciplináris együttműködés, célzott képalkotó vizsgálatok és szövettani megerősítés is szükséges lehet. A terápia egyénre szabott megválasztása, a konzervatív, az endoszkópos és a sebészi lehetőségek megfelelő alkalmazása kulcsfontosságú a sikeres kimenetel érdekében. A GP pontosabb ismertsége és elkülönítése hozzájárulhat a krónikus pancreatitises és pancreastumor-gyanús esetek célzottabb ellátásához a jövőben.
Etikai engedélyek és támogatások
A vizsgálat a Szegedi Tudományegyetem Regionális Humán Biológiai Kutatásetikai Bizottsága jóváhagyásával történt (114/2023-SZTE RKEB). A projekt az EU “Horizon 2020” kutatási és innovációs programjából kapott finanszírozást a 739593. számú támogatási megállapodás keretében (BCN). A Kulturális és Innovációs Minisztérium egyetemi kutatói ösztöndíj programjának a nemzeti kutatási, fejlesztési és innovációs alapból finanszírozott szakmai támogatásával készült.
Irodalom
3. Tyler P Black, et al: Groove Pancreatitis: Four Cases from a Single Center and Brief Review of the Literature. ACG Case Rep J 2014; 1(3): 154–157. https://doi.org/10.14309/crj.2014.35
4. Gupta S, Jain V. Groove pancreatitis in a patient with recurrent abdominal pain and history of alcohol misuse. Consultant 2022; 62(8): e5–e7.
https://doi.org/10.25270/con.2021.10.00007
5. Alberto Herreros de Tejada, et al. Endoscopic and EUS features of groove pancreatitis masquerading as a pancreatic neoplasm. Gastrointest Endosc 2008; 68(4): 796–8. https://doi.org/10.1016/j.gie.2008.02.015
6. Maryam Rezvan, et al. Heterotopic Pancreas: Histopathologic Features, Imaging Findings, and Complications. Radiographics 2017; 37(2): 484–499. https://doi.org/10.1148/rg.2017160091
7. Irie H, et al. MRI of groove. J Comput Assist Tomogr 1998; 22(4):651–5. https://doi.org/10.1097/00004728-199807000-00027
8. Gloria Addeo, et al. Groove pancreatitis: a challenging imaging diagnosis. Gland Surg 2019; 8(Suppl 3): S178–S187.
https://doi.org/10.21037/gs.2019.04.06
9. Miller FH, Lopes Vendrami C, Hammond NA, Mittal PK, Nikolaidis P, Jawahar A. Pancreatic Cancer and Its Mimics. Radiographics 2023; 43(11): e230054. https://doi.org/10.1148/rg.230054
10. Dahiya DS, Shah YR, et al. Groove pancreatitis: From enigma to future directions—A comprehensive review. J Gastroenterol Hepatol 2024; 39(11): 2260–2271. https://doi.org/10.1111/jgh.16683
11. Berral Santana AM, Cedrún Sitges I. Groove pancreatitis and how to differentiate it from pancreatic adenocarcinoma. Radiologia (Engl Ed) 2023; 65(1): 81–88. https://doi.org/10.1016/j.rxeng.2021.07.005
12. Buchs NC, Chilcott M, Poletti PA, Buhler LH, Morel P. Vascular invasion in pancreatic cancer: Imaging modalities, preoperative diagnosis and surgical management. World J Gastroenterol 2010; 16(7): 818–831.
https://doi.org/10.3748/wjg.v16.i7.818
13. Vemulapalli V, Natha C, Thomas AS. Autoimmune pancreatitis: A review. J Clin Med 2025; 14(9): 3076.
https://doi.org/10.3390/jcm14093076
14. Fujimori N, Ito T, Igarashi H, Oono T, et al. Retroperitoneal fibrosis associated with immunoglobulin G4-related disease. World J Gastroenterol 2013; 19(1): 35–41. https://doi.org/10.3748/wjg.v19.i1.35
15. Haglund C, Kuusela P, Roberts PJ. Tumour markers in pancreatic cancer. Ann Chir Gynaecol 1989; 78(1): 41–53.
16. Okasha H, Wahba M. EUS in the diagnosis of rare groove pancreatitis masquerading as malignancy. Gastrointest Endosc 2020; 92(2): 427–428. https://doi.org/10.1016/j.gie.2020.02.030
17. Khalil RM, Gouda WA. CT findings of the commonly overlooked groove pancreatitis. Egypt J Radiol Nucl Med 2017; 48(4): 785–790.
https://doi.org/10.1016/j.ejrnm.2017.05.006
18. Thomas A, Dev AV, John A, John RA, et al. The effectiveness of a conservative approach in the management of groove pancreatitis. Indian J Gastroenterol 2025. Online ahead of print. https://doi.org/10.1007/s12664-024-01715-x
19. Ikemura M, Tomishima K, Ota H, Kabemura D, et al. A case of groove pancreatitis with duodenal stenosis successfully treated by endoscopic ultrasonography-guided pancreaticogastrostomy. DEN Open 2022; 3(1): e190. https://doi.org/10.1002/deo2.190
20. Ioannidis A, Menni A, Tzikos G, Ioannidou E, et al. Surgical management of groove pancreatitis: A case report. J Pers Med 2023; 13(4): 644. https://doi.org/10.3390/jpm13040644
21. Ukegjini K, Steiger K, Weigl S, Andreou A, et al. Systematic review on groove pancreatitis: management of a rare disease. BJS Open 2023; 7(5): zrad094. https://doi.org/10.1093/bjsopen/zrad094
