Reviews
Peculiarities of endoscopic examinations during incretin therapy in diabetic and obese patients
Summary
Drugs acting on incretins can cause side effects and endoscopic examinations may become necessary. An elective upper endoscopy should be performed after a longer than usual fasting period (16-18 vs 12 h). Gastric retention of solid or liquid food is frequently encountered meaning the procedure has to be terminated. Some societies advice stopping of short- or long-term glucagon-like peptide-1 receptor agonists in the day or a week before the examination, while others recommend this on case-by-case basis only. Before colonoscopy, a longer than usual liquid diet should be adhered to, and use of modern bowel-cleansing preparations given in split dose is advised, tailored individually. Endoscopists’ have little individual experience in patients taking these drugs and implementation of a registry should lead to more knowledge about this special group of patients.
Összefoglaló
Az inkretinekre ható gyógyszerek emésztőszervi mellékhatásai, valamint a diabetes mellitus és társbetegségei szükségessé tehetik az endoszkópiát. Leggyakrabban ételmaradék észlelhető a gyomorban, amely olyan mértékű lehet, hogy a vizsgálat félbehagyását teszi szükségessé. A tápcsatorna felső szakaszának elektív endoszkópos vizsgálata előtt a betegeknek hosszabb (16–18 óra) étkezési szünetet kell tartani. Egyes szakmai társaságok a kezelés felfüggesztését javasolják egy nappal vagy héttel az endoszkópia előtt, mások szerint egyéni elbírálás szükséges. Kolonoszkópia előtt hosszabb diétára, a modern béltisztító szerek osztott adására és bőséges folyadékfogyasztásra van szükség. Az egyéni tapasztalat ezen a területen csekély, így szükséges lenne egy regiszter létrehozása, amely nagyobb számú beteg kiértékelését tenné lehetővé.
Történeti áttekintés
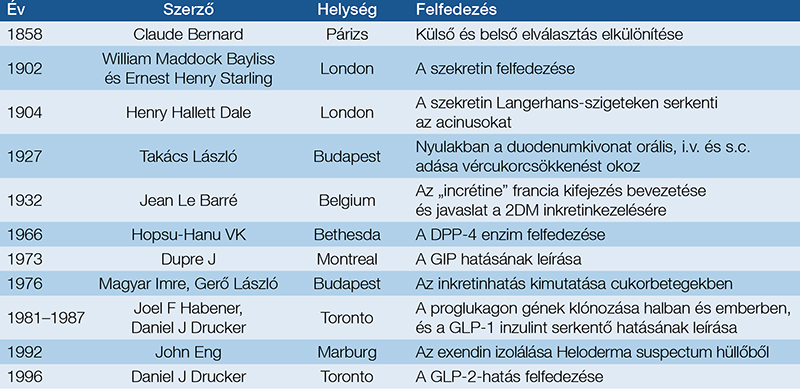
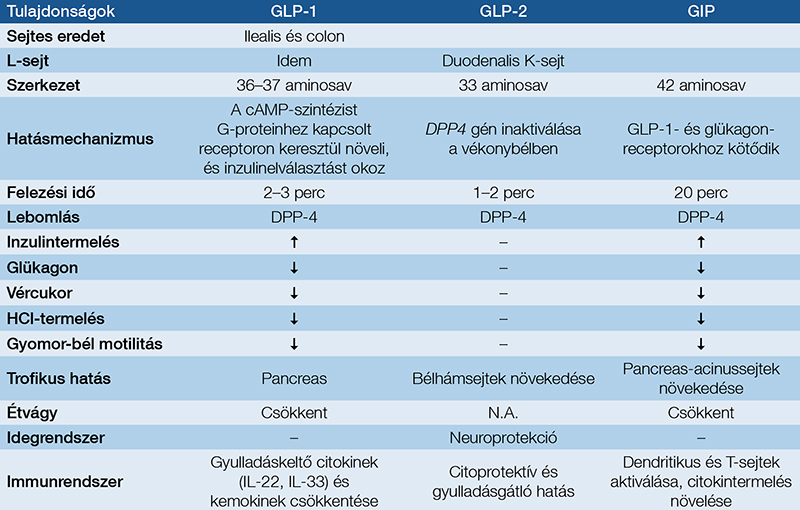
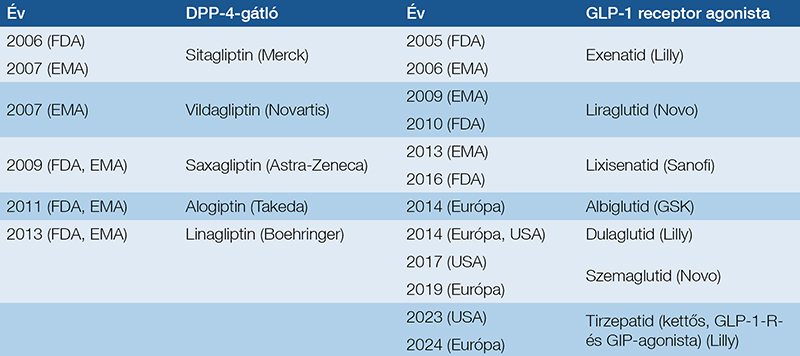
Az inkretinkészítmények történetét az 1. táblázatban a ma is idézett magyar hozzájárulásokkal mutatjuk be (1–4). Az inkretinek olyan hormonok, amelyek étkezés után szabadulnak fel és inzulinszekrécióhoz vezetnek (5). Mai tudásunk szerint a glükagonszerű peptid-1-et és 2-t (GLP-1 és GLP-2), valamint a glükózfüggő inzulinotrop polipeptidet (régebben: gastric inhibitory peptide) (GIP) tartjuk inkretinnek: hatásaikat a 2. táblázatban vázoljuk (2–6). Számos más peptid (pl. az amylin, a neuropeptidek) rendelkezik inkretinszerű tulajdonságokkal: ezek bemutatása meghaladja a dolgozat témáját. Élettani körülmények között az inkretineket a DDP-4 inaktiválja, így előbb a DPP-4-gátló készítményeket fejlesztették ki (3. táblázat), de a GLP-1-RA megjelenésével azok háttérbe szorultak.
Az egyre növekvő számú kezelt beteg miatt gyakran fordul elő, hogy a GLP-1-RA-készítményekkel kezelt esetekben endoszkópos vizsgálatot kell végezni. Az endoszkópiára két indikációs csoportban kerül sor:
- a GLP-1-RA-kezelés mellékhatásai miatt;
- a T2DM-hez és obesitashoz társult betegségek miatt (peptikus fekély és szövődményei, gastroparesis, Helicobacter pylori-fertőzés, pancreatitis, diverticulosis, tumorok, műtét előtti vizsgálatok, szűrés).
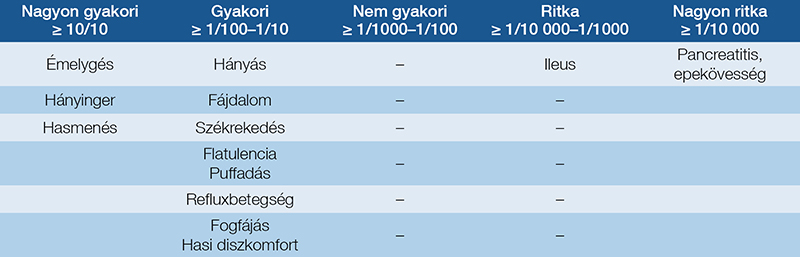
A GLP-1-RA-készítmények emésztőszervi mellékhatásait egységesen gyakoriság szerint osztályozzák (4. táblázat). A rövid hatású (1–2× naponta) és a heti 1× adagolású GLP-1-RA-kezelés során a kezelés első heteiben lépnek fel, ezért a kezeléseket fel kell építeni a legkisebb adagtól a legmagasabb engedélyezett adagig. Gyakoriságuk és intenzitásuk idővel csökken. Idősebb betegeknél gyakoribbak a mellékhatások. Túlsúlyos betegekben kevesebb a mellékhatás, mint T2DM-ben. Az FDA adatbázisában 21 281 mellékhatást jeleztek; a gyakorisági sorrend a hányinger, a hasmenés, a hányás, a hasi fájdalom, a székrekedés és a pancreatitis volt. Az elemzés szerint a hányinger és a hányás kockázata a szemaglutidkezelés során volt a legmagasabb; hasi fájdalmat leggyakrabban a liraglutid okozott. Obesitasban az engedélyezett adagok magasabbak, mint T2DM-ben. Szemaglutid- és tirzepatidkezelés során hányinger 44,4% és 43%-ban, hányás 21% és 15%-ban jelentkezett (7–17).
Pancreatitis ebben a sorrendben lép fel: liraglutid, szemaglutid, dulaglutid, lixisenatid, exenatid; gyakorisága 0,07–0,2%. A betegek félelmeivel ellentétben a GLP-1-RA-kezelés alatt a pancreatitis gyakorisága nem haladja meg az átlagos populációban mért arányokat (9).
Az orális szemaglutid az esetek 33–71%-ban okoz hányingert, ezt a szubkután adagolás 54%-ban, a placebo 28%-ban váltja ki (12).
A GLP-1-RA-kezelés egy skandináv regiszter, illetve retrospektív kohorszadatok alapján nem növeli az intestinalis obstrukció kockázatát (13, 14).
A DPP-4-gátlók esetében az alkalmazási előiratok szerint a székrekedés és a hányinger a nem gyakori mellékhatások között szerepel. Esetleírásokban és az alkalmazási előírásokban mindegyiknél szerepel nagyon ritka mellékhatásként az akut pancreatitis (beleértve annak nekrotizáló és haemorrhagiás formáját is), de metaanalízisek szerint a gyógyszercsoport más antidiabetikumokkal összehasonlítva nem emeli sem a pancreatitis, sem a pancreasrák kockázatát (15). Mind a GLP-1-RA-, mind a DDP-4-gátló kezelés kezdetén ajánlatos a betegek figyelmét felhívni a pancreatitis tüneteire, megelőzendő a pánikreakciókat és tévhiedelmeket.
A tápcsatorna felső szakaszának endoszkópos vizsgálata
A vizsgálat indikációja lehet a T2DM-től és/vagy a GLP-1-RA-kezeléstől független betegség (peptikus fekély, alarm tünetek, vérzés, dysphagia, reflux, halitosis, anémia, puffadás, kóros képalkotói eredmény) (16) vagy a kezelés mellékhatása (erős hasi fájdalom, hányás, pancreatitis, gastroparesis). A vizsgálat elvégezhető sürgősségi jelleggel (hyperemesis, vérzés) vagy elektíven, tervezett időpontban. Leggyakrabban az ételmaradék jelenlétét írták le: ez lehet darabos vagy folyékony; esetenként csak foltokban fedi a nyálkahártyát, máskor a gyomor lumenét kisebb-nagyobb arányban kitölti, attól függően, mit és mennyit evett a beteg. Leírták bezoár jelenlétét is (10–19). A gyomortartalom a vizsgálat alatt kiürülhet, megnehezítve a beavatkozást. Az intragastricus ételmaradék oka lehet a GLP-1-RA-kezelést megelőző lelassult gyomorürülés vagy gastroparesis, ennek hátterében állhat DM, hypothyreosis, refluxbetegség, alvási apnoe, autoimmun betegségek, Parkinson-kór, gyógyszerhatások, illetve maga az inkretinagonista-kezelés (19, 20). Több tényező együttes jelenléte megnehezítheti a tünetek pontos okának megállapítását. Az ételretenció következménye a hányinger és a hányás; bár a retenció mértéke és a tünetek erőssége között nincs lineáris összefüggés, ritkán gastroparesis alakulhat ki (21). Leírták a tachyphylaxiát is: rövid hatású GLP-1-RA esetén a kezdetben okozott gyomorürülési zavar néhány hét alatt csökkenhet (21). A gyomorürülés lassulása akár kedvezően is hathat a posztprandiális vércukorértékekre. T2DM-ben az orális szemaglutid is csökkenti a gyomorürülést, de elhízottakban ez a hatás kevésbé kifejezett (22).
A gyomorürülés kiértékelésére rendelkezésre áll a szcintigráfia, a 3D-s vagy a funkcionális ultrahang, a hagyományos báriumpasszázs és a kapszulaendoszkópia: ezek elérhetősége és időzítése azonban korlátozott és a centrumokra szorítkozik. Helyes, ha még a kezelés bevezetése előtt rákérdezünk a jellegzetes tünetekre (posztalimentáris telítettségérzés, hányinger); hasznos adatokat szolgáltathat a gasztrointesztinális motilitás vizsgálatában jártas ultrahangos szakember is. A képalkotó módszerek eredménye nem mindig egyezik az endoszkópia során látottakkal (21).
a) Gyomorretenció.A GLP-1-RA-készítményekkel kezelt betegekben az endoszkópia során az esetek 14–25%-ában találtak ételmaradékot a gyomorban, szemben a kontrollcsoportok 2,3–4,6%-os arányával (16, 21, 23). A vizsgálat megszakítása a gyomorbennék miatt 1,5–2,5%-ban következett be. Bronchialis aspirációt 0,2%–0,3%–0,7%-ban észleltek. Egy 2025-ös metaanalízisben 105 415 beteg közül 32 144 részesült GLP-1-RA-kezelésben. A gyomorretenció aránya 14% volt, a kontrollcsoportban 2,34%. A vizsgálat félbeszakítására 1,75%-ban volt szükség (kontroll: 0,3%). A vizsgálatot 2,24/1,09%-ban kellett megismételni. Aspirációt 0,73%-ban, illetve 0,35%-ban észleltek (23–27).
Az összesített eredmények alapján meghatározták, hogy milyen tényezők jelzik előre a gyomorretenciót, megelőzendő a sikertelen vizsgálatot. A férfiak inkább hajlamosak a retencióra, mint a nők; a magasabb BMI viszont nem befolyásolja a retenciót. A nem cukorbeteg és a T2DM-es betegek kockázata azonos, a magasabb hemoglobin A1c-érték és az inzulinkezelés nem fokozza a retenciót (26).
A gyomorretenció aránya 10,9% volt a dulaglutid-, 15,6% a szemaglutid-, 8,1% a liraglutid-, 6,2% az exenatid- és 18,9% a tirzepatidkezelés során. A tanulmányok többsége retrospektív, így az eredmények nem tekinthetők véglegesnek (23, 25).
A gyakorlatban a gyomorretenció elkerülése érdekében a tápcsatorna felső szakaszának endoszkópos vizsgálata előtti napon folyékony-pépes étrend fogyasztása javasolt; a vizsgálat előtti étkezési szünet a szokásos 12 óra helyett 16–18 órára hosszabbítható: így megelőzhető a sikertelen vagy ismételt vizsgálat. A cukorbetegeknél a beavatkozást a reggeli órákra kell időzíteni, továbbá a vércukorcsökkentő gyógyszerek és/vagy az inzulin adását ennek megfelelően csökkenteni kell. Mindezekről a beteget előzetesen tájékoztatni kell.
b) Légzőszervi szövődmények. Az endoszkópos vizsgálatoknak vannak olyan légzőszervi kockázati tényezői, amelyek szövődményekre hajlamosítanak: ezek az előrehaladott életkor, a COPD, demencia, a stroke, a fül-orr-gégészeti daganatok, gyulladások és a nyelőcsődaganatok. A lehetséges szövődmények az aspiráció és annak következtében a tüdőgyulladás és/vagy légzési elégtelenség, amelyek az endoszkópia után 1–14 nappal léphetnek fel. Feltételezték, hogy a GLP-1-RA és DDP-4-gátlók (akárcsak az ópiátok) a gyomorretenció révén hajlamosítanak a légzőszervi szövődményekre. Az eredmények ellentmondásosak: egy kohorsztanulmány szerint a GLP-1-RA-kezelés alatt végzett endoszkópia során az aspiráció kockázata magasabb, mint az SGLT-2-gátlóval végzett kezelések során (23). Egy amerikai metaanalízisben GLP-1-RA-kezelés mellett az aspiráció gyakorisága magasabb volt (25), míg egy másikban az aspiráció, a tüdőgyulladás és a légzési elégtelenség kockázata nem volt magasabb a GLP1-RA-kezelés, mint a DPP-4 gátló- vagy az ópiátkezelés során (26).
c) A vizsgálat félbeszakítása és ismétlése. GLP-1-RA-kezelés alatt az endoszkópos vizsgálat megszakításának kockázata ötszörösére, a vizsgálat ismétlésének kockázata kétszeresre növekedett (26).
Nem endoszkópos adat, de a GLP-1-RA adásával kapcsolatos, hogy az izraeli országos regiszterben 36 436 beteg részesült a Helicobacter pylori eradikációs kezelésében; közülük 426 kapott GLP-1-RA-készítményt is. Az eradikáció sikerének aránya 83,7% és 86,6% volt. A legjobb, 93,8%-os eredményt a szemaglutiddal kezelt csoportban értek el, a liraglutid melletti sikerráta csak 81,4% volt. A kedvező hatást a szerzők a lassú gyomorürülésnek tulajdonítják, de nincs adat, hogyan módosul az eradikációra adott gyógyszerek felszívódása és plazmaszintje GLP-1-RA-kezelés során (28).
Pancreatobiliaris endoszkópos beavatkozások (ERCP, EUH)
A GLP-1-RA-kezelés szövődménye lehet az akut pancreatitis, amelyre maga a T2DM is hajlamosít. Az ERCP biztonságosságáról GLP-1-RA-kezelés alatt nincs adat, de egy retrospektív amerikai tanulmányban 29 423 kezelt T2DM-es betegnél (liraglutid, szemaglutid, dulaglutid és tirzepatid) a GLP-1-RA csökkentette a pancreatitis szövődményeit, a szepszis és a sokk gyakoriságát; valamint kevesebbszer volt szükség gépi lélegeztetésre és parenterális táplálásra (29).
Egy esetbemutatásban EUH során a dulaglutidkezelés alatt fellépett pancreatitis és mesenterialis trombózis miatt szükségessé vált vizsgálatot szövődménymentesen sikerült elvégezni (30). Az elsőként használt GLP-1-RA-t, az exenatidot itthon is használják kis insulinomák lokalizálására: a 68Ga-val jelzett GLP-1-RA a PET/CT során pontosabbnak bizonyult, mint az EUH és/vagy az MRI (31).
Kapszulaendoszkópia
Liraglutid adása után írták le először a kapszula tranzitidejének meghosszabbodását. Egy retrospektív tanulmányban 36 betegnél a GLP-1-RA-kezelés alatt a gyomor- és a vékonybél-tranzitidő hosszabbodását igazolták. A kapszula lassabb ürülése az esetek 30%-ában alakult ki, szemben a kontrollcsoport 3%-ával. Emiatt javasolják a metoclopramid vizsgálat előtti adását. Az eredmény nem volt értékelhető az esetek 23%-ában, mivel a tranzitidő megnyúlása miatt a kapszula eleme lemerült, túllépve a gyárilag szavatolt 8 órás működési időt (32).
Kolonoszkópia
A felső traktus vizsgálatához képest a GLP-1-RA-kezelés idején végzett kolonoszkópiáról kevés adat van. Liraglutidkezelés alatt végzett kolonoszkópia során a nem megfelelő előkészítés, a BBPS értéke, a coecum intubációja és a polipdetekció aránya azonos volt a kontrollcsoporttal (32). Egy másik tanulmányban azonban mindezeket az indikátorokat gyengébbnek találták a GLP-1-RA-csoportban, és az ismételt vizsgálatra 15%-ban volt szükség (33). A vizsgálat előtt a szokásos 2 napnál hosszabb ideig ajánlott folyékony-pépes étrendet tartani (a pontos időtartamot egyénileg határozzák meg). A GLP-1-RA-készítményeket szedő betegek az ún. „nehezen előkészíthető esetek” csoportjába tartoznak, ezért ajánlott a modern béltisztító szerek (polietilénglikol, nátrium-pikoszulfát, macrogol) adása a keserűsó, a bisacodyl vagy a senozid helyett; továbbá az egyénileg tolerálható, nagy volumenű folyadék fogyasztása, kétszeri elosztásban a vizsgálat előtti napon (34). Evidenciajellegű ajánlásokhoz azonban prospektív tanulmányokra van szükség.
Az inkretinek és a gyulladásos bélbetegségek
A DPP-4 nemcsak az inkretineket bontja le, de immunszabályozó hatásokkal is rendelkezik (citokinek és kemokinek lebontása, dendritsejtek aktivitásának szabályozása, és T-sejtek aktiválása) (35). Mindezeknek jelentősége az emberi IBD bonyolult immunológiai folyamataiban nem tisztázott. A híresen pontos dán nemzeti regiszterben 2007–2019. között 3751 fő, T2DM-ben és IBD-ben (960 Crohn-betegség, 2791 colitis ulcerosa) szenvedő beteget kezeltek GLP-1-RA-készítményekkel (982 eset) vagy más antidiabetikumokkal (2769 eset). A GLP-1-RA-kezelésben részesülő betegeknél az új szteroid és TNF-alfa-gátló adásának szükségessége, a kórházi és sebészeti kezelések aránya alacsonyabb volt, mint más vércukorcsökkentő kezelések során (36). Direkt, fej-fej melletti prospektív összehasonlító tanulmány a GLP-1-RA-k, a DPP-4-gátlók és más antidiabetikumok között nem történt.
Az inkretinalapú kezelés és az emésztőrendszeri rákok
Mint minden innovatív készítménynél, az inkretinalapú kezeléseknél is felmerült a gyógyszerek esetleges rákkeltő hatásának kimutatása. A DPP-4 kifejeződése a tumorsejtekben fokozott, de ennek jelentősége nem ismert. Egy 5 éves követéses vizsgálatban 344 500 beteg részesült DPP-4-gátló kezelésben és 124 930 beteg metformint kapott. Az összes daganat gyakorisága 8,7%, illetve 8,3% volt. Vastagbélrákos cukorbetegeknél a DPP-4-gátlóval kezelt esetek 5 éves túlélése rövidebb volt. Feltételezik, hogy a DPP-4-gátlók elősegítik a tumor környezetében az epithelialis-mesenchymalis tranzíciót, kedvező körülményeket teremtve a tumorképződésnek.
A kezdeti esetbemutatások után a metaanalízisek kimutatták, hogy a DPP-4-gátlók nem növelik a hasnyálmirigyrák kockázatát (37).
A GLP1-RA-kezelés során egyes tanulmányok a kolorektális rák kockázatának növekedését, mások annak csökkenését mutatták ki. A hasnyálmirigyrák kockázata nem változik, a májrák kockázata viszont csökken (38).
Emberben az emésztőszervi rákok kialakulása évtizedes folyamat. A DPP-4-gátlókat és a GLP-1-RA-kat túl rövid ideje vezették be ahhoz, hogy akár onkogén, akár protektív hatásukat mérvadóan megítélhessük: ehhez is hosszú távú prospektív tanulmányok szükségesek.
Műtéti és endoszkópos bariatrikus eljárások
A bariátriai sebészet eljárásait és a GLP-1-RA-kezelést egymás kiegészítéseként lehet alkalmazni akkor, ha a műtét után nem megfelelő a testsúlycsökkenés vagy a beteg hajlamos a súlygyarapodásra. Ilyen esetekben a liraglutid és szemaglutid biztonságosan adható; hányinger 19%-ban, hányás csupán ritkán lép fel (39). Az endoszkópos eljárások (gyomorballon, endoszkópos gyomorszűkítés, duodenojejunalis bypass, transpyloricus ballon, duodenalis mucosa-resurfacing) utáni szövődmények (gyomorfekély, hányás, fájdalom) relatíve ritkán teszik szükségessé az ismételt endoszkópiát; GLP-1-RA-kezelés során ilyen esetekben még nincs tapasztalat (40).
Konszenzusok
2023-ben az Amerikai Aneszteziológiai Társaság konszenzust dolgozott ki a GLP-1-RA-kezelés alatt álló betegek endoszkópos ellátására az alábbiak szerint:
a) a tápcsatorna felső szakaszának sürgős endoszkópos vizsgálata esetén a GLP-1-RA-val kezelt beteget úgy kell ellátni, mintha étkezés utáni állapotban érkezett volna;
b) elektív vizsgálatok esetén a napi egyszeri adagolású GLP-1-RA-készítményeket az endoszkópia napján nem kell beadni; heti egyszeri adagolás esetén egy héttel a vizsgálat előtt a soros adagot nem kell beadni, bár ez vércukoremelkedést okozhat);
c) hányinger, hányás esetén a vizsgálatot el kell halasztani (41).
A fentiekkel ellentétben az ACG, az AGA és az AASLD közös állásfoglalása szerint a tápcsatorna felső szakaszának elektív endoszkópos vizsgálata esetén a GLP-1-agonista-kezelés elhagyása egyéni elbírálást igényel (42). Kivételt képeznek az elhízott betegek, ahol indokoltnak vélik a kezelés felfüggesztését az adott GLP-1RA felezési idejének (5–7 nap) háromszorosára. Európai állásfoglalás még nincs.
A kolonoszkópia esetében GLP-1-RA-kezelés során ajánlás még nem jelent meg. Szakértők szerint a legfontosabb a beteg megfelelő tájékoztatása mind az előkészítésről, mind a vizsgálat jellegéről és az adott GLP-1-RA lehetséges hatásairól: ez a szakasszisztensek és az orvosok feladata.
Következtetések
Vitathatatlan előnyei ellenére a GLP-1-RA-kezelés során a mellékhatások és a társbetegségek ellátása sajátos problémákat vet fel: ezeket a háziorvosoknak, a diabetológusoknak és a gasztroenterológusoknak ismerniük kell. A gyakorlatban egy háziorvosra/diabetológusra kisszámú olyan beteg jut, akit a GLP-1-RA-kezelés ideje alatt endoszkópiára kell küldeni; és fordítva: az endoszkópos szakemberhez ritkán jut olyan beteg, aki ilyen kezelést kap. Így az egyéni tapasztalat nehezen gyarapodik. A kontrollált tanulmányok szervezése bonyolult és költséges, ezért egy regiszter vezetése lehetővé tenné nagyobb számú beteg kiértékelését.
Rövidítések
- IBD = American Association for the Study of Liver Diseases
- ACG = American College of Gastroenterology
- ADA = American Diabetes Association
- AGA = American Gastroenterological Association
- ASGE = American Society for Gastrointestinal Endoscopy
- BBPS = Boston Bowel Preparation Scale
- COPD = krónikus obstruktív tüdőbetegség
- DPP-4 = dipeptidil-dipeptidáz-4
- EMA = European Medicinal Agency
- ERCP = endoszkópos cholangio-pancreatographia
- EUH = endoszkópos ultrahang
- FDA = Food and Drug Administration
- GLP-1 = glükagonszerű peptid-1
- GLP-1-RA = GLP-1-receptor agonista
- H. pylori = Helicobacter pylori
- IBD = gyulladásos bélbetegség
- MDT = Magyar Diabétesz Társaság
- MGT = Magyar Gasztroenterológiai Társaság
- RKT = randomizált kontrollált tanulmány
- T2DM = 2-es típusú diabetes mellitus
Irodalom
2. Rehfeld JF. The origin and understanding of the incretin concept. Front Endocrinol 2018; 9: 387. https://doi.org/10.3389/fendo.2018.00387
3. Magyar I, Gerő L, Korányi I, et al. Intravénás és duodenalis cukorterhelés cukorbetegekben, az enterohormonok szerepe. Magyar Belorv Arch 1976; 29: 57–64.
4. Drucker DJ, Habener JF, Holst JJ. Discovery, characterization, and clinical development of the glucagon-like peptides. J Clin Invest 2017; 127(12): 4217–4227. https://doi.org/10.1172/JCI97233
5. Zsembery Á. Az emésztőszervi hormonok és jelátvivők. In: Tulassay Zs, szerk. Gasztroenterológia. Budapest: Medicina Könyvkiadó Zrt; 2023. 30.
6. Ahrén B. DPP-4 inhibition and the path to clinical proof. Front Endocrinol 2019; 10: 376. https://doi.org/10.3389/fendo.2019.00376
7. Sorli C, Harashima SI, Tsoukas GM, et al. Efficacy and safety of once-weekly semaglutide monotherapy versus placebo in patients with type 2 diabetes (SUSTAIN 1): a double-blind, randomised, placebo-controlled, parallel-group, multinational, multicentre phase 3a trial. Lancet Diabetes Endocrinol 2017; 5(4): 251–260.
https://doi.org/10.1016/S2213-8587(17)30013-X
8. Capehorn MS, Catarig A-M, Furberg JK, et al. Efficacy and safety of one-weekly semaglutide 1 mg vs once daily liraglutide 1,2 mg as add-on to 1-3 oral antidiabetic drugs in subjects with type 2 diabetes (SUSTAIN 10). Diabetes Metab 2020; 46(2): 100–109. https://doi.org/10.1016/j.diabet.2019.101117
9. Smith MM, Van Raalte DH. Safety of semaglutide. Front Endocrinol 2021; 12: 645563. https://pubmed.ncbi.nlm.nih.gov/34305810/ https://doi.org/10/3389/fendo.2021.645563
10. Hu EH, Tsai ML, Lin Y, Chou TS, Chen TH. A review and meta-analysis of the safety and efficacy of using glucagon-like peptide-1 receptor agonists. Medicina 2024; 60(3): 357. https://doi.org/10.3390/medicina60030357
11. Aronne LJ, Bader Horn D, le Rox CW, et al. Tirzepatid as compared to semaglutide for the treatment of obesity. NEJM 2025; 393(1): 26–36. https:///doi.org/10.1056/NEJMMoa2416394
12. Niman S, Hardy T, Goldafen RF, et al. A review on the efficacy and safety of oral semaglutide. Drugs in R&D 2021; 21(2): 133–148.
https://doi.org/10.1007/s40268-021-00341-8
13. Ueda P, Wintzell V, Melbye M, et al. Use of DPP4 inhibitors and GLP-1 receptor agonists and risk of intestinal obstruction: Scandinavian Cohort Study. Clin Gastroenterol Hepatol 2024; 22(6): 1226–1237. https://doi.org/10.1016/j.cgh.2023.08.034
14. Gao Z, Tabernacki T, Dorney I, et al. Association of GLP-1 receptor agonists with risk of intestinal obstruction in patients with type 2 diabetes mellitus: a retrospective cohort study. Acta Diabetol 2025; 62(11): 1941–1951. https://doi.org/10.1007/s00592-025-02525-z
15. Dicembrini I, Montereggi C, Neu B, et al. Pancreatitis and pancreatic cancer in patients treated with dipeptidyl peptidase-4 inhibitors: an extensive and updated meta-analysis of randomized controlled trials. Diabetes Res Clin Pract 2020; 19: 107981. https://doi.org/10.1016/j.diabres.2019.107981
