Reviews
Upper gastrointestinal manifestations of systemic autoimmune diseases
Summary
Several systemic autoimmune diseases can lead to diverse manifestations and clinical abnormalities within the gastrointestinal tract. These alterations may present with overt symptoms, pose significant differential diagnostic challenges, and in certain cases, carry prognostic implications. In the upper gastrointestinal tract, pathological conditions may arise due to autoantibody-mediated tissue injury, disorders of secretion or motility, immune-mediated pathologies, adverse effects of immunosuppressive or biological therapies, and secondary disruptions in gut–brain interactions.
Összefoglaló
Számos szisztémás autoimmun betegség okoz különféle manifesztációkat és klinikai eltéréseket a tápcsatornában: lehetnek tünetképzők, jelenthetnek differenciáldiagnosztikai kihívást, és egyesek prognosztikai jelentőséggel bírnak. A felső tápcsatorna területén autoantitestek által mediált szöveti károsodás, szekréciós vagy motilitási zavar, immunmediált gyulladás, a kezelések mellékhatásai és a következményesen kialakuló agy–bél interakció zavarai miatt is kialakulhatnak kórállapotok.
Bevezetés
Számos szisztémás autoimmun betegség okoz klinikai eltéréseket a tápcsatornában. Ezen eltérések lehetnek tünetképzők, jelenthetnek differenciáldiagnosztikai kihívást az endoszkópos kép, a képalkotó és a laboratóriumi vizsgálati eredmények értékelésekor, valamint egyesek prognosztikai jelentőséggel bírnak. Számos gyakorlati kérdés merül fel a témával kapcsolatban:
- Mely autoimmun betegségek járhatnak felső tápcsatornai tünetekkel?
- Milyen felső gasztrointesztinális tünetekkel járhatnak a szisztémás autoimmun betegségek, és hogyan lehet felismerni az egyes autoimmun kórképeket (korai) tápcsatornai érintettség alapján?
- Milyen malignizálódási kockázattal járnak a tápcsatornai manifesztációt adó autoimmun kórképek?
Autoimmun kórképek manifesztációi a nyelőcső, a gyomor és a duodenum területén is megjelennek, de kezelésük is járhat mellékhatásokkal vagy szövődményekkel. A felső tápcsatornai tünetek és gyulladásos folyamatok differenciáldiagnosztikai feladatot jelentenek a gasztroenterológus szakorvosoknak, a családorvosoknak és a belgyógyászoknak egyaránt. Ezen kórképekre általánosságban jellemző, hogy a rutinszerű kivizsgálások jelentős hányadában vagy nem születik megfelelően alátámasztott diagnózis, vagy csak későn, a szövődmények megjelenését követően. A szisztémás autoimmun háttérrel rendelkező betegségeket autoimmun betegségekre, autoinflammatorikus betegségekre és kevert mintázatú betegségcsoportra osztjuk. Alapvetően elmondható, hogy a korán felismert autoimmun kórképekben javíthatunk a betegek életminőségén és túlélési mutatóin. Az autoimmun kórképekben a gasztrointesztinális eltérések jelentkezhetnek az autoantitestek által mediált szöveti károsodás miatt, a betegségből adódó szekréciós vagy motilitási károsodás okán, a T- és B-sejtes immunmediált szöveti / vascularis gyulladásos aktivitás révén, az alkalmazott terápiák mellékhatásai miatt (NSAID, metotrexát, szteroid, azathioprin, ciklofoszfamid stb.), valamint a következményesen kialakuló agy–bél interakció zavarai miatt.
A gasztrointesztinális traktust is érintő autoimmun kórképek a patomechanizmusuk közös jellemzői szerint 3 fő csoportra oszthatók (1):
- Autoimmun betegségek: az adaptív immunrendszer túlzott aktivációja jellemzi őket; (T- és B-sejtek) autoantitestek termelődésével és szervkárosodással járnak. Gyakori velejárójuk a szervkárosodás, jellemzőjük a női dominancia.
- Autoinflammatorikus betegségek: a veleszületett immunrendszer túlaktiválása jellemzi őket (pl. inflammaszóma, IL-1, IL-18). Genetikai háttér, láz, gyulladás, autoantitestek nélkül.
- Kevert mintázatú betegségek: mind az adaptív, mind pedig a veleszületett immunválasz szerepet játszik a kialakulásukban, változó klinikai képet okozva.
Bár ezek a betegségek immunpatogenezisükben és klinikai megnyilvánulásaikban is eltérőek, közös jellemzőjük, hogy a gasztrointesztinális traktus struktúrája és funkciója mindegyik esetében károsodik a vasculitis, az immunkomplex-depozíció vagy az extracelluláris mátrix megváltozása révén (1).
Az autoimmun betegségeknek nagy jelentőséget ad mind a gyakori előfordulásuk (kb. 10% az összprevalenciájuk az UK lakosságában) (2), mind pedig a mortalitásuk (vezető halálokok a fiatal és a középkorú nők körében). Tápcsatornai megjelenésük gyakorisága változó, és ezek klinikai jelentősége nem mindig egyértelmű. A nyelőcső, a gyomor és a vékonybél korai érintettsége diagnosztikus kihívást jelenthet, mivel a tünetek gyakran nem specifikusak, az okozott gyulladásos folyamatok többségben más kóreredetből származnak, és a kórszövettani diagnosztika is csak ritkán segít az ezek közti differenciálásban. A felső tápcsatornai manifesztációt okozó autoimmun folyamatok részben célszervspecifikusak, mint például az autoimmun gastritis (autoimmun metaplasticus gastritis = AMAG, anaemia perniciosa), részben pedig szisztémás autoimmun betegségek tápcsatornai manifesztációi, vagy egyéb mechanizmusú, nem autoimmun kórképek következtében kialakult patológiás állapotok (1. táblázat).
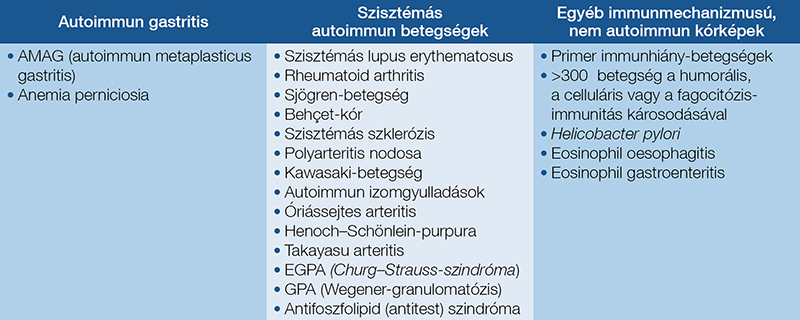
Külön említést érdemel a gyomor specifikus autoimmun gyulladásos folyamata (AIG, parietalis sejt elleni AT, illetve intrinsic faktor elleni AT-pozitivitással), amely elsősorban a corpus gyulladásos folyamatával jár; összességében mérsékelten emeli a gyomor malignus folyamatainak kialakulását. Ha az antrum gastritise és atrophiája mellett a corpus atrophiája is jelen van az autoimmun gastritisben (AIG), az korábbi vagy jelenlegi Helicobacter pylori-fertőzésre utal, amely tovább növeli a malignizálódási frekvenciát, valamint indokolja a helicobacteriosis keresését és 3 évente nagyfelbontású endoszkóppal a szövettani követést.
A coeliakia autoimmun mechanizmusú betegség, a duodenum típusos érintettsége mellett krónikus gastritissel jár.
Célkitűzés
Jelen összefoglaló a felső gasztrointesztinális tápcsatornai manifesztációkat adó autoimmun kórképeket, a felismerésükhez szükséges tápcsatornai tüneteket, a megjelenésüket és a prognózisukat részletezi a korai felismerés, valamint a megfelelő követés és terápia elősegítése céljából.
A leggyakoribb felső tápcsatornai tünetekkel járó autoimmun betegségek (1. ábra):
- Rheumatoid arthritis
- Autoimmun gastritis
- SLE (szisztémás lupus erythematosus)
- Sjögren-betegség
- Szisztémás szklerózis (scleroderma)
- Behçet-szindróma
- Eosinophil granulomatosus polyangitisszel (EGPA)
- Idiopátiás inflammatorikus myopathiák
- Henoch–Schönlein-purpura
- Polyarteritis nodosa
- Kawasaki-betegség
- Coeliakia

Mik a szisztémás autoimmun betegségek leggyakoribb felső tápcsatornai manifesztációi (2. táblázat)?
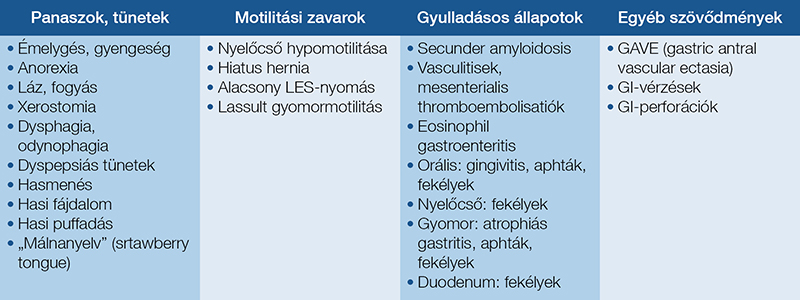
Az autoimmun kórképek a felső tápcsatornai traktusban részben a gyulladásból adódóan tartósan kellemetlen általános tüneteket okoznak, mint például a hányinger, az émelygés, a gyengeség, az étvágytalanság, a fogyás vagy az ismeretlen eredetű visszatérő láz. Amennyiben a gyulladásos folyamat a mucosát, az izomréteget, illetve a neuronális hálózatot érinti, „sicca” tünetek (xerostomia), anaciditás, fájdalom (globus pharyngeus, retrosternalis fájdalom, epigastrialis fájdalom, odynophagia, dyspepsiás panaszok), a maldigestiós-malabszorpciós mechanizmusokból adódó haspuffadás, a széklethabitus változása, valamint dysphagia jelentkezik.
A gyulladásos folyamatok érinthetik a felső gasztrointesztinális motilitást is, amely kapcsán minor és major nyelőcső-motilitási zavarok (3), valamint gyomormotilitási zavarok is kialakulhatnak. A Chicago 4.0 klasszifikáció (2022) alapján az ide is sorolható major nyelőcső-motilitási zavarok a következők: achalasia (I-III. altípus), az oesophago-gastriscus junctio kimeneti obstrukciója (EGJOO), a hiányzó kontraktilitás, az oesophagus distalis végének spasmusa, hypercontractilis oesophagus, illetve ineffektív nyelőcső-motilitás. Ezenfelül megkülönböztetünk minor nyelőcső-motilitási zavarokat is: ineffektív nyelőcső-motilitás (IEM), fragmentált perisztaltika. A gyomor motilitási zavarai közé tartoznak a következők: gastroparesis, dumping szindróma, pylorusspasmus és a dyspepsia alapját képező kóros motilitási eltérések.
Differenciáldiagnosztikai kihívást jelent az autoimmun betegségek által kiváltható gyulladásos állapotok széles tárháza: vasculitisek, mesenterialis thromboembolisatiók okozta eltérések, eosinophil gastroenteritis, eosinophil oesophagitis, orális afták és gingivitis, fekélyek, atrophiás gastritis és az intestinalis metaplasia megjelenése. Súlyos vérzéses vagy perforációs szövődmények igen ritkán alakulnak ki.
Szisztémás lupus erythematosus (SLE)
Az SLE egy ismeretlen eredetű krónikus autoimmun betegség, amely a szervezetben lényegében bárhol okozhat eltéréseket; leggyakrabban fiatal vagy középkorú nők érintettek (nők és férfiak aránya megközelítőleg 10:1). A betegség során számos antinukleáris autoantitest (ANA) termelődése jellemző (pl. anti-dsDNA, anti-Smith, extrahálható nukleáris antitestek stb. termelődnek), amelyek immunkomplexeket képeznek, és szöveti károsodást idéznek elő. A tápcsatorna súlyos gyulladásos folyamata a betegek kb. 2–4%-ban fordul elő: lupus hepatitis, serositis, illetve enteritis. A tápcsatornai manifesztációk, illetve szövődmények azonban igen gyakoriak: kb. 40%-ban jelennek meg legalább egyszer a betegség lefolyása kapcsán (4–6), és többségüket társbetegségek okozta szövődmények okozzák (pl. fertőzések). (4–6) Ezek leggyakoribb okai az immunkomplex vasculitis, a direkt simaizom-károsodás, a neuronális léziók, az antifoszfolipid antitestek okozta thromboticus keringési zavarok, a kezelésre használt gyógyszer mellékhatásai, valamint a megnövekedett gyakoriságú szekunder infekciók.
Felső gasztrointesztinális manifesztációk
- Orális fekélyek: Az SLE-s betegek akár 50%-ánál előfordulhatnak; általában fájdalommentesek, de bizonyos típusú fekélyek fájdalmasak lehetnek. Ezek a fekélyek jellemzően a kemény szájpadlásra, a bajusz belső részére vagy az ajakperemre korlátozódnak.
- Nyelőcső-, gyomor- és duodenumérintettség: A nyelőcső motilitási zavara kb. 20–70%-ban mérhető SLE-ben szenvedő betegeknél; e zavarok a nagyfelbontású manometriás vizsgálatokkal (HREM) talált eltérések kapcsán differenciáldiagnosztikai problémaként merülnek fel; a pontos patomechanizmusuk eddig nem ismert, de a Raynaud-szindrómával és az anti-RNP (ribonucleoprotein) jelenlétével hozták összefüggésbe (7). A betegek fő panasza a dysphagia (a betegek kb. 1–13%-ában) és az odynophagia, amelyek részben a vasculitis és a motilitási zavarok következményei. Nyelőcsőfekély, sőt ritkán perforáció is kialakulhat. Az immunszuppresszáns kezelés alatt álló SLE-s betegeknél fokozott a fertőzéses szövődmények megjelenése. A nyelőcsőben candidiasis, CMV-, HSV-fertőzések a leggyakoribbak. A gyomorban az SLE növeli a peptikus fekélybetegség kialakulását, amely kockázat elkülönül az NSAID-kezelések mellett kialakuló fekélyektől. A vékonybélben elsősorban a fehérjevesztő enteropathia és a krónikus intestinalis pszeudoobstrukció hozható összefüggésbe súlyos SLE-vel (8).
Gyakorlati gasztroenterológiai vonatkozások
Az SLE esetében a gasztrointesztinális tünetekre való odafigyelés létfontosságú, különösen akkor, ha a beteg akut hasi panaszokat mutat. Az endoszkópia, a CT- vagy az MRI-vizsgálatok, valamint a szérum autoantitestjeinek és komplementszintjeinek mérése segít a pontos diagnózis felállításában. Szükség esetén a szövettani vizsgálatok alkalmasak a vasculitis vagy a gyulladásos folyamatok megerősítésére.
Rheumatoid arthritis (RA)
Egy ismeretlen etiológiájú, krónikus, szisztémás gyulladásos betegség, amely a populáció körülbelül 0,46%-át érinti, nők körében nagyobb gyakorisággal (nők : férfiak = 3:1 arány) és elsősorban az ízületek synovialis gyulladása jellemzi. Extraarticularis manifesztáció a rheumatoid arthritisben szenvedő betegek kb. 40%-ában fordul elő.
RA-ban az emésztőrendszeri érintettség az enyhébb funkcionális zavaroktól (pl. a nyelőcső dysmotilitása) a súlyos szövődményekig (kollagén colitis, szekunder amyloidosis, vasculitis okozta iszkémia) terjedhet. A leggyakoribb tápcsatornai érintettséget azonban elsősorban az NSAID gyulladáscsökkentő kezelések és a metotrexátkezelések mellékhatásai jelentik. Az alapvető klinikai megnyilvánulása a szimmetrikus, többízületi polyarthritis, de az extraarticularis tünetek, így a gasztrointesztinális érintettség is gyakori.
Felső gasztrointesztinális manifesztációk
- Orális tünetek:
– Az ideiglenes temporomandibularis ízületi érintettség nehezítheti a rágást.
– Másodlagos Sjögren-szindróma miatt előfordulhat szájszárazság, ami további nyelési problémákat okozhat. - Nyelőcső:
– A csökkent perisztaltika, az alsó nyelőcső-záróizom gyengülése elősegítheti a gastrooesophagealis reflux kialakulását.
– Feltehetően Felty-szindrómában az esophagealis fekélyek megjelenése is lehetséges. - Gyomor:
– Az RA kezelésében gyakran használt NSAID-ok hozzájárulnak a peptikus fekélyek kialakulásához, illetve a krónikus atrophiás gastritis is gyakoribb, mint az átlagpopulációban.
– Hosszú távon kialakuló másodlagos (AA) amyloidosis a bélrendszer bármely részét érintheti, malabszorpcióval, krónikus hasmenéssel járva. - Hasnyálmirigy és a hepatobiliaris rendszer:
– Ritkábban fordul elő pancreatitis, illetve cholecystitis, appendicitis, perisplenitis vagy az arteria hepatica arteritise; ezek mind az RA által kiváltott vasculitis következményei lehetnek.
Gyakorlati gasztroenterológiai vonatkozások
Az RA esetében a gyógyszeres kezelés (pl. NSAID-ok, DMARD-ok, biológiai terápiák) mellett elengedhetetlen az NSAID-indukálta gastropathia megelőzése savszekréció-gátlók (protonpumpa-gátlók) alkalmazásával, valamint az amyloidosis és a vasculitis esetleges komplikációinak korai felismerése és kezelése.
Sjögren-betegség
Egy gyakori autoimmun betegség, amelyet az exokrin mirigyek – leginkább a nyál- és a könnytermelő mirigyek – gyulladása és destrukciója jellemez. Az érintett populációban jelentős a női dominancia (nők és férfiak aránya kb. 9:1), és a betegség általában középkorú nőknél jelentkezik.
Felső gasztrointesztinális manifesztációk
- Orális tünetek
– A csökkent nyáltermelés szájszárazsághoz, dysphagiához, fogszuvasodáshoz és szájfertőzésekhez vezethet. - Nyelőcső
– Az esophagealis dysmotilitas, amely akár 36–90%-ban előfordul, dysphagiát vagy odynophagiát okozhat. - Gyomor
– Krónikus atrophiás gastritis, alacsony gyomorsavtermeléssel (hypochlorhydria vagy achlorhydria) és ennek következtében magas gasztrinszint, B12-vitaminhiány kialakulása. - Hasnyálmirigy
– Bár a szindrómában gyakori a szubklinikai érintettség, akut vagy krónikus hasnyálmirigy-gyulladás ritkán fordul elő. - Máj és epevezeték
– Enyhe intrahepaticus epevezeték-gyulladás vagy primer biliáris cirrózisszerű kép alakulhat ki. - Duodenum és vékonybél
– Ritkán lymphocytainfiltráció okozhat malabszorpciós jellegű tüneteket.
Gyakorlati gasztroenterológiai vonatkozások
A tüneti kezelés (pl. mesterséges nyál, hidratáció, prokinetikumok) mellett fontos az immunszuppresszív terápia és a B-sejtes lymphoma szűrése.
Szisztémás sclerosis (Scleroderma)
A scleroderma egy kötőszöveti betegség, amely során kollagén-túltermelődés miatt a bőr és a zsigerek (köztük a gasztrointesztinális traktus) fibrózisa alakul ki. A betegség főként a 30–50 éves nőket érinti, és az egyik legfontosabb jellemzője a progresszív szöveti megvastagodás.
Felső gasztrointesztinális manifesztációk
- Orális változások:
– A periorális bőr megkeményedése, a microstomia (csökkent szájnyílás) és az orális nyálkahártya atrophiája étkezési problémákhoz vezet. - Nyelőcső:
– A nyelőcső a leggyakrabban érintett szerv, aminek következtében a nyelőcső alsó záróizmának elégtelen lezárása refluxot, dysphagiát okozhat, és idővel Barrett-metaplasia kialakulásához vezethet. - Gyomor és vékonybél:
– A motilitási zavarok gastroparesist, a bél pszeudoobstrukcióját, a vékonybél bakteriális túlnövekedését és ennek következtében malabszorpciót idéznek elő.
Gyakorlati gasztroenterológiai vonatkozások
A savszekréciót gátló terápia (emelt dózisú PPI) és a prokinetikus szerek javítják a reflux (GERD) és a dysmotilitas következményeit, míg a táplálásterápia elengedhetetlen a malabszorpciós tünetek korrigálásához.
Idiopátiás inflammatorikus myopathiák (ld. polymyositis, dermatomyositis)
A polymyositis és a dermatomyositis olyan szisztémás autoimmun betegségek, amelyek elsősorban a harántcsíkolt izmokat érintik, és jellemzően két hullámban (gyermekkorban és középkorban) fordulnak elő. Dermatomyositis esetén jellegzetes bőrkiütések is megfigyelhetők.
Felső gasztrointesztinális manifesztációk
A nyelőcső és az orális izomzat érintettsége miatt dysphagia, asztmaszerű tünetek, regurgitáció és korai teltségérzet jelentkezhet. A gyomor- és vékonybél-perisztaltika csökkenése miatt kialakuló hasi puffadás „passage” zavarokat eredményez. A kis artériák és az arteriolák iszkémiás vasculopathiája miatt ulceratiók, perforáció, vérzés vagy akár infarktus alakulhat ki a GI traktus bármely részén. Ritka szövődmény az intestinalis pneumatosis. A diagnózis felállításához izombiopszia, laboratóriumi vizsgálatok, valamint esophagealis- és bélmotilitási vizsgálatok szükségesek. Külön megjegyzendő, hogy kialakuló súlyos nyelészavar esetén PEG beültetése is szükségessé válhat ezen kórképeknél.
Kevert kötőszöveti betegség (MCTD)
Átfedést mutat több autoimmun kórkép jellegzetességeivel, így az SLE, a szisztémás sclerosis és a polymyositis jellemzői egyaránt megjelennek. Immunológiai sajátossága az anti-U1-RNP ellenanyag jelenléte. Jellemző fő klinikai tünetei a Raynaud-jelenség, a kéz ödémája, az arthralgia, az arthritis, a myositis, az izomgyengeség és a sclerodermaszerű bőrelváltozások.
Felső gasztrointesztinális manifesztációk
Gasztrointesztinális érintettség kb. 66–74%-ban mutatható ki, tünetei a sclerodermához hasonlóak: gyakori a nyelőcső motilitási zavara (45–85%-ában van jelen), az idő múlásával dysphagia alakul ki, és az alsó oesophagealis sphincter hypomotilitása miatt a gastro-oesophagealis refluxbetegség súlyossága fokozódik.
Antifoszfolipid antitest szindróma (APS)
Ismétlődő érrendszeri trombózisok, terhességi komplikációk és thrombocytopenia jellemzi, amelyhez tartósan magas szintű antifoszfolipid antitestek társulnak. Jelentkezhet önálló kórképként, de társulhat SLE-vel is. Felső gasztrointesztinális manifesztációk az érrendszeri trombózisok, amelyek a mesenterialis artériák, a portális vénás rendszer vagy a hepaticus vénák trombózisával alakulnak ki, akut kezdetű hasi fájdalmat, béliszkémiát, illetve pancreatitist okozva.
Vasculitisek
Óriássejtes arteritis (Giant cell arteritis)
Elsősorban az idősebb korosztályt érinti; granulomatosus gyulladás jellemzi a nagy- és a közepes méretű artériákban, leggyakrabban a temporális artériában. A betegség fő tünetei közé tartozik a fejfájás, a magas vérsüllyedés és a látásvesztés kockázata.
A felső gasztrointesztinális manifesztációk ritkák; béliszkémia és általában enyhe transzamináz- és ALP-emelkedéssel járó májérintettség fordul elő.
Takayasu arteritis
Krónikus granulomatosus vasculitis, amely elsősorban az aortát és fő leágazásait érinti, leginkább fiatal, 10–40 év közötti nőknél. A következményeket az érintett artériák falának megvastagodása, szűkülete vagy aneurizma képződése okozza. Felső gasztrointesztinális manifesztációkat a mesenterialis iszkémia és annak következményei okoznak; posztprandiális hasi fájdalommal, hányással, hasmenéssel, sőt bélinfarktussal járhat.
Polyarteritis nodosa (PAN)
A közepes és kis artériákban kialakuló nekrotizáló vasculitis, amely a gasztrointesztinális traktus számos részét érintheti. Különösen a mesenterialis artériák érintettsége okoz jelentős klinikai problémákat a következményes iszkémia miatt.
Felső gasztrointesztinális manifesztációk
- Hasi fájdalom a betegek 23–70%-ánál fordul elő; általában enyhe és jellegtelen, de akut kezdetű hasi fájdalom béliszkémiára, ulceratiók kialakulására utalhat. Következményesen manifeszt tápcsatornai vérzés, perforáció jelentkezhet.
- Májérintettség: Bár gyakran szubklinikai, a máj esetében az alkalikus foszfatáz szintjének emelkedése és néha hepatitis is kialakulhat.
Prognosztikai és terápiás szempontok
A súlyos gasztrointesztinális szövődmények (infarktus, perforáció) rossz prognózisúak; a korai diagnózis és az agresszív immunszuppresszív kezelés (kortikoszteroidok, ciklofoszfamid) alapvetők a kimenetel javításában.
Kawasaki-kór
A Kawasaki-kór elsősorban gyermekkorban fordul elő, és a közepes méretű artériákat érintő akut lázas állapotként ismert. Az orális tünetek (például az „epernyelv”, ajakrepedések) mellett a betegség kiemelten a koszorúerek érintettségével járhat.
Felső gasztrointesztinális manifesztációk
Ritkán előforduló hasi fájdalom, hányás, hasmenés, amelyek általában enyhék; cholecystitis, ritkán bél-iszkémia következtében ileus vagy obstrukció alakulhat ki.
Henoch–Schönlein purpura (HSP)
A Henoch–Schönlein purpura az IgA-depozíció által kiváltott, leggyakoribb szisztémás kisérérintettséget okozó vasculitis gyermekeknél. Klasszikus tünetei közé tartoznak a következők: a tapintható purpura, az ízületi fájdalmak, a vesebetegség és a hasi fájdalom (leggyakrabban periumbilicalis), ritkábban manifeszt vagy okkult GI-vérzés, esetleg intussusceptio jelentkezhet.
(Eosinophil granulomatosus vasculitis (Churg–Strauss-szindróma)
Eosinophil granulomatosus vasculitisnek is nevezik; tipikusan asztmás, allergiás betegeket érint, és a 30–50 éves korosztályban fordul elő; nem mutat markáns nemi különbséget. A betegség jellegzetessége az eosinophil és a granulomatosus, nekrotizáló vasculitis. Felső gasztrointesztinális manifesztációi az eosinophil gastroenteritis, a hasi fájdalom, a GI-vérzés, a hányinger és hányás, valamint az ulceratiók és perforáció a mesenterialis vasculitis következtében, illetve ritkán cholecystitis.
Granulomatosis és polyangitis (Wegener-granulomatosis)
A Wegener-granulomatosis egy szisztémás autoimmun betegség, amelynek alapja a kis artériák és vénák nekrotizáló vasculitise, granulomák képződésével. Főként a felső és az alsó légutakat, valamint a veséket érinti, de ritkán gasztrointesztinális tünetei is előfordulhatnak.
Felső gasztrointesztinális manifesztációk a gingivitis, a szájüregi ulcusok, a gyomor-bél traktus fekélyei tápcsatornai vérzéssel, perforációval. Pancreatitis és biliaris obstrukció is előfordult dokumentáltan a vasculitis következtében.
Behçet-kór
A Behçet-kór egy ismeretlen eredetű, pervazív vasculitis, amely fiatal egyéneket érint, bár minden életkorban előfordulhat. A betegség klasszikus jelei közé tartoznak az ismétlődő orális és genitális fekélyek, valamint az uveitis, de egyéb szervek (így az idegrendszer, az ízületek, a vesék és a gasztrointesztinális traktus) is érintettek lehetnek.
Felső gasztrointesztinális manifesztációk
- Orális fekélyek: Gyakran fájdalmas, sekély, kerek vagy ovális fekélyek, amelyek csoportosan jelennek meg.
- Nyelőcső és gyomor: Bár a nyelőcsőben ritkábban fordulnak elő fekélyek, a gasztrointesztinális érintettség bárhol kialakulhat a szájüregtől a végbélig.
- Hasnyálmirigy: Ritka esetekben hasnyálmirigy-gyulladás alakulhat ki, amely a vasculitis következménye lehet.
Gasztroenterológiai gyakorlat vonatkozása
Gasztrointesztinális megjelenését gyakran keverik össze gyulladásos bélbetegségekkel (M. Crohn).
Következtetések
A szisztémás autoimmun betegségek gasztrointesztinális manifesztációi összefüggésben állhatnak gyulladásos folyamatokkal, keringési szövődményekkel, valamint a motoros és a szekretoros funkciók kóros eltéréseivel, változatosak és viszonylag gyakran jelennek meg szövődményként. A betegek életminőségét és a betegség kimenetelét is szignifikánsan befolyásolhatják. A gasztrointesztinális szövődmények (mint például az orális fekélyek, a súlyos béliszkémia, ulceratiók, a perforáció vagy a tápcsatornai vérzés) jelentős morbiditást és emelkedő mortalitást eredményeznek, különösen a diagnózis felállításának késlekedése esetén. A korai diagnózis felállításában fontos szerepe van a tápcsatornai manifesztációt észlelő gasztroenterológusoknak, valamint a tünetorienteált kivizsgálás keretében meghatározott autoimmun szeropozitivitás vizsgálatának (9, 10). A klinikai kivizsgálás során a beteg panaszainak alapos felmérése mellett endoszkópos, radiológiai és szövettani vizsgálatokra is szükség van ahhoz, hogy a gasztrointesztinális érintettség pontos okát (legyen az a primer autoimmun folyamat vagy a gyógyszeres terápia mellékhatása) azonosítani lehessen. A kezelési stratégiák az adott kórkép patofiziológiájára épülnek: az immunszuppresszív terápiák (kortikoszteroidok, ciklofoszfamid, mikofenolát mofetil stb.) mellett a szimptomatikus támogatás (savszekréció-gátlók, prokinetikumok, táplálkozási támogatás) is létfontosságú. A különböző szakterületek (reumatológusok, gasztroenterológusok, patológusok és egyéb szakemberek) közötti együttműködés segíti a beteg optimális ellátását és a komplikációk megelőzését.
Irodalom
2. Conrad N, Misra S, Verbakel JY, Verbeke G, et al. Incidence, prevalence, and co-occurrence of autoimmune disorders over time and by age, sex, and socioeconomic status: a population-based cohort study of 22 million individuals in the UK. Lancet 2023; 401(10391): 1878–1890.
https://doi.org/10.1016/S0140-6736(23)00457-9. PMID: 37156255.
3. Yadlapati R, et al. Esophageal motility disorders on high-resolution manometry: Chicago classification version 4.0©. Neurogastroenterol Motil 2021; 33(1): e14058. https://doi.org/10.1111/nmo.14058. Erratum in: Neurogastroenterol Motil 2024 Feb; 36(2): e14179. https://doi.org/10.1111/nmo.14179 PMID: 33373111; PMCID: PMC8034247.
4. Li Z, Xu D, Wang Z, Wang Y, et al. Gastrointestinal system involvement in systemic lupus erythematosus. Lupus 2017; 26(11): 1127–1138. https://doi.org/10.1177/0961203317707825. Epub 2017 May 19. PMID: 28523968.
5. Alharbi S. Gastrointestinal Manifestations in Patients with Systemic Lupus Erythematosus. Open Access Rheumatol 2022 Oct; 14: 243–253. https://doi.org/10.2147/OARRR.S384256 PMID: 36281321; PMCID: PMC9587305.
6. Sultan SM, Ioannou Y, Isenberg DA. A review of gastrointestinal manifestations of systemic lupus erythematosus. Rheumatology (Oxford) 1999; 38(10): 917–32.
https://doi.org/10.1093/rheumatology/38.10.917 PMID: 10534541.
7. Sultan SM, Ioannou Y, Isenberg DA. A review of gastrointestinal manifestations of systemic lupus erythematosus. Rheumatology (Oxford) 1999; 38(10): 917–32. https://doi.org/10.1093/rheumatology/38.10.917. PMID: 10534541.
8. Ceccato F, Salas A, Góngora V, Ruta S, et al. Chronic intestinal pseudo-obstruction in patients with systemic lupus erythematosus: report of four cases. Clin Rheumatol; 27(3): 399–402. https://doi.org/10.1007/s10067-007-0760-5. Epub 2007 Oct 16. PMID: 17938989.
9. Zádori N, Németh D, Szakó L, Váncsa S, et al. Prevalence of Autoimmune-phenomena behind Chronic Gastritis of Unknown Origin, and their Role in the Poor Histological Outcome of the Stomach: A Single-centre, Retrospective Cross-sectional Study. J Gastrointestin Liver Dis 2022; 31(2): 168–175. https://doi.org/10.15403/jgld-4218. PMID: 35574624.
https://doi.org/10.2147/IJGM.S380419 PMID: 36258798; PMCID: PMC9572481.
