Viral hepatitis in pregnancy
Summary
Different liver and biliary tract diseases can be pregnancy-related disorders, or pre-existing, concurrent liver diseases, occur at different time of pregnancy leading to maternal and fetal morbidity and mortality. Viral hepatitis caused morbidity and mortality is significant health care problem. Pregnancy doesn’t affect the progression of viral hepatitis, with mild, aspecific symptoms, except hepatitise E caused high morbidity and mortality, and herpes simplex caused fatal liver failure in the 3rd trimester of pregnancy. Preterm delivery, complications can occur, but the importance of vertical and perinatal transmission is higher, Cytomegalovirus caused congenital abnormalities are severe. Authors review the knowledge of primary and main non primary hepatotrop viruses, with emphasizing the possibilities of decreasing the risk of perinatal transmission.
Várandósság alatt a máj- és az epeúti betegségek különböző formáival találkozhatunk, amelyek a terhességgel kapcsolatos sajátos, esetleg azzal összefüggésbe hozható, vagy attól teljesen független kórképek is lehetnek, amelyek a várandósság különböző időszakában léphetnek fel, anyai és magzati megbetegedéshez, valamint halálozáshoz vezethetnek. A vírushepatitisek okozta megbetegedések és halálozás jelentős népegészségügyi problémát képviselnek. A terhesség általában nem befolyásolja a vírushepatitis lefolyását, gyakran enyhe, jellegtelen tüneteket okoz, amely alól a hepatitis E-fertőzés okozta magas morbiditás és mortalitás és a herpes simplex a terhesség harmadik trimeszterében okozta fatális májelégtelenség jelent kivételt. A fertőzésekkel kapcsolatban koraszülésről, szülészeti komplikációkról beszámolnak, de a vertikális és a perinatális átvitel jelentősége nagyobb, a Cytomegalovírus-fertőzés okozta kongenitális következmények súlyosak. Szerzők a primer és a jelentősebb nem primer hepatotrop vírushepatitisekkel kapcsolatos ismereteket foglalják össze, kitérve a perinatális átvitel csökkentésének lehetőségeire.
Bevezetés
A várandósság parafiziológiás állapot, amely alatt a máj- és az epeúti betegségek különböző formáival találkozhatunk. Ezek a terhességgel kapcsolatos sajátos (hyperemesis gravidarum, intrahepaticus terhességi cholestasis, akut terhességi zsírmáj, HELLP-szindróma: hemolízis, elevated liver enzymes and low platelet count, májruptúra, vérzések), valamint a terhességgel esetleg összefüggő máj- és epebetegségek (epekőbetegség, akut cholecystitis, Budd–Chiari-szindróma), valamint a várandósság alatt jelentkező, a terhességre nem specifikus, attól teljesen független kórképek (vírushepatitisek, Dubin–Johnson–Rotor-szindróma, autoimmun hepatitisek, tárolási betegségek) is lehetnek, amelyek a várandósság különböző időszakában léphetnek fel, jelentős anyai és magzati megbetegedéshez, illetve halálozáshoz vezethetnek. Egyre több tapasztalattal rendelkezünk a májtranszplantáción átesett, immunszuppresszív kezelésben részesülő várandósokkal kapcsolatban is. A legtöbb gyógyszerhatóanyag ellenjavallt terhességben teratogén hatása miatt, de minden esetet egyénileg kell mérlegelni, a szülés megindítása, még idő előtt is, befolyásolja a betegség progresszióját (1, 2).
A vírushepatitisek okozta morbiditás és mortalitás jelentős, több mint 400 millió fertőzést és évente 1,4 millió halálozást okoznak. A vírushepatitisek heveny és idült formája ismert. Kórokozóként elsősorban a hepatotrop vírusok jönnek szóba hepatitis A-vírus (HAV), hepatitis B-vírus (HBV), hepatitis C-vírus (HCV), hepatitis D- (delta) vírus (HDV), hepatitis E-vírus (HEV), amelyeknek előfordulása nem gyakoribb várandósság alatt. Ezen kívül számos szisztémás vírus- (Cytomegalovírus, Epstein–Barr-vírus, Coxsackie-vírus, sárgaláz vírusa, herpes simplex vírus), baktérium- (Salmonella enterica, Mycobacterium tuberculosis, brucellosis, Coxiella burnetii, Borrelia burgdorferi), parazita- (schistosomiasis, malaria) vagy gombafertőzés (Candida) okozhat májkárosodást, előfordulásuk kevésbé gyakori terhesség alatt (1, 2, 3).
Az akut vírushepatitis a sárgaság leggyakoribb oka terhességben, általában a lefolyás jóindulatú, de a cholestasis a gyermekágyig fennáll, legjelentősebb következménye a vertikális transzmisszió lehetősége. Az akut hepatitis szindróma tünettanára jellemző a jellegtelen kezdet, a gyengeség, az étvágytalanság, az émelygés, a hányinger, a hányás, az izomfájdalom, a láz, a sárgaság, valamint a jobb bordaív alatti fájdalom. A szérum-bilirubinszint kóros értéke mellett jelentős (10–100 szoros) a transzamináz enzimek emelkedése. Súlyos, fulmináns formákban, az akut májelégtelenség kialakulásakor a parenchymás és/vagy vaszkuláris dekompenzáció klinikuma van jelen, a májenzimek emelkedett szintje, sárgaság, coagulopathia, ödémaképződés, ascites kialakulása mellett. Az első trimeszterben a hepatitisvírus-fertőzéseknek teratogén hatásuk nincs. A Cytomegalovírus okozta fertőzéstől eltekintve a kongenitális rendellenességek kockázatát nem növelik, koraszüléshez, szülészeti komplikációkhoz vezethetnek. A pontos diagnózist a vírusszerológiai vizsgálatok alapján állíthatjuk fel. A heveny vírushepatitisek általában jó gyógyhajlamúak, oki kezelés nincs, tüneti terápia javasolt (1).
Az idült hepatitisek klinikai képe még jellegtelenebb, gyakran aszimptomatikusak, a tünetek (fáradékonyság, rossz közérzet, étvágytalanság, visszatérő hőemelkedés, jobb bordaív alatti fájdalom, hasi diszkomfortérzés) enyhék vagy hullámzóak lehetnek.
A HAV- és HEV-fertőzés leggyakrabban akut, az esetek egy részében sárgasággal járó hepatitist okoz. A HAV okozta fertőzésnek idült formája nem ismert, a HEV a legújabb adatok alapján immunszupprimáltakban idült fertőzést okozhat. A HBV, HCV és HDV ezzel szemben gyakran okoz idült hepatitist.
Primer hepatotrop vírusok
Hepatitis A
Az emberi akut vírushepatitisek leggyakoribb kórokozója. Világszerte 1,4 millió új esetet jelentenek, bár előfordulása alulbecsült az enyhe tünetek miatt. Endémiás a fejlődő országokban, a rossz szociális körülmények között élőkben, ahol elsősorban a gyermekek fertőződnek meg. A fejlett országokban ezzel szemben az A-vírus okozta hepatitis felnőttekben gyakoribb, és jellegzetes utazási megbetegedésnek számít (4). A terhességi hepatitisek kevesebb, mint 2%-áért felelős, 1/1000 terhes nőt érint (5).
Terhességben a betegség lefolyása nem súlyosabb, de a vetélés és a koraszülés gyakoribb, főleg a második, harmadik trimeszteri fertőzések esetén. Beszámoltak egyéb szülészeti szövődmények (idő előtti kontrakciók, vérzés, abruptio placentae) gyakoribb előfordulásáról is (4, 5).

A betegeket fertőző osztályon kell elhelyezni, mert a környezetüket veszélyeztetik, továbbá az esetek 1%-ában atrophia hepatis flava alakulhat ki, és intenzív kezelés bevezetése válhat szükségessé (2).
Intrauterin, illetve perinatálisan a magzat is fertőződhet. Az anya akut A-hepatitise nem jár együtt a magzat károsodásával, egy-egy esetben számoltak be a magzatban ascites, meconium peritonitis, distalis ileumperforáció kialakulásáról. Szoptatás során átvitele nem ismert, ezért a fertőzött anyánál a szoptatás felfüggesztése nem indokolt, az újszülöttet passzív vagy aktív vakcinációban indokolt részesíteni (4, 6).
A megelőzésre hatékony védőoltás áll rendelkezésre, inaktivált vírusvakcina, amely 2 oltásból áll (0. és 6-12/18. hónap), a szerokonverzió aránya 95% feletti. Az inaktivált vakcinát az FDA C-osztályúnak minősítette terhességben. Amennyiben a várandós hepatitis A-vírussal fertőzött beteggel kerül közvetlen érintkezésbe, ha korábban nem oltották, legkésőbb két héten belül indokolt passzív immunizálása, amely biztonságos, nincs magzatra gyakorolt hatása. A higiénés rendszabályok betartása kiemelkedő jelentőségű a fertőzés terjedésének megállításában (4, 5).
A terhesség megszakítása, illetve a császármetszés nem indokolt. A szülés előtt 48 órával a magzat fertőződése immunglobulin adásával előzhető meg (1).
Hepatitis B
Világszerte kb. 350 millió a HBV-fertőzött, másfél milliárd a fertőzésen átesettek száma, többségük Távol-Keleten és Afrikában él. Hazánkban 0,5-0,7, Európában 0,5-2% a HBsAg-pozitivitás.
A nem parenterális terjedés módjai közül legjelentősebb a szexuális kapcsolat és a vertikális átvitellel járó perinatális fertőzés, amely leggyakrabban a szülés alatt jön létre. In utero fertőzés csak az esetek 10%-ában lép fel. A szülés alatti átvitel kockázatát a nagy vírusszám és a HBeAg-pozitivitás növeli (1, 7). A vertikális és a perinatális transzmisszióra a placentabetegségek és a szülési komplikációk hajlamosítanak (1). A neonatális fertőzés általában tünetmentes, és az esetek 90%-ában idült fertőzéssé alakul (7).
A terhesség nem befolyásolja a heveny és az idült HBV-fertőzés lefolyását, ritkán alakul ki fellángolás, májelégtelenség, speciális antivirális kezelése nincs (1, 7).
A fertőzés általában nem befolyásolja az anyai és a magzati morbiditást és mortalitást, de beszámoltak gyakoribb koraszülésről, alacsonyabb születési súlyról és intrauterin elhalásról is (7). Cirrózisos anyánál a perinatális szövődmények és az anyai kimenetel rosszabb (placentaabrupció, gesztációs hipertónia, peripartum haemorrhagia) (7).
A terhesség alatt a várandósok HBsAg-szűrővizsgálata kötelező. Magyarországon az anyák 0,5%-1%-a HBV-hordozó. HBsAg-pozitív várandósoknál HBV-PCR-vizsgálat javasolt. HBeAg-pozitív anyáknál a vertikális transzmisszió gyakori (50-80%, vs. HBeAg-negativitás: 10-40%), antiHBe-pozitivitás esetén a kockázat kisebb, 25%, aszimptomatikus hordozóknál 5% (1, 7). Az akut exacerbáció kockázata miatt szülés után – az addig kezelést nem igénylő – HBsAg-pozitív nők esetében is szoros obszervációja javasolt (8).
Amennyiben a vírustiter több, mint 200 000 IU/ml, a várandósnál tenofovir-kezelést kell kezdeni a 24–28. hét között, amely a szülést követően 12 hétig folytatandó. A szoptatás nem ellenjavallt HBsAg-pozitív, illetve tenofovir-kezelésben részesülő kismamáknak. Az interferon, pegilált interferon teratogenitása miatt ellenjavallt (1, 7, 8, 9).
HBsAg-pozitív anya esetén az újszülöttet védőoltásban kell részesíteni: a szülést követő 0-12 órán belül 200 IE anti-HBs immunglobulin adandó, legkésőbb – a szülést követő egy héten belül – rekombináns HBV-vakcina első dózisának beadása szükséges, a következőket 1, majd 6 hónap múlva kell az újszülöttnek, csecsemőnek megkapnia. Ilyen módon az újszülöttek kb. 85%-a hatékony megelőzésben részesül (1, 2, 7).
Az anya HBsAg-pozitivitása esetében a családtagokat, a szexuális partnert is ajánlatos szűrni, és szükség esetén védőoltásban részesíteni (2).
Hepatitis C
A WHO legújabb adatai szerint az idült HCV-fertőzöttek száma 71 millió világszerte (10). A fertőzöttség hazánkban kb. 0,7–1%. Magyarországon körülbelül 50 000-re becsülhető a HCV-RNS-pozitív egyének száma (12). A terhes nők 1-2%-a fertőzött Európában és az USA-ban, de néhány fejlődő országban a 8%-ot is elérheti, a pontos adat nem ismert (1). Egyiptomban a cirkumcízió, valamint a schistosomiasis kezelése következtében az anti-HCV-poztivitás nagy, 15,5%, 35 év feletti nőkben 30% (13).
A HCV parenterális átvitellel fertőz, a betegek többsége 1993 előtti transzfúzióval vagy más egészségügyi beavatkozás során fertőződött meg. Napjainkban az intravénás kábítószerek használata és/vagy a férfi homoszexualitás (men who have sex with men, MSM) tekinthetők fő veszélyforrásnak. A fejlődő, illetve a közepes fejlettségű országokban a nozokomiális ellátás során átvitt HCV-fertőzés is gyakori (11).
Terhességben az anya HCV-fertőződésének jellemző útja az intravénás droghasználat. A fertőzött vérkészítmény, transzfúzió az esetek 11%-áért felelős. A fertőzött kismamák 40-70%-ának nem ismert kockázati tényezője (14).
A heveny HCV-hepatitis enyhe, a terhesség lefolyását nem befolyásolja. Teratogén hatása nincs. A vertikális átvitel kockázata 5-10% (1, 15). A HCV-fertőzést a gesztációs diabétesszel, a koraszüléssel, valamint az alacsony születési súllyal összefüggésbe hozták (14). Idült HCV-fertőzött terhesekben az átlagos aminotranszamináz-aktivitás kisebb, amelynek hátterében a placenta és a faetus által termelt interferon, a hemodilúció, az immuntolerancia, az immunszuppresszív citokinek termelődése állhat. Posztpartum rebound figyelhető meg, néhány esetben számoltak be terhesség alatti exacerbációról (1, 13). HBV- és HCV-koinfekció a szülés alatti vérzés kockázatát növeli.
A perinatális átvitel kockázatát a magas (>106/ml9) anyai vírusszám, a belső magzati monitorozás, az amniocentesis, az alkohol- és a drogabúzus növelik. A fertőzés történhet a placentán át (transcytosis, a mononukleáris sejtek szállítása, a trophoblastok fertőződése, valamint a placenta károsodása által), de gyakoribb a szülés kapcsán. Elhúzódó szülés, a HIV-koinfekció a transzmisszió arányát 4-5-szörösére emeli (19,4%). A császármetszés átvitelt megelőző szerepe azonban nem igazolt. Leánymagzatok vertikális fertőződésének esélye nagyobb. Más tényezők, mint pl. az anyai életkor, paritás, genotípus szerepe nem bizonyított. A terhességi intrahepaticus cholestasis nagyobb kockázatáról számoltak be HCV-fertőzésben (1, 12, 13, 14).
A klinikai, laboratóriumi és virológiai leletekkel igazolt heveny C-hepatitis terápiája tüneti. Az akut fázisban kórházi elhelyezésre a pihenés biztosítása, tüneti kezelés és a betegek környezetében élő személyek védelme miatt, elkülönítés céljából van szükség. A ritka, fulmináns formák időben történő felismerése, kezelése szintén hospitalizációt, intenzív osztályos kezelést indokol (2).
A szoptatás során, valamint a családtagok között a nem szexuális átvitel elhanyagolható. Az anya C-vírus-pozitivitásakor a szoptatás nem ellenjavallt, a mellbimbó berepedése, vérzése, HIV-koinfekció esetén azonban a szoptatás felfüggesztése megfontolandó (12, 14).
Anti-HCV-pozitív anya gyermekénél 18 hónapos korban anti-HCV-vizsgálat, pozitív esetben HCV-RNS-vizsgálat végzendő. A gyermek egy-két hónapos korában szűrésként HCV-RNS végezhető (2).
A korábbi, terhesség alatt ellenjavallt interferon-, pegilált interferon-, ribavirinkezelést hatékonyabb, biztonságosabb, szájon át, rövidebb ideig adható, közvetlenül a vírusra ható, direkt antivirális készítmények váltották fel. Az új típusú direkt antivirális készítmények sem alkalmazhatóak terhesség alatt. Krónikus C-hepatitisben szenvedő várandósok kezelése a szülés és szoptatás utánra halasztandó (12). Spontán gyógyulást figyeltek meg a posztpartum periódusban (1).
Aktív vagy passzív védőoltás, tekintettel a vírus változékonyságára, jelenleg nem áll rendelkezésünkre (5).
Együttes HCV-HIV-fertőzés
Kb. 40 millióan fertőzöttek HIV-vel és 4,5 millióan mindkét vírussal. A koinfekció főleg Szub-Szaharai Afrikában jelentős. A HCV-fertőzés gyakoribb HIV-fertőzött terhesekben. A korábbi intravénás droghasználat a fő kockázati tényező. HIV-koinfekció a HCV-fertőzés vertikális transzmissziójának arányát tovább (4-5×) növeli terhességben, amely a HIV okozta immunszuppresszió következtében kialakuló nagyobb viraemia következménye. A HCV-koinfekció a HIV-átvitel esélyét nem befolyásolja. Terhesség alatti antiretrovirális kezelés eredményeképpen az esetek 75%-ában nem detektálható HIV-RNS a szüléskor, a HCV-RNS-koncentráció csökkentésével a transzmisszió esélyét mérsékli, ugyanakkor a HCV-fertőzés az antiretrovirális kezelés hepatotoxicitásának esélyét növeli (16, 17).
Hepatitis D
A HDV csak a HBsAg-vel együtt képes fertőzni, vagy idült HBV-fertőzésben szenvedő egyént képes megbetegíteni. Endémiás területeken (mediterrán országok, pl. Dél-Olaszország, Görögország) szoros személyi kontaktus útján terjed. Nem endémiás vidékeken főleg vérrel, vérkészítményekkel, parenteralisan vihető át.
A HBV/HDV koinfekció, valamint a HDV-fertőzés lefolyását a terhesség nem befolyásolja. Akut vagy krónikus hepatitis B reaktivációja esetén gondolni kell rá. Ritka. Vertikális transzmisszó nem bizonyított, a szülés megindítása nem indokolt. A szoptatás biztonságos. A HBV immunprofilaxis a vertikális transzmissziót megelőzi (1, 6).
Hepatitis E
A hepatitis E-vírus (HEV) fertőzés leggyakrabban enterális úton (faecooralisan) történik fertőzött vízzel, élelmiszerrel, a 3-as és a 4-es genotípus zoonozis, fertőzött házi sertéshús, illetve vaddisznó fogyasztásával akvirálható (18). A rosszabb szociális és gazdasági körülmények között élő országokban, Afrika, Ázsia, Közép-Amerika, gyakoribb. A HEV incidenciája, főleg a 3-as genotípusé, nő Európában. A HEV fokozott morbiditással és mortalitással jár együtt és halálos kimenetelű lehet várandós asszonyokban, amelynek az alultápláltság és a rossz szociális körülmények kedveznek (1). Endémiás területeken 60%-ban fulmináns májelégtelenség alakulhat ki, 31%-os halálozással (6).
Az anti-HEV szeroprevalencia 5–10%-os az egészséges felnőttek között. A terhesség első trimeszterében 1,5%, a második trimeszterben 8,5%, a harmadikban a HEV-fertőzés 10–20%-ban halálos kimenetelű az anyában az akut májelégtelenség, az eclampsia és a haemorrhagia következtében. Heveny HEV-fertőzésben a vertikális átvitel 50%, a magzat is súlyosan károsodhat, gyakori a magzatelhalás, az újszülöttekben hepatitis, hypothermia, hypoglykaemia alakul ki (1).
A heveny E-hepatitis kezelése tüneti. Fulmináns formákban intenzív osztályon való kezelés szükséges. A ribavirin teratogenitása miatt nem alkalmazható. Krónikus hepatitisbe történő átmenet bizonyított. Az általános higiénés rendszabályokon kívül mind ez ideig passzív vagy aktív immunprofilaxis nem áll rendelkezésünkre (1, 2, 6).
Egyéb, nem hepatotrop vírusok által okozott akut hepatitisek
A heveny hepatitis szisztémás vírusfertőzés részjelensége is lehet, primeren nem hepatotrop vírusok is létrehozhatják. A klinikai kép hasonló a primer hepatoptrop vírusoknál leírtakhoz, a pontos etiológiai diagnózist vírusszerológiai vizsgálatokkal állíthatjuk fel.
Cytomegalovírus
A korábban Cytomegalovírus-fertőzésen még nem átesett anyák 1,4%-a fertőződhet a terhesség során, a reaktiváció esélye 10% a várandósság alatt. Az anyai fertőzés gyakran aszimptomatikus, vagy jellegtelen tünetei lehetnek: láz, fáradtság, izomfájdalom, fejfájás, orrfolyás. A Cytomegalovirus-fertőzés vertikális átadásának magzati következményei jelentősek, de a terhesség lefolyását nem befolyásolja (15).
Az anya-magzati átvitelnek a kockázata az első, a magzati károsodás esélye a harmadik trimeszterben nagyobb. A fertőződés létrejöhet a méhlepényen keresztül, a cervicovaginalis váladék aspirációjával, a szoptatás során, vagy ritkán a genitáliáról aszcendálva. A CMV a leggyakoribb kongenitális vírusfertőzés, születéskori prevalenciája 0,5% (0,2–2,5%), az érintett újszülöttek halálozása 5%, központi idegrendszeri érintettséget, hallásvesztést okozhat (15).
Terhesség alatt nincs speciális terápiás lehetőség, immunglobulin és valacyclovir adása a vertikális átvitel esélyét csökkentik és így a magzati kimenetelt előnyösen befolyásolhatják, de alkalmazásuk egyelőre nem alátámasztott (19).
Herpes simplex vírus
A HSV szeroprevalenciája terhességben 72%. A herpes simplex (HSV-1, HSV-2) okozta vírushepatitis ritka, de gyakran fatális akut májelégtelenséget okozhat, főleg a harmadik trimeszterben, amelyben szerepet kap a várandós anyák csökkent celluláris immunválasza is. Spontán abortuszt, intrauterin növekedési retardációt, idő előtti szülést okozhat. A terhességben fellépő herpes simplex hepatitis mortalitása nagyobb, mint 80%, a betegség gyakran fokális és konfluáló haemorrhagiás és koagulációs necrosist okoz a májban. 90%-ban anicterusos. Jellemzője a magas transzaminázérték, a normális vagy enyhén emelkedett szérum-bilirubinszint, gyakran a típusos bőr-nyálkahártya léziók nélkül (a vulván, vaginában és cervixen gyakran láthatók herpeses erupciók). Szerológiai tesztek eredménye a kórismét megerősíti (HSV-IgM, HSV-PCR), a vírusszint a transzamináz-értékekkel a betegség súlyosságát jelzi. A szerokonverzió 2% (2, 15).
Az újszülött fertőzésének esélye késő terhességben 30-50%, korai terhességben történt fertőződés esetén kevesebb, mint 1%, transzplacentárisan vagy aszcendáló módon jöhet létre, perinatálisan az újszülött 80-90%-ban a szülés során fertőződik. A neonatalis HSV-fertőzés tünetei bőr-, szem-, szájléziók, a központi idegrendszeri érintettség és a disszeminált betegség, amelynek halálozása kezeletlen esetekben a 80%-ot is meghaladja. Neurológiai maradványtünetekként vakság, görcsök, tanulási nehézsége maradhat vissza (15).
A fertőzött anyától származó újszülöttek szoros megfigyelése és szükség esetén azonnali kezelése indokolt. A betegség kezelése acyclovirral és vidarabinnal történhet, a császármetszés az újszülött szülés közben történő fertőződésének kockázatát csökkenti (1, 2).
Következtetések
A várandósság speciális klinikai állapot számos fiziológiás változással, amelyek közül több a májat is érintheti. A májbetegségek mind a várandós, mind a magzat, az újszülött megbetegedésére hatással van. A vírushepatitisek a terhességtől független kórképek, amelyek a várandósság különböző időszakában léphetnek fel, általában tünetszegény formában zajlanak mind heveny, mind idült fertőzéskor, ugyanakkor a HEV-fertőzés jelentős anyai és magzati megbetegedést és halálozást okoz, a herpes simplex a terhesség harmadik trimeszterében okozta fatális májelégtelenséget eredményez. Cytomegalovírus-fertőzés kongenitális következményei súlyosak (2. táblázat).

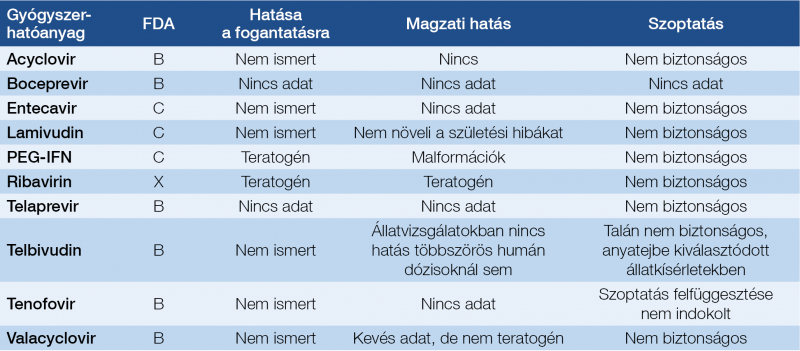
Más vírussal történő együttes fertőzés az anyai fertőzést befolyásolja, a magzati fertőzés esélyét növeli. A laboratóriumi paraméterek terhességben fiziológiás eltérései nem könnyítik meg a kórisme felállítását. A szerológiai markerek változásai alapján a diagnózis felállítható, ha gondolunk rá. A speciális antivirális kezelést azok teratogén hatása korlátozza, így kevés kivételtől eltekintve nem alkalmazzuk őket (3. táblázat). Nagy szerepe jut a megelőzésnek a perinatális átvitelben, a császármetszés bizonyos esetekben az átvitel lehetőségét csökkenti. A szoptatást a vírusfertőzés nem ellenjavallja
2. Lengyel G, Fehér J. Vírushepatitisek. In Hepatológia (Szerk.: Fehér J, Lengyel G.) Budapest: Medicina Könyvkiadó Rt.; 2001. p. 492–538.
3. Talwani R, Gilliam BL, Howell C. Infectious Diseases and the Liver. Clin Liver Dis 2011; 15: 111–130.
4. Chaudhry SA, Koren G. Hepatitis A infection during pregnancy. Can Fam Physician 2015; 61: 963–694.
5. Zhao Y, Jin H, Zhang X, et al. Viral hepatitis vaccination during pregnancy. Hum Vaccin Immunother 2016; 12: 894–902.
6. Almashhrawi AA, Ahmed KT, Rahman RN, et al. Liver diseases in pregnancy: diseases not unique to pregnancy. World J Gastroenterol 2013; 19: 7630–7638.
7. Piratvisuth T. Optimal management of HBV infection during pregnancy. Liver Int 2013; 33 (Suppl 1): 188–194.
8. Horváth G, Gerlei Zs, Gervain J, et al. A hepatitis B- és D-vírus-fertőzés diagnosztikája, antivirális kezelése Magyar konszenzusajánlás Érvényes: 2017. szeptember 22-től. Orv Hetil 2018; 159(Suppl 1): 24–37.
9. European Association for the Study of the Liver. EASL 2017 Clinical Practice Guidelines on the management of hepatitis B virus infection. J Hepatol 2017; 67: 370–398.
10. http://www.who.int/news-room/fact-sheets/detail/hepatitisc
11. Hagymási K, Lengyel G. A hepatitis C vírus epidemiológiája, a fertőzés átvitelének lehetőségei. LAM 2014; 24: 253–257.
12. Hunyady B, Gerlei Zs, Gervain J, et al. A hepatitis C-vírus-fertőzés szűrése, diagnosztikája, antivirális terápiája, kezelés utáni gondozása Magyar konszenzusajánlás Érvényes: 2017. szeptember 22-től. Orv Hetil 2018; 159(Suppl 1): 3–23.
13. Floreani A. Hepatitis C and pregnancy. World J Gastroenterol 2013; 19(40): 6714–6720.
14. Prasad MR, Honegger JR. Hepatitis C virus in pregnancy. Am J Perinatol 2013; 30(2): 149–159.
15. Silasi M, Cardenas I, Kwon JY, et al. Viral infections during pregnancy. Am J Reprod Immunol 2015; 73: 199–213.
16. Checa Cabot CA, Stoszek SK, Quarleri J, et al; NICHD International Site Development Initiative Perinatal/Longitudinal Study in Latin American Countries Study Group. Mother-to-Child Transmission of Hepatitis C Virus (HCV) Among HIV/HCV-Coinfected Women. J Pediatric Infect Dis Soc 2013; 2: 126–135.
17. Snijdewind IJ, Smit C, Godfried MH, et al. HCV coinfection, an important risk factor for hepatotoxicity in pregnant women starting antiretroviral therapy. J Infect 2012; 64: 409–416.
18. Pavio N, Meng XJ, Doceul V. Zoonotic origin of hepatitis E. Curr Opin Virol 2015; 10: 34–41.
19. Society for Maternal-Fetal Medicine (SMFM), Hughes BL, Gyamfi-Bannerman C. Diagnosis and antenatal management of congenital cytomegalovirus infection. Am J Obstet Gynecol 2016; 214: B5–B11.
