Reviews
Quality indicators for colonoscopy in inflammatory bowel disease patients
Summary
In inflammatory bowel diseases, ileo-colonoscopy is one of the most important diagnostic techniques, and its quality is crucial for effective treatment. While the adenoma detection rate is one of the most important endoscopic indicators for screening colonoscopies, knowing and adhering to different quality indicators at different stages of inflammatory bowel disease guarantees a good outcome. In addition to describing the specific criteria, this review article places particular emphasis on the specificities of bowel preparation, disease activity scoring systems, and the challenges of colonoscopy reporting in inflammatory bowel disease.
Összefoglalás
A gyulladásos bélbetegségek esetén az ileokolonoszkópia az egyik legfontosabb diagnosztikus módszer, amelynek megfelelő minőségben történő elvégzése kulcsfontosságú az eredményes kezelés szempontjából. Míg a szűrő kolonoszkópiák esetén az adenomadetekciós ráta az egyik legfontosabb mérőszáma az endoszkópiának, a gyulladásos bélbetegség különböző szakaszaiban eltérő minőségi mutatók ismerete és betartása garantálja a megfelelő végeredményt. Az összefoglaló közlemény a speciális kritériumrendszer ismertetésén túl különös hangsúlyt helyez a bélelőkészítés, az aktivitási pontrendszerek és a leletírás sajátosságaira a gyulladásos bélbetegekben végzett vastagbéltükrözés kapcsán.
Bevezetés
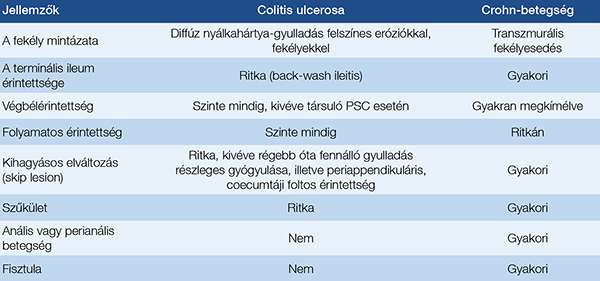
A gyulladásos bélbetegségek (inflammatory bowel diseases, IBD) két fő megjelenési formája a fekélyes vastagbélgyulladás (ulcerative colitis, UC) és a Crohn-betegség (Crohn’s disease, CD). Mivel az UC minden esetben a végbél és a vastagbél különböző hosszúságú szakaszának a megbetegedése, a CD pedig az esetek 80-85%-ban az ileokolonoszkópia során elérhető lokalizációban fordul elő (1), a vastagbéltükrözés az IBD diagnosztizálásának továbbra is az egyik kulcsfontosságú eszköze, amely nemcsak a diagnózis felállítására, hanem a betegség aktivitásának és a kezelés hatékonyságának nyálkahártyaszintű megítélésére, a rákmegelőző állapotok azonosítására is alkalmas. Ezenkívül terápiás potenciálja van – mint minden egyéb indikáció esetén is –, hiszen lehetővé tesz olyan terápiás beavatkozásokat, mint a diszplasztikus léziók, korai daganatok endoszkópos reszekciója és a rövid szakaszú szűkületek tágítása (2). Tekintettel arra, hogy a CD gyakran érinti a terminális ileumot, illetve minden negyedik Crohn-betegben csak a vékonybélben fordul elő, döntő fontosságú, hogy a kolonoszkópia során a vizsgáló az ileumba is bejusson. Bár jelen közleménynek nem célja a két betegség endoszkópos jellemzőinek taglalása, az 1. táblázat egy rövid áttekintést nyújt a differenciáldiagnosztikai jellemzőkről (3).
Fontos megjegyezni, hogy akkor végezzünk endoszkópiát, ha annak a betegre nézve relevanciája, következménye van: a diagnózissal a birtokunkban elkezdődik a megfelelő kezelés, az endoszkópos kép alapján terápiás döntés születik, kizárjuk vagy megerősítjük a rákos átalakulás lehetőségét a következő években, illetve terápiás intervencióra kerül sor. Kiemelt fontosságú azonban az is, hogy minden ténykedésünket megfelelően strukturált, részletes, a vizsgálatot nem látó orvos számára is egyértelmű információt hordozó leletben rögzítsük (1. ábra).

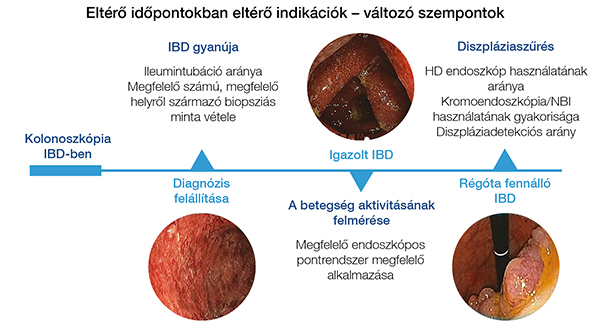
A kolonoszkópiát végző gasztroenterológusok többsége tisztában van a vizsgálat általános minőségi indikátoraival (coecumelérési ráta, adenomadetektálási arány, eszközkihúzási idő stb.), azonban talán kevesebben tudják, hogy az IBD-ben végzett vastagbéltükrözésekre más technikai jellemzők (is) érvényesek. Fontos szempont, hogy eltérő időpillanatban, a betegség lefolyásának különböző szakaszaiban végzett diagnosztikus kolonoszkópia során más válik kulcsfontosságúvá, nem ugyanazon szempontok jellemzik vizsgálatunk minőségét az IBD gyanúja esetén, vagy ha diszpláziaszűrés történik (2. ábra).
A European Society of Gastrointestinal Endoscopy (ESGE) és a United European Gastroenterology (UEG) az utóbbi években a különböző endoszkópos eljárások minőségének javítását és európai szintű harmonizálását tekintette fő céljának, a vastagbéltükrözés kapcsán a premalignus léziók felfedezését, valamint azok megfelelő technikával történő eltávolítását helyezte a középpontba. Ezen szervezetek ajánlásai részben alkalmazhatók az IBD esetén végzett diszpláziaszűrés esetén is, de nyilvánvalóan más kritériumrendszer alkalmazása szükséges az egyéb indikációval végzett vizsgálatok alkalmával. E célból született meg az ESGE ajánlása az IBD-ben elvégzett vastagbéltükrözés minőségi kritériumairól, amelyet 2022-ben publikáltak (4). A minőségi kritériumok összefoglalása a 3. ábrán látható.
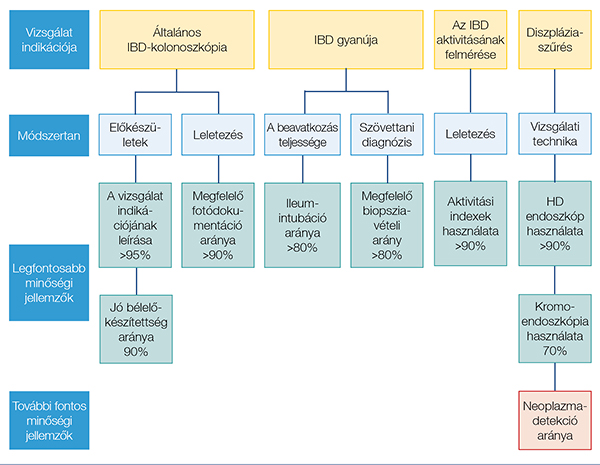
Mennyiben tér el az az ajánlás a nem IBD-ben végzett endoszkópos minőségi mutatóktól? Több annál. Mindenképpen több az ileumintubáció fontosságának hangsúlyozásával, az aktivitási pontrendszerek alkalmazásának kiemelésével, valamint az adekvát helyről, megfelelő számban vett biopszia jelentőségének említésével. A többi mutató – a bélelőkészítés, a fotódokumentáció, a megfelelően strukturált endoszkópos lelet, a megfelelő endoszkópok és technikák alkalmazása, illetve a neoplazma-detekciós arány – megfeleltethető az „általános” kolonoszkópos mutatóknak, a speciális betegcsoporthoz és helyzethez igazítva.
A következőkben – azok időrendi sorrendjében – három dolgot emelnék ki, melyeket különösen fontosnak érzek az IBD endoszkópiája kapcsán: 1) Bélelőkészítés; 2) Aktivitási indexek; 3) Megfelelő lelet. Miért ezt a hármat? Azért, mert 1) a bélelőkészítés kapcsán vannak eltérő szempontok és tévhitek, amelyek tömören megválaszolhatóak; 2) az aktivitási indexek alkalmazása nélkül egyazon beteg endoszkópos leletei sem összehasonlíthatóak, másik orvoshoz jutva a korábbi endoszkópos aktivitás többnyire értelmezhetetlen; 3) a nem megfelelő lelet ismételt endoszkópiákat tesz szükségessé, ha a beteg másik ellátóhelyre kerül.
Bélelőkészítés
Kell-e bélelőkészítés minden esetben?
Nyilvánvalóan a legfontosabb a kellően tiszta bél diszpláziaszűrés esetén. Ezt ne végezzük aktív bélbetegség esetén! Egyrészt az aktivitás nehezíti a diszplázia felismerését mind az endoszkópos, mind a patológus részéről, másrészt az aktív IBD rizikófaktor a nem kellő béltisztulás szempontjából is, főként szűkületes CD esetén (5). Ez utóbbi fennállásakor a bélelőkészítés komplettálhatja a subileust, emiatt célszerű a béltisztítást intézeti körülmények között, közös gasztroenterológiai-sebészeti felügyelet mellett végezni. Egyedi mérlegelést igényel, hogy az adott helyzetben mekkora a veszélye a iatrogén bélelzáródásnak, de ha már az előkészítés előtt nívók igazolhatóak, megfontolandó, hogy beöntésekkel próbáljuk tisztítani a belet – ha az endoszkópia még ebben a szituációban is indokoltnak tűnik. Ha az aktív CD nem jár szűkülettel, mindenképpen béltisztítás szükséges a hasmenéses székletszámtól függetlenül. Speciális helyzet az aktív UC, mert ebben az esetben általában a gyakori székelési ingerek, a vér- és nyákürítés kellő béltisztaságot jelent – főként a gyulladásos szegmensek területén, attól proximálisan már nem feltétlenül. Mennyi az a napi székelési inger (széklet-, vér-, nyákürítési) szám, amikor már nem szükséges, vagy akár veszélyes is lehet a béltisztítás? Saját tapasztalatból merítve, akkor nem alkalmazunk előkészítést, amikor a beteg az ingerek száma alapján már hospitalizációra szorul, vagyis hat vagy több véres nyák- és/vagy székletürítése van. A súlyos UC-t jellemző Truelove–Witts-kritériumok 60 év elteltével is bizonyítottan használhatóak, így érdemes ismételten felsorolni a hospitalizációt igénylő UC jellemzőit: legalább 6 véres nyák/széklet ürítés mellett jelentkező láz, tachycardia, anémia vagy gyorsult süllyedés (emelkedett CRP) (6). Ilyen esetben a tervezett kolonoszkópia előtti fokozott folyadékbevitel, valamint a vizsgálat előtti vacsora és reggeli kihagyása elegendő előkészületet jelent.
Milyen bélelőkészítőt használjunk?
A 2019-ben a bélelőkészítésről publikált ESGE-ajánlás egy rövid fejezetben foglalkozik az IBD-vel. Kiemeli a tökéletes bélelőkészítés fontosságát, különösen kromoendoszkópia alkalmazása esetén. Ez nyilvánvalóan legalább ilyen fontosságú lesz az újabb, az endoszkópiát a mikroszkóppal kombináló eljárások alkalmazása esetén a közeljövőben. Az ESGE polietilénglikol- (PEG-) alapú, alacsony vagy magas térfogatú (1 vagy 2 liter) bélelőkészítést javasol IBD-ben annak típusától, lokalizációjától, illetve aktivitásától függetlenül (7). Ez a nem IBD-s páciensek randomizált kontrollált vizsgálatain alapul, ahol nátrium-pikoszulfát (NPS) alkalmazása mellett 10-szer gyakoribb volt az enyhe bélgyulladás, mint PEG esetében (8). Bár az ajánlás „strong recommandation with high quality evidence”, megszületésének időpontjában nem állt rendelkezésre adat, amelyben az NPS hatékonyságát és biztonságosságát vizsgálták volna IBD-ben, valamint olyan sem, ahol összehasonlították volna a kétféle bélelőkészítőt. Az egyetlen, ebben a témában 2017-ben publikált metaanalízis, amelyet az ajánlás során is citáltak, a különböző térfogatú PEG-ek összehasonlításán túl a szenna hatékonyságát vizsgálta (9).
Az ESGE ajánlása óta eltelt időben több, ha nem is nagyszámú közlemény jelent meg ebben a témakörben. Az ezeket az adatokat összehasonlító metaanalízis nem talált különbséget a hatékonyság és a biztonságosság szempontjából a PEG- és az NPS-alapú bélelőkészítők között IBD-ben (10). Azonban a tolerabilitás és a kedvezőbb mellékhatásprofil az NPS-alapú bélelőkészítők alkalmazása mellett szólt (11). A hazánkban jelenleg forgalomban lévő NPS-alapú bélelőkészítők közül egyedül a Citrafleet (Goodwill Pharma) IBD-ben való alkalmazásáról vannak publikált adataink (12). A tanulmányban vizsgált 233 beteg 28,33%-a volt IBD-s. A kolonoszkópos előkészítés tolerálhatóságát egy tízpontos skálán átlagosan 8,71±1,80 pontra értékelték. Ezt a nem (férfi 8,88±1,59 vs. nő 8,55±1,96), az életkor (60 év alattiak 8,61±1,87 vs. 60 év felettiek 8,83±1,79), a korábbi többszörös hasi műtét (nincs műtét 8,74±1,76 vs. többszörös műtét 8,54±2,02), a korábbi bélreszekció (bélreszekció nélkül 8,70±8,70±2,02 1,79 vs. bélreszekció után 8,76±1,89) és az IBD jelenléte (IBD nélkül 8,76±1,77 vs. IBD esetén 8,57±1,88) nem befolyásolta. Adataink alapján a Citrafleet hatékonyan és biztonságosan alkalmazható bármilyen korú és társbetegségekkel rendelkező, akár korábban bélreszekciós műtéten átesett IBD esetén. Mindemellett ugyanezen bélelőkészítővel végzett vizsgálataink azt is kimutatták, hogy a szerrel végzett bélelőkészítés bélflórára kifejtett hatása átmeneti, és négy héten belül rendeződik az IBD mindkét formájában (13).
Aktivitási indexek
Mikor alkalmazzunk aktivitási indexeket?
Minden alkalommal, amikor IBD-ben szenvedő beteget vizsgálunk, akkor is, ha nincs szemmel látható aktivitás. A nyálkahártya-gyógyulás tökéletessége a hosszú távú kedvező betegséglefolyás alapja, nem mindegy egy UC-s beteg esetén, hogy a nyálkahártyakép Mayo 0 vagy 1. Ez csupán a leírás alapján, pontok nélkül az esetek többségében nem állapítható meg, nem is beszélve arról, hogy az aktivitás súlyossága sem mérhető fel az indexek használata nélkül. Az endoszkópos lelet értékét, komparabilitását a pontok alkalmazása biztosítja, ezáltal megkímélhetjük a beteget egy rövid időn belül elvégzett ismétlő vizsgálattól. Ezt tovább fokozhatjuk az adekvát fotó- és/vagy videodokumentációval.
Milyen aktivitási indexeket alkalmazzunk?
UC-ben mind a Mayo-index, mind az UCEIS (Ulcerative Colitis Endoscopic Index of Severity) alkalmazható. Nagyon fontos, hogy az endoszkópos súlyosság bélszakaszonként változó lehet, és a kiterjedés mértéke korrelál a betegség súlyosságával. Emiatt javasoljuk a panMayo pontrendszer alkalmazását, amely során a vastagbél öt szegmensében szegmensenként meg kell adni az adott szakaszra jellemző Mayo-pontot (ascendens, transversum, descendens, sigma, rectum), majd ezt aktivitás esetén (minimum egy szegmensben legalább 2 Mayo-pontszám) 3-mal megszorozva kapjuk meg a végső pontszámot. Mi értelme van a szorzásnak? Az, hogy így pontszámban elkülönül egymástól az inaktív és az aktív betegség. Ha a betegnek aktív proctitise van közepes súlyossággal, 2-es Mayo-pontszámmal, akkor a panMayo érték 6. Ez magasabb, mintha pancolitis esetén csaknem komplett nyálkahártya-gyógyulásnál minden szegmensben foltos hyperaemia lenne, Mayo 1 minden szegmensben. Mivel nincs aktivitás, nem kell a szorzás, így az összpontszám 5, amely alacsonyabb, mint az előbbi aktív proctitis esetén (14). A panMayo-pontok alapján meghatározható endoszkópos súlyossági beosztást a 2. táblázatban ábrázoljuk.
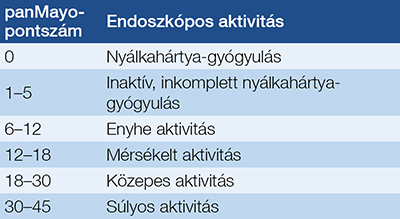
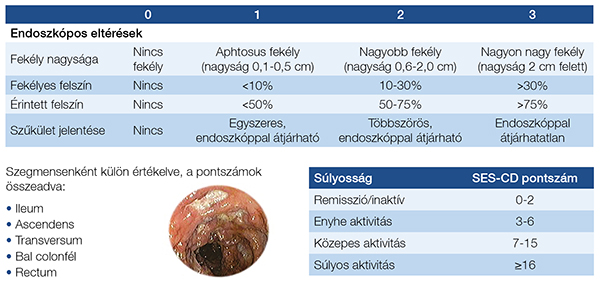
Vizsgálataink alapján a panMayo-pontszám jól korrelál az endoszkópiát követő komplikált betegségkimenetellel, a szövődményekkel, műtéti igénnyel is (15). CD-ben általánosan elfogadott a SES-CD (Simple Endoscopis Score of Crohn’s Disease) alkalmazása (16), amely szintén szegmensenként pontozza az aktivitást a gyulladásos terület kiterjedése és a fekélyek nagysága alapján (4. ábra).
Az endoszkópos lelet IBD-ben
A kolonoszkópia diagnosztikus értéke a jól megírt lelettel válik teljessé. Ha a betegség kiterjedése, súlyossága, esetleges diszplasztikus léziók jelenléte nem egyértelmű a terápiás döntéshozó számára, az ismételt vizsgálatra kényszerül, amely a beteg számára jelentős terheléssel jár, és fokozza a szövődmények lehetőségét is. A leletnek tartalmaznia kell az endoszkópia előtti adatokat, a nyálkahártya és a vizsgálat alatt végzett beavatkozások minél pontosabb leírását és az endoszkópia során látott eltérések következményeit, a terápiás és utánkövetési javaslatokat (17) (3. táblázat).
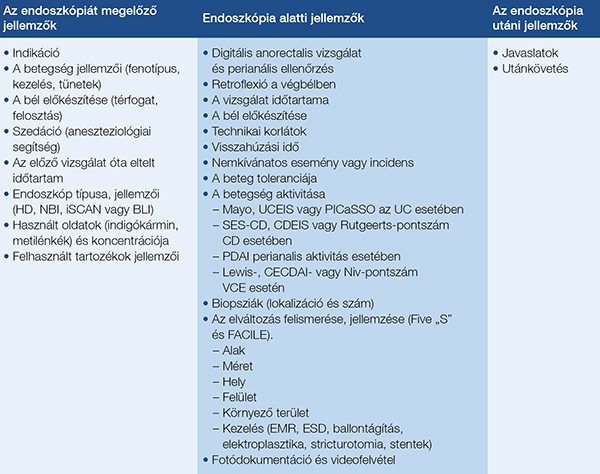
Összefoglalva az endoszkópos leletben világosan és tömören le kell írni minden lényeges orvosi és endoszkópos technikai információt, elváltozást, terápiás beavatkozást, szövődményt, mellékhatást, összefoglaló véleményt, és ezek alapján javaslatokat megfogalmazni a terápiás következményekre, valamint a következő vizsgálat időtartamára (5. ábra).

Összefoglalás
Az IBD-ben elvégzett vastagbéltükrözés kapcsán kiemelt fontosságú, hogy tisztában legyünk azzal, hogy már a vizsgálat előkészítése is eltérő lehet. Nem mindig van szükség, illetve lehetőség a béltisztításra, de ha igen, akkor a tolerabilitás szempontjából az NPS-alapú bélelőkészítők preferálandóak. Fontos, hogy a vizsgálat során értékeljük az aktivitást objektív módon pontrendszerekkel, és a leletezés során egy nyelvet használjunk. Úgy írjuk meg a leletet, hogy aki azt olvassa, a mi szemünkkel lásson!
Irodalom
https://doi.org/10.25122/jml-2018-0075 PMID: 31406511;
PMCID: PMC6685307.
2. Pal P, Reddy DN. Interventional endoscopy in inflammatory bowel disease: a comprehensive review. Gastroenterol Rep (Oxf). 2024 Jul 25; 12: goae075. https://doi.org/10.1093/gastro/goae075 PMID: 39055373;
PMCID: PMC11272179.
3. Hong SM, Baek DH. Diagnostic Procedures for Inflammatory Bowel Disease: Laboratory, Endoscopy, Pathology, Imaging, and Beyond. Diagnostics (Basel). 2024 Jun 28; 14(13): 1384.
https://doi.org/10.3390/diagnostics14131384 PMID: 39001273;
PMCID: PMC11241288.
4. Dekker E, Nass KJ, Iacucci M, Murino A, Sabino J, Bugajski M, et al. Performance measures for colonoscopy in inflammatory bowel disease patients: European Society of Gastrointestinal Endoscopy (ESGE) Quality Improvement Initiative. Endoscopy. 2022 Sep; 54(9): 904–915.
https://doi.org/10.1055/a-1874-0946 Epub 2022 Jul 29. PMID: 35913069.
5. Kumar A, Shenoy V, Buckley MC, et al. Endoscopic Disease Activity and Biologic Therapy Are Independent Predictors of Suboptimal Bowel Preparation in Patients with Inflammatory Bowel Disease Undergoing Colonoscopy. Dig Dis Sci 2022; 67: 4851–4865.
https://doi.org/10.1007/s10620-022-07530-8
6. Truelove SC, Witts LJ. Cortisone in ulcerative colitis; final report on a therapeutic trial. Br Med J 1955 Oct 29; 2(4947): 1041–8.
https://doi.org/10.1136/bmj.2.4947.1041 PMID: 13260656;
PMCID: PMC1981500.
7. Hassan C, East J, Radaelli F, Spada C, Benamouzig R, Bisschops R, et al. Bowel preparation for colonoscopy: European Society of Gastrointestinal Endoscopy (ESGE) Guideline – Update 2019. Endoscopy 2019 Aug; 51(8): 775–794. https://doi.org/10.1055/a-0959-0505 Epub 2019 Jul 11.
PMID: 31295746.
8. Lawrance IC, Willert RP, Murray K. Bowel cleansing for colonoscopy: prospective randomized assessment of efficacy and of induced mucosal abnormality with three preparation agents. Endoscopy 2011 May; 43(5): 412–8. https://doi.org/10.1055/s-0030-1256193 Epub 2011 May 4.
PMID: 21547879.
9. Restellini S, Kherad O, Bessissow T, Ménard C, Martel M, Taheri Tanjani M, et al. Systematic review and meta-analysis of colon cleansing preparations in patients with inflammatory bowel disease. World J Gastroenterol 2017 Aug 28; 23(32): 5994–6002.
https://doi.org/10.3748/wjg.v23.i32.5994 PMID: 28932092;
PMCID: PMC5583585.
10. Chatterjee A, Kaur S, Jena A, Patil AN, Dutta U, Sebastian S, Sharma V. Strategies to Improve Colonoscopy Preparation in Inflammatory Bowel Disease. A Systematic Review and Network Meta-analysis of Randomized Trials. J Gastrointestin Liver Dis 2024 Jun 29; 33(2): 245–253.
https://doi.org/10.15403/jgld-5433 PMID: 38944852.
11. Briot C, Faure P, Parmentier AL, Nachury M, Trang C, Viennot S, et al.; CLEAN Study Group. Efficacy, Tolerability, and Safety of Low-Volume Bowel Preparations for Patients with Inflammatory Bowel Diseases: The French Multicentre CLEAN Study. J Crohns Colitis 2019 Sep 19; 13(9): 1121–1130. https://doi.org/10.1093/ecco-jcc/jjz040 PMID: 30785181.
12. Bor R, Matuz M, Fabián A, Szepes Z, Szántó K, Farkas K, et al. Efficacy, tolerability and safety of a split-dose bowel cleansing regimen of magnesium citrate with sodium picosulfate – A phase IV clinical observational study. Rev Esp Enferm Dig 2021 Sep; 113(9): 635–642.
https://doi.org/10.17235/reed.2020.7073/2020 PMID: 33371690.
13. Bacsur P, Rutka M, Asbóth A, Resál T, Szántó K, Jójárt B, et al. Effects of bowel cleansing on the composition of the gut microbiota in inflammatory bowel disease patients and healthy controls. Therap Adv Gastroenterol 2023 Jun 6; 16: 17562848231174298.
https://doi.org/10.1177/17562848231174298 PMID: 37324319; PMCID: PMC10265323.
14. Bálint A, Farkas K, Szepes Z, Nagy F, Szűcs M, Tiszlavicz L, et al. How disease extent can be included in the endoscopic activity index of ulcerative colitis: the panMayo score, a promising scoring system. BMC Gastroenterol 2018 Jan 8; 18(1): 7.
https://doi.org/10.1186/s12876-017-0725-3 PMID: 29310593; PMCID: PMC5759871.
15. Bacsur P, Wetwittayakhlang P, Resál T, Földi E, Vasas B, Farkas B, et al. Accuracy of the Pancolonic Modified Mayo Score in predicting the long-term outcomes of ulcerative colitis: a promising scoring system. Therap Adv Gastroenterol 2024 Mar 21; 17: 17562848241239606.
https://doi.org/10.1177/17562848241239606 PMID: 38524790;
PMCID: PMC10958809.
16. Daperno M, D’Haens G, Van Assche G, Baert F, Bulois P, Maunoury V, et al. Development and validation of a new, simplified endoscopic activity score for Crohn’s disease: the SES-CD. Gastrointest Endosc 2004 Oct; 60(4): 505–12. https://doi.org/10.1016/s0016-5107(04)01878-4
PMID: 15472670.
17. Adamina M, Feakins R, Iacucci M, Spinelli A, Cannatelli R, D’Hoore A, et al. ECCO Topical Review Optimising Reporting in Surgery, Endoscopy, and Histopathology. J Crohns Colitis 2021 Jul 5; 15(7): 1089–1105.
https://doi.org/10.1093/ecco-jcc/jjab011 PMID: 33428711.
